Что такое мпз: МПЗ в бухгалтерском учете — понятие и состав
МПЗ — это… Что такое МПЗ?
МПЗметод микропотенциал-зонда
геофиз.
физ.
Источник: [email protected]
МПЗМалоярославецкий приборный завод
Словарь: С. Фадеев. Словарь сокращений современного русского языка. — С.-Пб.: Политехника, 1997. — 527 с.
МПЗмясоперерабатывающий завод
МПЗмагнитное поле Земли
Словарь: С. Фадеев. Словарь сокращений современного русского языка.
механизм привода закрылков
авиа
Словарь: Словарь сокращений и аббревиатур армии и спецслужб. Сост. А. А. Щелоков. — М.: ООО «Издательство АСТ», ЗАО «Издательский дом Гелеос», 2003. — 318 с.
мпзмиллипьеза
МПЗмусороперерабатывающий завод
МПЗматериально-производственные запасы
бухг.
фин. МПЗмногофункциональный пропалыватель Задворнова
сельскохозяйственный инструмент для обработки почвы
в маркировке, сельхоз.
Источник: http://www.yartpp.ru/index.php?option=com_content&view=article&id=44032&Itemid=98&lang=ru
МПЗмедиальная префронтальная зона
псих.
Источник: http://www.nanonewsnet.ru/articles/2012/deistvie-gallyutsinogenykh-gribov-vpervye-issledovali-s-pomoshchyu-mrt?utm_campaign=subscribe_techno&utm_medium=email&utm_source=subscribe
международно-правовая защита
радио
связь, юр.
Источник: http://www.grfc.ru/index.phtml?page=134&tbl=tb_92&id=157&vview=169
МПЗмачтопропиточный завод
Источник: http://www. eprussia.ru/epr/60/3963.htm
eprussia.ru/epr/60/3963.htm
Пример использования
Котельничский МПЗ (Кировская обл.)
МПЗмини-перерабатывающий завод
мини-завод по переработке нефти
энерг.
Источник: http://www.gosnadzor.ru/news_otr/122006/no241206.html
МПЗ международно-правовая защита
международная правовая защита
юр.
МПЗМосковский прожекторный завод
ЗАО
http://www. mpz-projector.ru/
mpz-projector.ru/
Источник: http://www.expert.ru/rus_business/2006/07/prozhektorniy_zavod/
МПЗмеханизмы психологической защиты
мед.
Источник: http://terramedica.spb.ru/4_2004/uljukin.htm
МПЗмиелопролиферативные заболевания
мед.
Источник: http://hematology.ph-dynasty.ru/docs/pdf_articles/hematology/2003_4/046-050Vladimirskaya.pdf
Словарь сокращений и аббревиатур. Академик. 2015.
Материально-производственный запас организации: что входит в его состав, классификация МПЗ
Производственные запасы – это основа для всего оборота компании.
В процессе производства большая часть материально-производственных запасов применяется в качестве предметов труда. В каждом производственном цикле (период с момента запуска производственного процесса до момента выхода готового продукта) они целиком потребляются.
Кстати, цикл – в данном случае является определяющим понятием. Ведь лишь те объекты, которые полностью утрачиваются, и относятся к обсуждаемой теме. Другими словами, это расходные ресурсы, сырье, катализаторы процедуры, которые тратятся.
В отличие от многоцикличных предметов, например, оборудования, станка. Ведь его срок жизни на предприятии определяется не циклом, а сроком годности, который теоретически и может быть равен или даже менее длителен, чем диапазон цикла, но все же в него не входит.
Понятие и классификация материально-производственных запасов
Чтобы понять суть этого термина, достаточно уяснить тот факт, что это расходники. То есть предметы, которые свою совокупную стоимость полностью теряют, отдают конечному продукту. Который и является товаром, итогом всего процесса. Выходит, именно эти элементы представляют собой основную строку расходов – а значит, себестоимости. Конечно, сюда еще следует добавить множество иных источников трат, как транспортировка, оформление, оплата пошлин и налогов за исключение НДС.
То есть предметы, которые свою совокупную стоимость полностью теряют, отдают конечному продукту. Который и является товаром, итогом всего процесса. Выходит, именно эти элементы представляют собой основную строку расходов – а значит, себестоимости. Конечно, сюда еще следует добавить множество иных источников трат, как транспортировка, оформление, оплата пошлин и налогов за исключение НДС.
Второй аспект, который определяет термин – это однократность. Они участвуют в производстве лишь один раз. Даже если после цикла сохранились остатки, это всего лишь означает, что не все ресурсы были задействованы. Но после того как материал один раз участвует в создании изделия, он уже не может быть использован повторно.
Логично предположить, что это в первую очередь сырье. Из которого и создают товар. Но помимо него есть еще множество различных объектов, которые, так или иначе, задействованы в цикле. Если говорить о МПЗ, понятия и классификация существуют различные. Но главный способ группировки всегда один – деление на основные и вспомогательные. Далее можно классифицировать по роли в процессе, по техническим характеристикам и иным параметрам. Но всегда выделяют главные запасы, которые формируют будущий продукт, и вспомогательные. Далее можно классифицировать по роли в процессе, по техническим характеристикам и иным элементам. Но всегда выделяют основные запасы, которые и формируют будущий продукт, и вспомогательные. Они напрямую не становятся частью товара, но без них процедура все равно будет невозможна.
Далее можно классифицировать по роли в процессе, по техническим характеристикам и иным параметрам. Но всегда выделяют главные запасы, которые формируют будущий продукт, и вспомогательные. Далее можно классифицировать по роли в процессе, по техническим характеристикам и иным элементам. Но всегда выделяют основные запасы, которые и формируют будущий продукт, и вспомогательные. Они напрямую не становятся частью товара, но без них процедура все равно будет невозможна.
Что данная категория включает в себя
В первую очередь — основные резервы. Это сырье, которое становится частью продукта. Примечательно, что такое понятие чаще применяют, если речь идет о сельскохозяйственной продукции. В остальных случаях принято именовать основу – материалами. Источники могут быть разнообразные. Одни товары создаются буквально из парочки наименований, для других нужны десятки или даже сотни видов. Далее запчасти. То есть некоторые элементы, которые входят в его состав, но не создаются на производстве либо в принципе участвуют в ином цикле.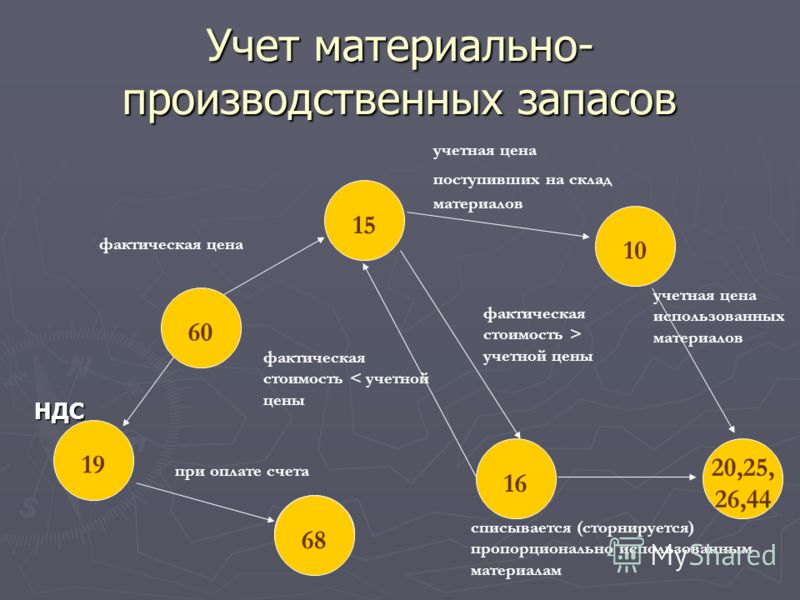
Еще в состав материальных запасов включаются дополнительные объекты. Они необходимы для работы, но не из них создается изделие. Они могут напрямую влиять как вещества для нанесения маркеров, так и не затрагивать его в целом. Например, расходники для обслуживания имущества, содержания его, защиты от внешней среды, тара, упаковочные предметы, даже спецодежда. При этом стоит строго отделять упаковки, которые являются частью товара, и те, которые относятся к дополнительным элементам. Так, стеклянная тара, в которой содержатся корнишоны – это часть продукции. А вот картонная коробка, в которой производится транспортировка, а также скотч, с помощью которого ящики фиксируются – это уже дополнительные объекты.
Классификация
Фактически к материально-производственным запасам относят практически все на площадке, помимо человеческих ресурсов и оборудования. Зачастую, если говорить про техническую градацию, то выделяют следующие виды:
Зачастую, если говорить про техническую градацию, то выделяют следующие виды:
- Сырье или материалы, как уже отмечалось, зависит от специфики хозяйствующего субъекта.
- Полуфабрикаты. Причем приобретенные извне. То есть созданные не на этой площадке. И даже если существует другой завод, который также является частью этой компании, поставляет полуфабрикаты, они все равно считаются приобретенными.
- Запасные элементы.
- Топливо. Они используются для обеспечения энергией оборудование, транспортировочные средства.
- Инвентарь. Вне зависимости от ценового фактора и габаритов.
- Тара. А также иной способ содержания, упаковки, переноса предметов.
- Специальная одежда и оснащение сотрудников. Включая защитные приборы, которые используются единожды.
Стоит понимать, наиболее полный состав производственных запасов – это больший список, а здесь даны лишь его верхние категории. Каждая из них на конкретном предприятии обычно подразделяется еще на десятки пунктов. Да и третий уровень разделение вполне может иметь место. Поэтому зачастую корректно систематизировать весь этот массив бывает весьма проблематично. Приходится использовать строгий регламент учета, постоянно вносить данные, а также своевременно проводить различные проверки. В части — инвентаризацию и аудит, чтобы сверить фактическое наличие предметом труда с документарным.
Да и третий уровень разделение вполне может иметь место. Поэтому зачастую корректно систематизировать весь этот массив бывает весьма проблематично. Приходится использовать строгий регламент учета, постоянно вносить данные, а также своевременно проводить различные проверки. В части — инвентаризацию и аудит, чтобы сверить фактическое наличие предметом труда с документарным.
Основные
Итак, что относится к таким МПЗ. Это все активы оборотного капитала, которые используются для создания товара. Два ключевых фактора, необходимых для производства – МПЗ и человеческий труд.
Вспомогательные
Все, что нужно для бесперебойной работы производственного процесса. Но при этом не участвующее в создании. Зачастую большая часть этих предметов используется для хранения, транспортировки, защиты. А также самих сотрудников, задействованных в работе.
Для наглядности оформим это так:
Основа | Вспомогательные |
Сырье | Топливо |
Материалы | Тара |
Полуфабрикаты | Инвентарь |
Комплектующие | Упаковочные элементы |
Градация по техническим признакам
Эти элементы не принято разделять по качеству, стоимости. Главный аспект – предназначение. Но также часто разделение допускается по техническим аспектам. Горючие вещества относятся к одной категории, пластиковый инвентарь к другой, металлический – к третьей. Габариты такой классификации целиком и полностью зависят от того, сколько на конкретном производстве используется различных предметов. Разделяются по техническим признакам не только вспомогательные, но и основные.
Главный аспект – предназначение. Но также часто разделение допускается по техническим аспектам. Горючие вещества относятся к одной категории, пластиковый инвентарь к другой, металлический – к третьей. Габариты такой классификации целиком и полностью зависят от того, сколько на конкретном производстве используется различных предметов. Разделяются по техническим признакам не только вспомогательные, но и основные.
Следует знать и про особую группу. В состав материалов включаются МБП. Дословно – это малоценные или быстроизнашиваемые объекты. То, что будет относиться к первым – это вопрос сложный. По сути, определяется сначала стоимость, и в сравнительной характеристике уже выявляются малоценные. Так, все зависит от сырья на предприятии. А вот объекты, которые быстро изнашиваются, – это имущество со сроком службы менее года. Естественно, что цикл на большинстве предприятий будет куда короче. Но все же такие быстроизнашиваемые нерасходные части принято выносить в МПЗ.
Особенности
Так, теперь кратко выявим отличительные черты.
- Срок жизни – один цикл.
- Полностью утрачивают собственную ценность.
- Переносят свою стоимость на себестоимость конечного товара.
- Являются главной для создания изделия или хранения его на складе.
Номенклатура и единица бухгалтерского учета
Как уже упоминалось, принципиально важно вести полный учет всех средств, которые используются в производственном цикле. При этом каждому конкретному объекту присваивается свой номер. Общая информация вносится в номенклатуру, то есть в список основных материалов, которые были задействованы.
Все информация фиксируется до этапа создания и после него. Сверяются расхождения, выявляются излишки средств и недостатки. Ведь по техническому регламенту строго отмечается, сколько номенклатурных единиц затрачивается на создание того или иного товара. Ведь МПЗ – это производственные запасы организации, и если не вести строгий контроль, то появится неучтенный перерасход. А также возможное хищение на предприятии, что прямым образом скажется на конечной прибыли и финансовой устойчивости организации.
Отражение в балансе
Вне зависимости от того, для чего конкретно полученный товар будут предназначаться в деятельности хозяйствующего субъекта, он всегда учитывается в бухгалтерском балансе по ключевому фактору. Это себестоимость, совокупность фактических затрат, которые понесла компания. Зачастую проблем с определением нет, ведь договор купли-продажи с контрагентом легко предоставляет всю необходимую информацию.
Другой момент в том, что в состав материально-производственных запасов включают те, которые уже успели потерять свою стоимость. Например, в процессе транспортировки. Или устарели, были исключены из оборота. Тогда главной оценкой станет уже цена продажи, а не закупочная.
А кроме того, некоторые материалы, полученные не с помощью договора купли-продажи. В первом случае – это прямое внесение от учредителей в форме пополнения капитала. При оприходовании стоит руководствоваться ценовыми рекомендациями самих учредителей. А также часто имеют место случаи безвозмездной поставки. В форме акции, как вариант. Тогда для оприходования нужно будет вычислить текущую на момент приема рыночную цену и ориентироваться на нее. Причем, если оценка потребует дополнительных денежных затрат, как оплата работы эксперта-оценщика, эти расходы также относятся в счет себестоимости полученной продукции.
В форме акции, как вариант. Тогда для оприходования нужно будет вычислить текущую на момент приема рыночную цену и ориентироваться на нее. Причем, если оценка потребует дополнительных денежных затрат, как оплата работы эксперта-оценщика, эти расходы также относятся в счет себестоимости полученной продукции.
Оценка
Существуют два основных варианта, как можно оценить поставку. Первый способ – смотреть на учетную цену. Второй – на закупочную стоимость. Обычно производственные запасы организации входят (включаются) в состав общих поставок. Наряду со всеми остальными товарами, которые получает компания.
Учетная цена
Другими словами, в расчет берется цена объекта, которая была занесена в бухгалтерский лист контрагента. Чаще всего метод используется, если контрагента нет, а организация поставляет материал напрямую от собственного филиала или второй производственной площадки.
Учет по фактическим затратам
В этом случае придется выявить суммы всех расходов, которые были направлены на получение товара. А их источники могут быть самые различные. Причем часть расходов, которые связаны с непредвиденными ситуациями не относятся к изначальной стоимости, а уходят на баланс издержек при транспортировке, например.
А их источники могут быть самые различные. Причем часть расходов, которые связаны с непредвиденными ситуациями не относятся к изначальной стоимости, а уходят на баланс издержек при транспортировке, например.
Слагаемые себестоимости
Итак, давайте более конкретно рассмотрим, как же можно понять, сколько денежных трат понесло предприятие. Чтобы вписать каждую полученную товарную единицу, при оприходовании нужно выявить совокупную цифру, которая учитывает расходы вне зависимости от источника. Ведь запасы в производстве – это статья, которая нуждается в повышенном контроле.
- Непосредственная оплата поставщику. То есть, исполнение своих договорных обязательств по сделке купли-продажи. Размер вычисляется, естественно, по цене, прописанной в начальном договоре.
- Различные торговые пошлины, которые были добавлены. Их объемы уже зависит от логистики. От того, какой путь прошел товар, пока не был доставлен на производственную площадку.
- Цена доставки.

- Налоги, которые не были возвращены.
- Затраты на различные консультационные, охранные и иные услуги. Которые могли потребоваться в процессе доставки.
- Стоимость оплаты труда наемных работников, которые проводили погрузку, выгрузку, сортировку на складе.
- Оплата услуг посредников.
Это примерный список. В каждом конкретном случае он может дополняться, становиться больше или меньше. Все зависит от длины и сложности пути, который прошел товар.
Учет запасов
Учитывая тот факт, что любые потери по этой статье несут крупные убытки вплоть до остановки производства, контролировать наличие необходимо всеми путями. Это постоянные проверки наличия нужных единиц на местах, а также построение грамотной стратегии расходования. Другими словами, нужно постоянно знать, сколько осталось расходников и как их правильно применять.
И для этой задачи полезными окажутся программные продукты от «Клеверенс». Они позволяют упростить оба процесса до элементарной составляющей. Умные программы знают, что входит в производственные запасы, как их правильно учитывать, заносить на баланс. В пару кликов делают работу, на которую ушли бы часы. Причем ПО и оборудование адаптируются под любую специфику. И в отличие от многих аналогов прекрасно адаптированы конкретно под наше законодательство и требования по бухгалтерской и налоговой отчетности.
Умные программы знают, что входит в производственные запасы, как их правильно учитывать, заносить на баланс. В пару кликов делают работу, на которую ушли бы часы. Причем ПО и оборудование адаптируются под любую специфику. И в отличие от многих аналогов прекрасно адаптированы конкретно под наше законодательство и требования по бухгалтерской и налоговой отчетности.
Например, можно выбрать специализированный софт для терминалов сбора данных со встроенным сканером штрихкода «Склад 15». Он предназначен для автоматизации всех товароучетных операций на складах, обычных и адресного хранения. Можно проводить такие операции как инвентаризация, приход на склад, а также работать с ячейками и подобрать заказы.
Аудит
Это не только проверка наличия, но также и выявление правильных условий хранения, целевой эксплуатации, корректного расхода. Проверяется, как сотрудники обращаются с ресурсами, грамотно ли они их расходуют, в каких условиях объекты содержатся на складе. Не повредит ли такое хранение их дальнейшим эксплуатационным характеристикам.
Анализ
Аналитическая работа зачастую проводится очень обширная. За начальные точки берутся такие данные, как средняя величина всех ценностей, их темпы роста или снижения, ключевые точки резкого изменения величины и объемов производства. Выявляется, как качество МПЗ влияет на длительность оборота, какие конкретно позиции в настоящий момент наиболее важны для компании, где нужно проводить дополнительную закупку.
Вся эта работа очень объемная, но как уже говорилось, продукты от «Клеверенс» позволят ее значительно упростить. Ведь приложения компании уже знают все основные методики расчетов, проведения развернутого анализа. Необходимо лишь забить нужные цифры.
С какой целью создают запасы
Достаточно вдуматься, что входит в МПЗ, чтобы ответить на подобный вопрос. Ведь если на предприятии на данный момент нет определенных объемов сырья, расходников, то цикл продолжать невозможно. При этом в случае различных ЧП, стоит понимать, что возможна задержка поставки новых товаров. А если подобное случается, площадка должна все равно некоторое время работать в штатном режиме, просто используя остатки.
А если подобное случается, площадка должна все равно некоторое время работать в штатном режиме, просто используя остатки.
Количество показов: 6155
Налоговый учет материально-производственных запасов | Бухгалтерия ПРОФ
Налоговый учет материально-производственных запасов предприятия
Материально-производственные запасы присутствуют на балансе любого предприятия. Правильно оценить их стоимость, значит, избавить себя от лишних претензий налоговых органов, не переплачивая при этом лишние деньги.
Что такое МПЗ?
Под МПЗ или материально-производственными запасами фирмы понимают следующее её имущество:
- активы, использующиеся при осуществлении производственной деятельности. Сюда включают сырьё, полуфабрикаты и комплектующие, материалы, необходимые для изготовления продукции, выполнения работ или оказания услуг, и переносящие свою ценность на стоимость готового продукта;
- готовые продукты, в том числе товары, предназначенные для реализации;
- вспомогательные материалы, включая упаковку, горючее и энергетические ресурсы, запчасти, инвентарь, спецодежду и т.п.
Из чего складывается стоимость МПЗ?
При ведении налогового учета, ценность материально-производственных запасов будет складываться из цены, которую пришлось уплатить фирме, и трат, связанных с приобретением: расходов на доставку, комиссий, пошлин и др.
МПЗ, купленные в иностранной валюте, не будут включать в свою стоимость разницу курса валют, т.к. данные затраты причисляются к внереализационным расходам/доходам. Точно так не относятся к стоимости и проценты по обязательствам, которые были получены с целью приобретения МПЗ.
НДС не причисляется к тратам компании на МПЗ, исключая те фирмы, что избавлены от уплаты налога на добавленную стоимость. В случае если МПЗ были получены организацией безвозмездно или после демонтажа/ремонта собственных ОС, их ценность будет равняться рыночной цене.
Запасы, поступившие от учредителей в качестве вклада в уставной капитал фирмы, принимаются по чекам и иным документам покупки данных ценностей, а при их отсутствии – по результатам независимой оценки. Если учредителем является юридическое лицо, стоимость активов принимается по данным налогового учета компании-учредителя.
Ценность МПЗ, полученных по договору обмена, приравнивается к ценности переданного по данному договору имущества.
Списанные МПЗ и их налоговый учет
Ценность списанных запасов может быть рассчитана по средней себестоимости или по себестоимости единицы.
Второй способ отличается высокой трудоемкостью и может быть использован в организациях с малой и неизменной номенклатурой МПЗ или там, где специфика оценки МПЗ характеризуется особым штучным порядком.
Большей же популярностью пользуется метод определения стоимости по средней себестоимости, равной отношению себестоимости определенной группы запасов к их количеству в данной группе.
Списание данных активов по средней себестоимости предполагает:
- Отражение выбранного способа в учетной политике фирмы;
- Формирование учета, позволяющего точно определять: группы и типы запасов при проведении рабочей аналитики, количество МПЗ при их оприходовании и отпуске в производство, себестоимость определенной партии;
- Закрепление метода определения средней себестоимости во внутренних регламентах фирмы.
Не нужно напоминать, что все операции, в которых участвуют материально-производственные запасы, должны иметь документальное подтверждение.
Читайте другие статьи «Бухгалтерии ПРОФ», чтобы освежить в памяти такие моменты, как бухгалтерский и налоговый учет банковских гарантий, налоговый учет финансовых вложений, постановка на налоговый учет физического лица и другое.
Появились дополнительные вопросы? Закажите обратный звонок, и мы свяжемся с Вами сами!
Товарно-материальные ценности | 1С:Бухгалтерия 8
Учет товаров, материалов и готовой продукции реализован согласно ПБУ 5/01 «Учет материально-производственных запасов» и методическим указаниям по его применению.
Аналитический учет запасов на счетах учета в программе всегда ведется по номенклатурным позициям (наименованиям товаров, материалов, продукции). Кроме этого, дополнительно может быть установлен аналитический учет запасов по партиям и по складам (по количеству или по количеству и сумме).
Настройки учета запасов едины для целей бухгалтерского и налогового учета. Для внешнеторговых операций поддерживается учет таможенных деклараций и страны происхождения товара.
Автоматизированы операции поступления и списания товарно-материальных ценностей (ТМЦ). Можно оформить перемещение ценностей между складами, продажу, передачу в производство.
Поддерживаются способы оценки материально-производственных запасов (МПЗ) при их выбытии:
- по средней себестоимости;
- по себестоимости первых по времени приобретения материально-производственных запасов (способ ФИФО).
Самым простым по реализации является способ — по средней себестоимости. Данный способ не требует ведения учета по партиям. При использовании способа ФИФО обязательно ведется партионный учет. Различные способы оценки могут применяться независимо для каждой организации. При этом в бухгалтерском и налоговом учете конкретной организации способы оценки МПЗ совпадают.
Предусматривается проведение инвентаризаций товарно-материальных ценностей в разрезе складов и материально-ответственных лиц. По результатам инвентаризации автоматически подсчитывается разница между учетным количеством и фактическим количеством ценностей, выявленным в результате инвентаризации. На основании выполненной инвентаризации можно автоматически сформировать документы списания или оприходования.
Предусмотрена возможность комплектации и разукомплектации ТМЦ. Автоматизированы операции по учету возвратной многооборотной тары. Учтена специфика налогообложения таких операций и расчетов с поставщиками и покупателями. Ведется количественно-суммовой учет поступлений, отгрузок и остатков возвратной тары в разрезе контрагентов.
Предусмотрен учет спецодежды, спецоснастки, хозяйственного инвентаря. Стоимость спецодежды может быть списана единовременно или в течение срока эксплуатации. Учет ведется в разрезе материально-ответственных лиц. Информацию об остатках товаров, их поступлении и выбытии в течение определенного периода времени можно просмотреть с помощью стандартных отчетов.
Учет тары
Особым видом товарно-материальных ценностей, используемым при отгрузке и транспортировке товаров и готовой продукции, является возвратная многооборотная тара. В «1С:Бухгалтерии 8» регистрируются различные операции с возвратной многооборотной тарой: передача покупателю, возврат покупателем, получение от поставщика, возврат поставщику.
Инвентаризация
Залогом сохранности имущества организации является регулярное проведение инвентаризаций. Обеспечивается возможность проведения инвентаризации товарно-материальных ценностей в разрезе складов и материально-ответственных лиц.
Пример оформления инвентаризации
По данным инвентаризации можно распечатать типовую форму ИНВ-19 «Сличительная ведомость», ИНВ-3 «Инвентаризационная опись товаров» и другие. При выявлении излишков (недостач) товарно-материальных ценностей можно автоматически сформировать документы оприходования (списания) ценностей на основании инвентаризации.
Спецодежда и спецоснастка
Спецодежда и спецоснастка представляют собой разновидность товарно-материальных ценностей с особым порядком списания на затраты. Для каждой позиции спецодежды и спецоснастки устанавливаются параметры списания: срок полезного использования в месяцах, способ погашения стоимости в производстве (линейный, погашать стоимость при передаче в эксплуатацию, пропорционально объему продукции), способ отражения расходов в затратах.
Пример работы со спецодеждой
Стоимость спецодежды и спецоснастки может быть списана единовременно при передаче в эксплуатацию или списываться в течение срока эксплуатации. Если стоимость списывается в течение срока эксплуатации, то погашение стоимости выполняется автоматически регламентной операцией закрытия месяца.
При передаче спецодежды и спецоснастки в эксплуатацию она продолжает учитываться на специальных забалансовых счетах до момента фактического выбытия. Предусмотрена возможность возврата спецодежды и спецоснастки их эксплуатации на склад, передачи между материально-ответственными лицами, а также списания в связи с полным износом или по факту порчи.
Комплектация и разукомплектация
В производственной деятельности нередко возникает ситуация, когда, не производя каких-либо дополнительных действий или операций, необходимо составить из нескольких единиц МПЗ одну новую единицу, либо преобразовать одну единицу учета в несколько отдельных. Для создания такого рода комплектов, а также для обратной процедуры — разукомплектации набора на отдельные предметы предназначен специальный документ.
Учет поступления материально-производственных запасов | Статья в журнале «Молодой ученый»
В статье рассматривается порядок учета материально-производственных запасов в соответствии с Положением по бухгалтерскому учету «Учет материально-производственных запасов», а также Федеральным законом «О бухгалтерском учете» от 06.12.2011 № 402-ФЗ. Приведены особенности их учета в полиграфических организациях.
Ключевые слова: материально-производственные запасы, бухгалтерский учет, полиграфические организации
The article considers the procedure for accounting for inventories in accordance with the Accounting Regulations «Accounting for inventories», as well as the Federal Law «On Accounting» dated 06.12.2011 No. 402-FZ. Features of their accounting at printing enterprises are given.
Key words: inventories, accounting, printing enterprises
Предметы труда (а это в первую очередь материалы) — это обязательный элемент любого производственного процесса, одновременно со средствами труда и рабочей силой. Именно материалы являются материальной основой продукта, производимого в организации. Они подразделяются, прежде всего, на основные и вспомогательные. Какое бы не было производство, оно использует большое количество материалов. В первую очередь это относится к производственным видам экономической деятельности, поскольку именно в них происходит реальное производство, то есть производится тот или иной продукт. Наряду с этим и в организациях иных видов экономической деятельности МПЗ в общем, и материалы в частности, составляют значимую часть в имуществе. Любая организация нуждается в хозяйственных материалах, канцтоварах, запасных частях для ремонта основных средств и т. п.
Готовая, или произведенная продукция, теперь также относится к категории материально-производственных запасов. Например, в организациях торговли к МПЗ относят те товары, запасы которых достаточно значительны. Товары — это приобретенная для перепродажи готовая продукция других организаций.
Также в состав МПЗ включают часть средств труда, которые во время производства выполняют функции средств труда, но их срок службы существенно меньше, чем основных средств (менее 1 года). Это, прежде всего, инвентарь и хозяйственные принадлежности. Исходя из этого, несмотря на то, что в любой организации есть достаточно большое количество этих предметов, для целей бухгалтерского учета они относятся к оборотным средствам с упрощенными правилами учета в составе затрат на производство продукции (оказание услуг, выполнение работ).
Основой организации бухгалтерского учета являются первичные документы по поступлению и расходу производственных запасов. Предварительный, текущий и последующий контроль за движением, сохранностью и целесообразным использованием материальных ресурсов осуществляют непосредственно по первичным документам. Эти документы должны составляться в полном соответствии с требованиями Федерального закона от 06.12.2011№ 402-ФЗ «О бухгалтерском учете», обязательно содержать подписи лиц, совершивших операции [1]. Принципиально новой является норма о разработке форм первичных документов самими организациями, которые утверждаются руководителем организации. Можно полагать, что организации будут использовать в качестве основы образцы первичных документов, разработанные Росстатом, и подстраивать их в соответствии со своими потребностями.
Материалы и сырье поступают от подотчетных лиц, поставщиков, которые закупили материалы за наличный расчет, от ликвидации и списания собственного производства. Помимо этого, материально-производственные запасы могут быть получены безвозмездно и по товарообменным операциям, и внесены учредителями как их вклад в уставный капитал.
Учет материальных ценностей на синтетических счетах ведется по фактической стоимости приобретения, или же по учетным ценам.
Под учетными ценами подразумеваются плановые цены, которые установлены организациями.
Используя учет материалов по фактической стоимости, в дебет соответствующих субсчетов вносятся все расходы на их приобретение.
При поступлении материалов составляются такие проводки: Д-т сч. 10 «Материалы», соответствующий субсчет К-т сч. 60 «Расчеты с поставщиками и подрядчиками» — на стоимость поступивших материалов по ценам поставщиков со всеми наценками сбытовых и снабженческих организаций и транспортно-заготовительными расходами, включенными в счета поставщиков. Также сюда включается оплата процентов при приобретении в кредит, который представлен поставщиком или банком на эти цели, стоимость услуг по доставке материалов водным и ж/д транспортом, сумму комиссионного вознаграждения посреднику.
Приобретение материалов отражается в учете на счете 10 «Материалы». Наряду с этим процесс приобретения можно отразить используя счета 15 «Заготовление и приобретение материальных ценностей» и 16 «Отклонения в стоимости материальных ценностей».
В таком случае счет 15 «Заготовление и приобретение материальных ценностей» используется в качестве накопительного. На нем в течение всего процесса приобретения МПЗ накапливаются расходы, которые связаны с формированием цены приобретения. По дебету этого счета отражается: сумма страховых платежей, стоимость материалов и их доставки, сумма таможенных платежей, если они предусмотрены условиями доставки, сумма процентов по банковским кредитам, если они начисляются до принятия МПЗ к учету, и т. д. в соответствии с п. 6 ПБУ 5/01 «Учет материально-производственных запасов». Процесс завершается поступлением МПЗ на склад:
Д-т сч. 10 «Материалы»
К-т сч. 15 «Заготовление и приобретение материальных ценностей».
Необходимо обратить внимание на то, что при налогообложении прибыли сумма процентов за пользование банковским кредитом, вне зависимости от момента их начисления, будет включаться в состав внереализационных расходов. Это говорит о том, что бухгалтер организации должен будет составить регистр-расчет по налоговому учету формирования учетной цены материалов, не включая в нее сумму процентов за кредит и регистр-расчет по налоговому учету внереализационных расходов. Подобная корректировка учетных данных зачастую приводит к росту внереализационных расходов организации в отчетном периоде и, исходя из этого, уменьшению налоговой базы по налогу на прибыль на этот период. Однако с другой стороны уменьшенная учетная цена на материально-производственные запасы позволить снизить расходы на производство продукции и увеличить налоговую базу по этому налогу в тех отчетных периодах, когда организация будет включать в производственные затраты стоимость приобретенных с использованием банковского кредита материалов.
Помимо этого, использование счета 15 «Заготовление и приобретение материальных ценностей» возможно тогда, когда организация применяет плановые (нормативные) цены, в качестве учетных цен МПЗ. Это цены, по которым материалы включаются и в плановую (нормативную) калькуляцию себестоимости продукции (работ, услуг). Отражение операций приобретения материалов в учете в таком случае будет следующим:
- Д-т сч. 10 «Материалы» К-т сч. 15 «Заготовление и приобретение материальных ценностей» — на сумму учетной стоимости материалов;
- Д-т сч. 15 «Заготовление и приобретение материальных ценностей» К-т сч. 60 «Расчеты с поставщиками и подрядчиками» — на сумму фактической цены приобретения;
- Д-т сч. 15 «Заготовление и приобретение материальных ценностей» К-т сч. 16 «Отклонение в стоимости материальных ценностей» — на сумму превышения нормативной стоимости МПЗ над фактической;
- Д-т сч. 16 «Отклонение в стоимости материальных ценностей» К-т сч. 15 «Заготовление и приобретение материальных ценностей» — на сумму превышения фактической цены приобретения над нормативной.
НДС, который уплачивается при приобретении материалов, отражается в учете вне зависимости от того, какой счет используется для формирования их учетной цены.
При приемке материалов, которые были оплачены авансом, могут быть обнаружены излишки или недостачи поступивших материалов по сравнению с данными, которые указаны в сопроводительных документах. Это оформляется соответствующим актом. В этом случае к учету принимаются только фактически полученные ценности, а те те, которые указаны в документах поставщика.
Если при приемке материалов, которые были оплачены авансом, выявлена недостача или порча, которые возникли по вине поставщика, то на их стоимость направляется претензия поставщику. Это отражается в учете таким образом:
Д-т сч. 76 «Расчеты с разными дебиторами и кредиторами», субсчет «Расчеты по претензиям»
К-т сч. 60 «Расчеты с поставщиками и подрядчиками».
В сумму претензии входит также налог на добавленную стоимость, который приходится на недостающие ценности. Если по условиям договора к поставщику применяются штрафы за недопоставку ценностей или другие недочеты, то они также включаются в сумму претензии:
Д-т сч. 76 «Расчеты с разными дебиторами и кредиторами», субсчет «Расчеты по претензиям»
К-т сч. 91 «Прочие доходы и расходы», субсчет «Прочие доходы».
На сумму излишков, выявленных при оприходовании, выписывают платежное поручение и доплачивают поставщику либо относят на увеличение прочих доходов организации:
Д-т сч. 10 «Материалы»
К-т сч. 91 «Прочие доходы и расходы», субсчет «Прочие доходы».
В организациях полиграфии к материально-производственным запасам, которые отражают специфику их деятельности, относят картон, переплетные материалы, бумагу, клей, краску и т. п. При получении, например, бумаги для выполнения полиграфических работ, ее отражают на забалансовом счете 003 «Материалы, принятые в переработку», поскольку право собственности на нее не переходит к полиграфической организации. Получение бумаги отражается по дебету счета 003. После того, как работы завершены и бумага, полученная ранее, использована, счет 003 кредитуют.
При безвозмездном получении материально-производственных запасов по договору дарения бухгалтером составляется следующая проводка: Д-т сч. 10 «Материалы», соответствующий субсчет К-т сч. 98 «Доходы будущих периодов», субсчет «Безвозмездно полученные ценности» — на стоимость ценностей, которая указана в договоре, а также в сопроводительном документе.
По мере поступления материалов, которые были получены безвозмездно, в производство либо на иные нужды будут составляться такие проводки:
Д-т сч. 20 «Основное производство» — материалы отпущены основному производству;
Д-т сч. 23 «Вспомогательные производства» — материалы отпущены вспомогательным производствам;
Д-т сч. 25 «Общепроизводственные расходы» — материалы отпущены на общепроизводственные нужды;
Д-т сч. 26 «Общехозяйственные расходы» — материалы отпущены на общехозяйственные нужды;
Д-т сч. 44 «Расходы на продажу» — материалы отпущены отделу сбыта для организации продажи продукции;
К-т сч. 10 «Материалы», соответствующий субсчет.
В бухучете будет признаваться доход текущего периода в той же сумме, на которую были отпущены материально-производственные запасы:
Д-т сч. 98 «Доходы будущих периодов», субсчет «Безвозмездно полученные ценности»
К-т сч. 91 «Прочие доходы и расходы», субсчет «Прочие доходы».
Литература:
- О бухгалтерском учете: Федеральный закон от 06.12.2011 № 402-ФЗ.
- Об утверждении Положения по бухгалтерскому учету «Учет материально-производственных запасов» ПБУ 5/01: приказ Минфина России от 09.06.2001 № 44н.
Основные термины (генерируются автоматически): бухгалтерский учет, материал, ценность, запас, расход, Заготовление, поставщик, приобретение, соответствующий субсчет, сумма процентов.
Организация материально-производственных запасов в 1С Бухгалтерия
Оглавление
1. Поступление МПЗ
2. Списание МПЗ
Материально-производственные запасы – это материалы, которые используются в производстве товаров, работах, при предоставлении услуг, а также для хозяйственных нужд в организации. Бухгалтерский учет материально-производственных запасов ведется в 1С:Бухгалтерия 3.0 на счете 10 посредством документов поступления и списания.
1. Поступление МПЗ
Для того, чтобы ввести в 1С 8 документ поступления МПЗ, зайдите в раздел «Покупки» и выберите «Поступление (акты, накладные)».
Далее нажмите «Поступление» и выберите «Товары (накладная)».
Заполните информацию из документа от поставщика:
·Номер, дата – номер и дата накладной или УПД от поставщика;
·Контрагент – поставщик;
·Договор – выберите договор, по которому производится поставка;
·Счет на оплату – если в программу введен счет от поставщика, то выберите его. Также документ поступления можно ввести непосредственно на основании документа «Счет».
·Организация, подразделение – выберите нужные.
·Расчеты – укажите счета расчетов с контрагентом и правила зачета аванса.
·Грузоотправитель и грузополучатель – нужно изменить, если эти реквизиты отличаются от организации и контрагента.
·НДС – заполните правила учета НДС.
После этого переходите к заполнению табличной части документа. Заполнить ее можно разными способами:
· с помощью кнопки «Добавить» – в этом случае в документ 1С 8 добавляется строчка, в которой активируем функцию «Показать все» и выбираем из справочника нужную номенклатуру (если нужной в справочнике нет, добавляем новую). При необходимости вводим в строке количество, цену, ставку НДС.
· с помощью кнопки «Подбор», открыв окно подбора материалов из справочника, в котором можно подобрать нужные товары через поиск. Вводим количество и цену, после чего жмем «Перенести в документ».
Нажмите Провести и закрыть. Документ создан!
2. Списание МПЗ
Списание МПЗ в производство или в затраты оформляется документом «Требование-накладная». Оформить этот документ можно двумя способами:
1. Откройте «Склад – Требования-накладные», и нажмите «Создать».
2. На основании документа «Поступление товаров»:
В созданном документе важно заполнить поле «Цель расхода».
Далее заполним табличную часть вкладки «Материалы» по кнопкам «Добавить» или «Подбор».
На вкладке «Счет затрат» указываем нужный счет для отнесения затрат, подразделение затрат и статью затрат.
По кнопке «Провести и закрыть» создаем требование-накладную в 1С. Организация материально-производственных запасов проведена успешно.
Консультант компании ООО «Кодерлайн»
Ульяна Куприна
Выбор способа оценки запасов при выбытии
Методы оценки, разрешенные в налоговом учетеВ целях исчисления налога на прибыль организаций для определения материальных расходов при списании сырья, материалов, используемых в производстве продукции, выполнении работ и оказании услуг согласно п. 8 ст. 254 Налогового кодекса РФ могут применяться следующие методы оценки: по стоимости единицы запасов; по средней стоимости; по стоимости первых по времени приобретений (метод ФИФО). Такие же методы оценки применяются и при списании покупных товаров при их реализации (подп. 3 п. 1 ст. 268 НК РФ).
Однако порядок расчета при том или ином методе в НК РФ не раскрывается, а способ расчета (взвешенный или скользящий) вообще не упомянут.
Налогоплательщик вправе уменьшить доходы от таких операций на сумму расходов, непосредственно связанных с такой реализацией, в частности на расходы по оценке, хранению, обслуживанию и транспортировке реализуемого имущества. При реализации покупных товаров расходы, связанные с их покупкой и реализацией, формируются с учетом положений ст. 320 НК РФ. Напомним, что ст. 320 НК РФ определяет, что налогоплательщик имеет право сформировать стоимость приобретения товаров с учетом расходов, связанных с приобретением этих товаров в соответствии с подп. 3 п. 1 ст. 268 НК РФ. Стоимость приобретения товаров, отгруженных, но не реализованных на конец месяца, не включается налогоплательщиком в состав расходов, связанных с производством и реализацией, до момента их реализации. Порядок формирования стоимости приобретения товаров определяется налогоплательщиком в учетной политике для целей налогообложения и применяется в течение не менее двух налоговых периодов.
Статьей 313 НК РФ установлено, что система налогового учета организуется налогоплательщиком самостоятельно исходя из принципа последовательности применения норм и правил налогового учета, т. е. применяется последовательно от одного налогового периода к другому. Порядок ведения налогового учета устанавливается налогоплательщиком в учетной политике для целей налогообложения, утверждаемой соответствующим приказом (распоряжением) руководителя.
Отметим, что некоторые понятийные различия в НК РФ и нормативных документах по бухгалтерскому учету никак не мешают использовать «бухгалтерскую» методику. Судите сами. Понятие «метод оценки» из ст. 254 НК РФ идентично понятию «способ оценки» из ПБУ 5/01. Соответственно, понятие «стоимость единицы запасов» идентично понятию «себестоимость единицы запаса». Получается, что «налоговые» методы идентичны тем, что используются в бухгалтерском учете. Следовательно, на основании ст. 11 и 54 НК РФ организация может обратиться к порядку, предусмотренному законодательством о бухгалтерском учете, где подробно расписано, как применять указанные методы. Такой же вывод сделал Минфин России в отношении порядка применения метода оценки покупных товаров при их реализации по средней себестоимости (письмо от 11 августа 2015 г. № 03−03−06/2/46 207).
Отметим, что в подп. 3 п. 1 ст. 268 НК РФ не уточняется, вправе ли организации применять разные методы оценки покупных товаров при их реализации. По мнению Минфина России, это возможно в отношении различных групп товаров в зависимости от их характеристик. Такой порядок оценки должен быть предусмотрен учетной политикой организации (письмо от 26 октября 2015 г. № 03−03−06/1/61 288).
Итак, Налоговый кодекс РФ позволяет организации самостоятельно выбрать способ учета расходов на приобретение товаров и запасов.
На наш взгляд, необходимо обратить внимание на постановление А С Поволжского округа от 20 января 2017 г. № Ф06−16 408/2016 по делу № А55−3680/2016. Суть дела: налоговый орган произвел расчет базы по налогу на прибыль на основании регистров бухгалтерского учета налогоплательщика и первичных учетных документов, полученных от налогоплательщика и его контрагентов, ввиду того что в проверяемом периоде налогоплательщик регистры налогового учета не вел. Поскольку порядок формирования стоимости приобретения товаров в учетной политике налогоплательщика определен не был, налоговый орган, проанализировав перечисленные в подп. 3 п. 1 ст. 268 НК РФ методы оценки покупных товаров, счел наиболее подходящим для данной организации и ее вида деятельности метод оценки по средней стоимости: по мнению налогового органа, этот метод позволяет сохранять величину прибыли на среднем уровне и тем самым избежать как непредсказуемо высоких ее значений, возникающих при резком падении цен, так и неожиданных убытков, являющихся следствием возрастания их стоимости.
Суд пришел к выводу о необоснованном применении налоговым органом данного метода, указав, что в силу ст. 268 НК РФ право выбора того или иного метода принадлежит налогоплательщику, и налоговый орган не вправе оценивать целесообразность этого выбора и применять метод по своему усмотрению. Несмотря на то что в учетной политике налогоплательщика отсутствует метод оценки покупных товаров, это не свидетельствует о неуплате им налога на прибыль, из первичных документов налогоплательщика, в том числе счетов-фактур, товарных накладных, следует, что им применялся метод оценки покупных товаров по стоимости единицы товара, а налог на прибыль был доначислен налоговым органом необоснованно.
Ген MPZ: MedlinePlus Genetics
Болезнь Шарко-Мари-Тута
Исследователи идентифицировали более 120 мутаций гена MPZ , которые вызывают форму болезни Шарко-Мари-Тута, известную как тип 1B. Синдром Шарко-Мари-Тута — это заболевание, характеризующееся мышечной слабостью и сенсорными проблемами, особенно в руках и ногах. Многие из мутаций гена MPZ , которые вызывают синдром Шарко-Мари-Тута, изменяют отдельные белковые строительные блоки (аминокислоты) в нулевом миелиновом белке.Другие мутации приводят к белку, в котором отсутствует одна или несколько аминокислот. Измененный нулевой белок миелина, вероятно, не может должным образом взаимодействовать с другими компонентами миелина, что может нарушить уплотнение миелина. В результате периферические нервы не могут запускать движение мышц или передавать информацию от сенсорных клеток обратно в мозг, что приводит к слабости и сенсорным проблемам, характерным для болезни Шарко-Мари-Тута.
Некоторые мутации гена MPZ вызывают тяжелую форму болезни Шарко-Мари-Тута типа 1B.Симптомы проявляются в младенчестве или раннем детстве и включают задержку развития двигательных навыков, таких как ходьба. Эту форму болезни Шарко-Мари-Тута иногда называют синдромом Дежерина-Сотта, врожденной гипомиелинизацией или синдромом Русси-Леви. Исследователи полагают, что мутации гена MPZ , вызывающие тяжелую форму заболевания, вероятно, нарушают образование миелина на раннем этапе развития.
Несколько мутаций в гене MPZ вызывают другие формы болезни Шарко-Мари-Тута, известные как тип 2I, тип 2J и доминантное промежуточное звено D.Эти формы болезни Шарко-Мари-Тута, которые часто не проявляются до зрелого возраста, влияют на специализированные отростки нервных клеток (аксонов), которые передают импульсы мышцам и другим нервным клеткам. Люди с болезнью Шарко-Мари-Тута 2J типа также могут иметь потерю слуха и аномалии открытия глаза, через которое проходит свет (зрачок). Неясно, как мутации гена MPZ вызывают эти нарушения.
Подробнее об этом состоянии здоровьяOMIM запись — * 159440
Ауэр-Грумбах, М., Штрассер-Фукс, С., Робл, Т., Виндпассинджер, К., Вагнер, К. Синдром Шарко-Мари-Тута 2 с поздним началом, вызванный двумя новыми мутациями в гене MPZ. Neurology 61: 1435-1437, 2003. Примечание: Erratum: Neurology 62: 678 only, 2004. [PubMed: 14638973] [Полный текст: http: // www.Neurology.org/cgi/pmidlookup?view=long&pmid=14638973]
Бало, Р. Х., Джен, Дж. К., Ким, Г., Бало, Р. В. Хронический кашель из-за мутации thr124met в нулевом периферическом миелиновом белке (ген MPZ). Неврология 62: 1905-1906, 2004. [PubMed: 15159512] [Полный текст: http://www.neurology.org/cgi/pmidlookup?view=long&pmid=15159512]
Бланке-Гроссар, Ф., Pham-Dinh, D., Dautigny, A., Latour, P., Bonnebouche, C., Corbillon, E., Chazot, G., Vandenberghe, A. Невропатия Шарко-Мари-Тута типа 1B: третья мутация кодона серина 63 в гене главного периферического гликопротеина миелина P0. Clin. Genet. 48: 281-283, 1995. [PubMed: 8835320] [Полный текст: https: // onlinelibrary.wiley.com/resolve/openurl?genre=article&sid=nlm:pubmed&issn=0009-9163&date=1995&volume=48&issue=6&spage=281]
Буркоэль, К.Ф., Такашима, Х., Гарсия, Калифорния, Олни, Р.К., Джонсон, Дж., Берри, К., Руссо, П., Кеннеди, С., Тиби, А.С., Скавина, М., Уильямс, Л.Л., Мансиас , П., Батлер, И.Дж., Краевски, К., Шай, М., Лупски, мл. Болезнь Шарко-Мари-Тута и родственные нейропатии: распределение мутаций и корреляция генотип-фенотип. Анна. Neurol. 51: 190-201, 2002. [PubMed: 11835375] [Полный текст: https: // onlinelibrary.wiley.com/resolve/openurl?genre=article&sid=nlm:pubmed&issn=0364-5134&date=2002&volume=51&issue=2&spage=190]
Картер, М.С., Ли, С., Уилкинсон, М. Ф. Зависимый от сплайсинга регуляторный механизм, который обнаруживает сигналы трансляции. EMBO J. 15: 5965-5975, 1996. [PubMed: 84] [Полный текст: https: // onlinelibrary.wiley.com/resolve/openurl?genre=article&sid=nlm:pubmed&issn=0261-4189&date=1996&volume=15&issue=21&spage=5965]
Чапон, Ф., Латур, П., Дирасон, П., Шеффер, С., Ванденберге, А. Аксональный фенотип болезни Шарко-Мари-Тута, связанный с мутацией в гене нулевого белка миелина. J. Neurol. Нейрохирургия. Психиатр. 66: 779-782, 1999. [PubMed: 10329755] [Полный текст: https: // jnnp.bmj.com/lookup/pmidlookup?view=long&pmid=10329755]
Crehalet, H., Latour, P., Bonnet, V., Attarian, S., Labauge, P., Бонелло, Н., Бернар, Р., Миллат, Г., Руссон, Р., Бозон, Д. Неправильное связывание мяРНК U1: новая причина CMT1B. Нейрогенетика 11: 13-19, 2010. [PubMed: 19475438] [Полный текст: https: // dx.doi.org/10.1007/s10048-009-0199-8]
Де Йонге, П., Тиммерман, В., Сеутерик, К., Нелис, Э., Де Вриндт, Э., Лофгрен, А., Vercruyssen, A., Verellen, C., Van Maldergem, L., Martin, J.-J., Van Broeckhoven, C. Мутация thr124-to-met в гене нулевого периферического миелинового белка (MPZ) связана с клинически отличным фенотипом Шарко-Мари-Тута. Мозг 122: 281-290, 1999. [PubMed: 10071056] [Полный текст: https: // Acade.oup.com/brain/article-lookup/doi/10.1093/brain/122.2.281]
Фабрици, Г. М., Феррарини, М., Кавалларо, Т., Жарре, Л., Поло, А., Риццуто, Н. Соматическая и мозаичная мутация зародышевой линии в MPZ / P0 имитирует рецессивное наследование CMT1B. Неврология 57: 101-105, 2001. [PubMed: 11445635] [Полный текст: http: // www.neuroology.org/cgi/pmidlookup?view=long&pmid=11445635]
Фабрици, Г. М., Пеллегрини, М., Ангиари, К., Кавалларо, Т., Морини, А., Тайоли, Ф., Кабрини, И., Оррико, Д., Риццуто, Н. Дозовая чувствительность гена новой мутации во внутриклеточном домене P0, связанной с болезнью Шарко-Мари-Тута типа 1B. Neuromusc. Disord. 16: 183-187, 2006. [PubMed: 16488608] [Полный текст: https: // linkinghub.elsevier.com/retrieve/pii/S0960-8966(06)00024-1]
Фабрици, Г. М., Тайоли, Ф., Кавалларо, Т., Ригателли, Ф., Симонати, А., Мариани, Г., Перроне, П., Риццуто, Н. Фокально свернутый миелин при нейропатии Шарко-Мари-Тута типа 1B с ser49leu в нулевом миелиновом белке. Acta Neuropath. 100: 299-304, 2000. [PubMed: 10965800] [Полный текст: https: // dx.doi.org/10.1007/s0040195]
Харати, Ю., Батлер, И. Дж. Врожденная гипомиелинизирующая нейропатия. J. Neurol. Нейрохирургия. Психиатр. 48: 1269-1276, 1985. [PubMed: 4087003] [Полный текст: https://jnnp.bmj.com/lookup/pmidlookup?view=long&pmid=4087003]
Хаясака, К., Химоро, М., Сато, В., Такада, Г., Уэмура, К., Симидзу, Н., Берд, Т. Д., Коннелли, П. М., Шанс, П. Ф. Невропатия Шарко-Мари-Тута типа 1B связана с мутациями гена миелина P (0). Nature Genet. 5: 31-34, 1993. [PubMed: 76
] [Полный текст: https: // doi.org / 10.1038 / ng0993-31]Хаясака, К., Химоро, М., Савайши, Ю., Нанао, К., Такахаши, Т., Такада, Г., Николсон, Г.А., Оврие, Р.А., Тачи, Н. De novo мутация гена миелина P (0) при болезни Дежерина-Соттаса (наследственная моторная и сенсорная нейропатия III типа). Nature Genet. 5: 266-268, 1993. [PubMed: 7506095] [Полный текст: https: // doi.org / 10.1038 / ng1193-266]
Хаясака, К., Химуро, М., Ван, Ю., Таката, М., Миносима, С., Симидзу, Н., Миура, М., Уэмура, К., Такада, Г. Структура и хромосомная локализация гена, кодирующего нулевой белок миелина человека (MPZ). Геномика 17: 755-758, 1993. [PubMed: 7503936] [Полный текст: https: // linkinghub.elsevier.com/retrieve/pii/S0888-7543(83)71400-X]
Хаясака, К., Нанао, К., Тахара, М., Сато, В., Такада, Г., Миура, М., Уэмура, К. Выделение и определение последовательности кДНК, кодирующей основной структурный белок периферического миелина человека. Биохим. Биофиз. Res. Commun. 180: 515-518, 1991. [PubMed: 1719967] [Полный текст: https: // linkinghub.elsevier.com/retrieve/pii/S0006-291X(05)81094-0]
Хаясака К., Охниши А., Такада Г., Фукусима Ю., Мураи Ю. Мутация гена myeline (sic) P0 при нейропатии Шарко-Мари-Тута 1 типа. Биохим. Биофиз. Res. Commun. 194: 1317-1322, 1993. [PubMed: 7688964] [Полный текст: https://linkinghub.elsevier.com/retrieve/pii/S0006291X83719686]
Икегами, Т., Николсон, Г., Икеда, Х., Исида, А., Джонстон, Х., Уайз, Г., Оврие, Р., Хаясака, К. Новая гомозиготная мутация гена миелина P (0), вызывающая болезнь Дежерина-Соттаса (наследственная моторная и сенсорная нейропатия III типа). Биохим. Биофиз. Res. Commun. 222: 107-110, 1996. [PubMed: 8630052] [Полный текст: https: // linkinghub.elsevier.com/retrieve/pii/S0006-291X(96)
Иноуэ, К., Хаджави, М., Охьяма, Т., Хирабаяши, С., Уилсон, Дж., Реджин, Дж.Д., Мансиас, П., Батлер, И. Дж., Уилкинсон, М. Ф., Вегнер, М., Лупски, Дж. Р. Молекулярный механизм различных неврологических фенотипов, передаваемых усекающими аллелями мутациями. Nature Genet. 36: 361-369, 2004. [PubMed: 15004559] [Полный текст: https: // doi.org / 10.1038 / ng1322]
Кабзинская Д., Корвин-Пиотровска Т., Дрешлер Х., Драк Х., Хаусманова-Петрусевич И., Кочанский А. Позднее начало болезни Шарко-Мари-Тута 2 типа с нарушением слуха, связанное с новой мутацией Pro105Thr в гене MPZ. (Письмо) Являюсь. J. Med. Genet. 143A: 2196-2199, 2007. [PubMed: 17663472] [Полный текст: https: // doi.org / 10.1002 / ajmg.a.31908]
Каку, Д. А., Парри, Г. Дж., Маламут, Р., Лупски, Дж. Р., Гарсия, К. А. Исследования нервной проводимости при полинейропатии Шарко-Мари-Тута, связанной с сегментарной дупликацией 17 хромосомы. Неврология 43: 1806-1808, 1993. [PubMed: 8414036] [Полный текст: https://dx.doi.org/10.1212/wnl.43.9.1806]
Камхольц, Дж., Шай, М.Э. Синдром Шарко-Мари-Тута 2 с поздним началом, вызванный двумя новыми мутациями в гене MPZ. Неврология 63: только 194, 2004. [PubMed: 15249646] [Полный текст: http: // www.Neurology.org/cgi/pmidlookup?view=long&pmid=15249646]
Хаджави, М., Иноуэ, К., Вишневски, В., Охьяма, Т., Снайпс, Г.Дж., Лупски, Дж. Р. Куркумин устраняет задержку эндоплазматического ретикулума и индуцированный агрегацией апоптоз, связанный с вызывающими нейропатию мутантами миелинового белка с нулевым усечением. Являюсь. J. Hum. Genet. 77: 841-850, 2005. [PubMed: 16252242] [Полный текст: https: // linkinghub.elsevier.com/retrieve/pii/S0002-9297(07)63364-3]
Киллиан, Дж. М., Клопфер, Х. У. Гомозиготная экспрессия доминантного гена невропатии Шарко-Мари-Тута. Анна. Neurol. 5: 515-522, 1979. [PubMed: 475348] [Полный текст: https://onlinelibrary.wiley.com/resolve/openurl?genre=article&sid=nlm:pubmed&issn=0364-5134&date=1979&volume=5&issue=6&spage=515]
Кочанский, А., Драк, Х., Кабзинская, Д., Рыневич, Б., Ровинска-Марцинска, К., Новаковски, А., Хаусманова-Петрусевич, И. Новая мутация гена MPZ при врожденной нейропатии с гипомиелинизацией. Неврология 62: 2122-2123, 2004. [PubMed: 15184631] [Полный текст: http: // www.Neurology.org/cgi/pmidlookup?view=long&pmid=15184631]
Кулькенс, Т., Болхуис, П. А., Вольтерман, Р. А., Кемп, С., те Нийенхейс, С., Valentijn, L.J., Hensels, G.W., Jennekens, F.G.I., de Visser, M., Hoogendijk, J.E., Baas, F. Делеция кодона серина 34 из гена основного периферического миелинового белка P (0) при болезни Шарко-Мари-Тута типа 1B. Nature Genet. 5: 35-39, 1993. [PubMed: 76
] [Полный текст: https: // doi.org / 10.1038 / ng0993-35]
Лил, А., Бергхофф, К., Бергхофф, М., Дель Валле, Г., Контрерас, К., Монтойя, О., Эрнандес, Э., Barrantes, R., Schlotzer-Schrehardt, U., Neundorfer, B., Reis, A., Rautenstrauss, B., Heuss, D. Болезнь Шарко-Мари-Тута: новая мутация tyr145ser в гене нулевого миелинового белка (MPZ, PO) вызывает разные фенотипы у гомозиготных и гетерозиготных носителей в пределах одной семьи. Нейрогенетика 4: 191-197, 2003. [PubMed: 12845552] [Полный текст: https: // dx.doi.org/10.1007/s10048-003-0153-0]
Ли, Ю. К., Ю, К. Т. Р., Лин, К. П., Чанг, М. Х., Сюй, С. Л., Лю, Ю. Ф., Лу, Ю.К., Сунг, Б. В. Мутация MPZ G123S характеристика: свидетельство сложного патогенеза CMT-болезни. Неврология 70: 273-277, 2008. [PubMed: 18209201] [Полный текст: http: // www.Neurology.org/cgi/pmidlookup?view=long&pmid=18209201]
Лемке Г., Аксель Р. Выделение и последовательность кДНК, кодирующей основной структурный белок периферического миелина. Cell 40: 501-508, 1985. [PubMed: 2578885] [Полный текст: https://linkinghub.elsevier.com/retrieve/pii/0092-8674(85)
Лемке, Г. Молекулярная биология основных генов миелина. Trends Neurosci. 9: 266-270, 1986.
Лупски, Я.Р., Монтес де Ока-Луна, Р., Слаугенгаупт, С., Пентао, Л., Гузетта, В., Траск, Б.Дж., Соседо-Карденас, О., Баркер, Д.Ф., Киллиан, Д.М., Гарсия, Калифорния, Чакраварти, А., Патель, П.И. Дупликация ДНК, связанная с болезнью Шарко-Мари-Тута типа 1А. Cell 66: 219-232, 1991. [PubMed: 1677316] [Полный текст: https: // linkinghub.elsevier.com/retrieve/pii/0092-8674(91)-4]
Маэда, М. Х., Мицуи, Дж., Сунг, Б.-В., Такахаши, Ю., Ишиура, Х., Хаяси, С., Shirota, Y., Ichikawa, Y., Matsumoto, H., Arai, M., Okamoto, T., Miyama, S., Shimizu, J., Inazawa, J., Goto, J., Tsuji, S. Повышенная доза гена нулевого миелинового белка вызывает болезнь Шарко-Мари-Тута. Анна. Neurol. 71: 84-92, 2012. [PubMed: 22275255] [Полный текст: https: // doi.org / 10.1002 / ana.22658]
Мандич, П., Фосса, П., Каппони, С., Герольди, А., Аквавива, М., Гулли, Р., Чиотти, П., Манганелли, Ф., Грандис, М., Беллоне, Э. Клинические особенности и молекулярное моделирование новых мутаций MPZ при демиелинизирующих и аксональных невропатиях. Europ. J. Hum. Genet. 17: 1129-1134, 2009. [PubMed: 142] [Полный текст: https: // dx.doi.org/10.1038/ejhg.2009.37]
Мандич, П., Манкарди, Г. Л., Варез, А., Сориани, С., Ди Мария, Э., Беллоне, Э., Бадо, М., Гросс, Л., Виндебанк, А. Дж., Аджмар, Ф., Шеноне, А. Врожденная гипомиелинизация, вызванная мутацией нулевого белка миелина Q215X. Анна. Neurol. 45: 676-678, 1999. [PubMed: 10319895] [Полный текст: https: // onlinelibrary.wiley.com/resolve/openurl?genre=article&sid=nlm:pubmed&issn=0364-5134&date=1999&volume=45&issue=5&spage=676]
Марросу, М.Г., Ваккарджиу, С., Марросу, Г., Ваннелли, А., Чианкетти, К., Мунтони, Ф. Болезнь Шарко-Мари-Тута 2 типа, связанная с мутацией нулевого гена миелинового белка. Неврология 50: 1397-1401, 1998. [PubMed: 9595994] [Полный текст: https: // dx.doi.org/10.1212/wnl.50.5.1397]
Мартини, Р., Зеласек, Дж., Тойка, К. В., Гизе, К. П., Шахнер, М. У мышей с дефицитом нулевого белка (P0) наблюдается дегенерация миелина в периферических нервах, характерная для наследственных человеческих невропатий. Nature Genet. 11: 281-286, 1995. [PubMed: 7581451] [Полный текст: https://doi.org/10.1038/ng1195-281]
Масталья, Ф.Л., Новак, К. Дж., Стелл, Р., Филлипс, Б. А., Эдмонстон, Дж. Э., Дорош, С. М., Уилтон, С. Д., Холлмайер, Дж., Какулас, Б. А., Лэйнг, Н. Г. Новая мутация в гене нулевого белка миелина в семье с промежуточной наследственной моторной и сенсорной невропатией. J. Neurol. Нейрохирургия. Психиатр. 67: 174-179, 1999. [PubMed: 10406984] [Полный текст: https: // jnnp.bmj.com/lookup/pmidlookup?view=long&pmid=10406984]
Мису, К., Йошихара, Т., Шикама, Ю., Аваки, Э., Ямамото, М., Хаттори, Н., Хираяма, М., Такегами, Т., Накашима, К., Собуэ, Г. Аксональная форма болезни Шарко-Мари-Тута, демонстрирующая отличительные особенности в связи с мутациями в гене нулевого периферического миелинового белка (thr124met или asp75val). J. Neurol. Нейрохирургия. Психиатр. 69: 806-811, 2000. [PubMed: 11080237] [Полный текст: https: // jnnp.bmj.com/lookup/pmidlookup?view=long&pmid=11080237]
Надь, Э., Макват, Л. Э. Правило для положения терминирующего кодона в интрон-содержащих генах: когда бессмыслица влияет на количество РНК. Тенденции Биохим. Sci. 23: 198-199, 1998. [PubMed: 9644970] [Полный текст: https://linkinghub.elsevier.com/retrieve/pii/S0968-0004(98)01208-0]
Накагава, М., Суэхара, М., Сайто, А., Такашима, Х., Умехара, Ф., Сайто, М., Канзато, Н., Мацудзаки, Т., Такенага, С., Сакода, С., Идзумо, С. , Осаме, М. Новая мутация гена MPZ при доминантно наследуемой нейропатии с фокально свернутыми миелиновыми оболочками. Неврология 52: 1271-1275, 1999. [PubMed: 10214757] [Полный текст: http: // www.neuroology.org/cgi/pmidlookup?view=long&pmid=10214757]
Нелис, Э., Хайтес, Н., Ван Брокховен, К. Мутации в генах периферического миелина и связанных генах при наследственных периферических невропатиях. Гм. Мутат. 13: 11-28, 1999. [PubMed: 9888385] [Полный текст: https://doi.org/10.1002/(SICI)1098-1004(1999)13:1<11::AID-HUMU2>3.0.CO; 2-A]
Оки, Р. Дж., Уотсон, М. Л., Селдин, М. Ф. Построение физической карты на хромосоме 1 мыши и человека: сравнение 13 МБ ДНК мыши и 11 МБ ДНК человека. Гм. Molec. Genet. 1: 613-620, 1992. [PubMed: 1301170] [Полный текст: https://academic.oup.com/hmg/article-lookup/doi/10.1093/hmg/1.8,613]
Оврие, Р. А., Маклеод, Дж. Г., Кончин, Т. Э. Гипертрофические формы наследственной моторной и сенсорной нейропатии: исследование гипертрофической болезни Шарко-Мари-Тута (HMSN тип I) и болезни Дежерина-Сотта (HMSN тип III) в детском возрасте. Мозг 110: 121-148, 1987. [PubMed: 3467805] [Полный текст: https://academic.oup.com/brain/article-lookup/doi/10.1093/brain/110.1.121]
Фам-Динь, Д., Фурбил, Ю., Бланке, Ф., Маттей, М.-Г., Рокель, Н., Латур, П., Шазо, Г., Ванденберге, А., Даутиньи, А. Главный нулевой ген периферического миелинового белка: структура и локализация в кластере генов рецепторов Fc-гамма на хромосоме 1q21.3-q23 человека. Гм. Molec. Genet. 2: 2051-2054, 1993. [PubMed: 7509228] [Полный текст: https: // Acade.oup.com/hmg/article-lookup/doi/10.1093/hmg/2.12.2051]
Plante-Bordeneuve, V., Guiochon-Mantel, A., Lacroix, C., Lapresle, J., Саид, Г. Семья Русси-Леви: от первоначального описания до гена. Анна. Neurol. 46: 770-773, 1999. [PubMed: 10553995] [Полный текст: https: // onlinelibrary.wiley.com/resolve/openurl?genre=article&sid=nlm:pubmed&issn=0364-5134&date=1999&volume=46&issue=5&spage=770]
Роа, Б.Б., Уорнер, Л. Е., Гарсия, К. А., Руссо, Д., Лавлейс, Р., Ченс, П. Ф., Лупски, Дж. Р. Мутации гена нулевого белка миелина (MPZ) при недупликационной болезни Шарко-Мари-Тута 1 типа. Гм. Мутат. 7: 36-45, 1996. [PubMed: 8664899] [Полный текст: https: // doi.org / 10.1002 / (SICI) 1098-1004 (1996) 7: 1 <36 :: AID-HUMU5> 3.0.CO; 2-N]
Rouger, H., LeGuern, E., Gouider, R., Tardieu, S., Birouk, N., Gugenheim, M., Bouche, P., Agid, Y., Brice, A. Высокая частота мутаций в кодоне 98 гена периферического миелинового белка Po у 20 французских пациентов с CMT1. (Письмо) Являюсь. J. Hum. Genet. 58: 638-641, 1996. [PubMed: 8644725]
Русси, Г., Леви, Г. Sept cas d’une maladie familiale specialulaiere. Rev. Neurol. 45: 427-450, 1926.
Сабет, А., Ли, Дж., Гандур, К., Пу, К., Ву, X., Камхольц, Дж., Шай, М. Э., Камби, Ф. Биопсия кожи демонстрирует аномалии сплайсинга MPZ при нейропатии Шарко-Мари-Тута 1B. Неврология 67: 1141-1146, 2006. [PubMed: 17030746] [Полный текст: http: // www.Neurology.org/cgi/pmidlookup?view=long&pmid=17030746]
Скьявон, Ф., Рампаццо, А., Мерлини, Л., Анджелини, К., Мостаччуоло, М.Л. Мутации одной и той же последовательности гена миелина P0, вызывающие два разных фенотипа. Гм. Мутат. Дополнение 1: S217-S219, 1998. [PubMed: 9452091] [Полный текст: https: // doi.org / 10.1002 / humu.1380110170]
Seeman, P., Mazanec, R., Huehne, K., Suslikova, P., Keller, O., Rautenstrauss, B. Потеря слуха как первый признак позднего развития аксональной CMT болезни из-за новой мутации P0. Неврология 63: 733-735, 2004. [PubMed: 15326256] [Полный текст: http://www.neurology.org/cgi/pmidlookup?view=long&pmid=15326256]
Сендерек, Дж., Hermanns, B., Lehmann, U., Bergmann, C., Marx, G., Kabus, C., Timmerman, V., Stoltenburg-Didinger, G., Schroder, J.M. Невропатия Шарко-Мари-Тута типа 2 и точечные мутации PO: две новые аминокислотные замены (Asp61Gly; Tyr119Cys) и возможная «горячая точка» на Thr124Met. Мозговой путь. 10: 235-248, 2000. [PubMed: 10764043] [Полный текст: https: // onlinelibrary.wiley.com/resolve/openurl?genre=article&sid=nlm:pubmed&issn=1015-6305&date=2000&volume=10&issue=2&spage=235]
Скре, Х. Генетические и клинические аспекты болезни Шарко-Мари-Тута. Clin. Genet. 6: 98-118, 1974. [PubMed: 4430158] [Полный текст: https: // onlinelibrary.wiley.com/resolve/openurl?genre=article&sid=nlm:pubmed&issn=0009-9163&date=1974&volume=6&issue=2&spage=98]
Смит, Л.С., Руфхаофт, Д., ван Руиссен, Ф., Баас, Ф., ван Дорн, П. А. Врожденная гипомиелинизирующая нейропатия, долгосрочное катамнестическое исследование в пострадавшей семье. Neuromusc. Disord. 18: 59-62, 2008. [PubMed: 17825553] [Полный текст: https: // linkinghub.elsevier.com/retrieve/pii/S0960-8966(07)00683-9]
Сорур, Э., Макмиллан, Дж., Упадхьяя, М. Новая мутация гена миелина P0 в семействе CMT1B. Гм. Мутат. 9: 74-77, 1997. [PubMed: 89
] [Полный текст: https://doi.org/10.1002/(SICI)1098-1004(1997)9:1<74::AID-HUMU16>3.0.CO; 2-M]
Су, Ю., Брукс, Д. Г., Ли, Л., Леперк, Дж., Трофаттер, Дж. А., Раветч, Дж. В., Лебо, Р. В. Ген нулевого белка миелина мутировал у пациентов типа 1B Шарко-Мари-Тута. Proc. Nat. Акад. Sci. 90: 10856-10860, 1993. [PubMed: 7504284] [Полный текст: http://www.pnas.org/cgi/pmidlookup?view=long&pmid=7504284]
Сатклифф, Дж.ГРАММ. Гены миелина. Тенденции Genet. 3: 73-76, 1987.
Сигети, К., Сайфи, Г. М., Армстронг, Д., Белмонт, Дж. У., Миллер, Г., Лупски, Дж. Р. Нарушение дифференцировки мышечных волокон при врожденной гипомиелинизирующей нейропатии, вызванное новой нулевой мутацией миелинового белка. Анна. Neurol. 54: 398-402, 2003. [PubMed: 12953275] [Полный текст: https: // doi.org / 10.1002 / ana.10681]
Тачи, Н., Исикава, Ю., Минами, Р. Два случая врожденной нейропатии гипомиелинизации. Brain Dev. 6: 560-565, 1984. [PubMed: 6099985] [Полный текст: https://linkinghub.elsevier.com/retrieve/pii/S0387-7604(84)80101-1]
Томас, Ф.П., Лебо, Р. В., Росоклия, Г., Дин, X.-S., Лавлейс, Р. Э., Латов, Н., Хейс, А. П. Томакулезная невропатия в хромосоме 1 Синдром Шарко-Мари-Тута. Acta Neuropath. 87: 91-97, 1994. [PubMed: 7511317] [Полный текст: https: // dx.doi.org/10.1007/BF00386259]
Триггс, У. Дж., Браун, Р. Х., мл., Менкес, Д. Л. Случай 18-2006: женщина 57 лет с онемением и слабостью ступней и ног. Новый англ. J. Med. 354: 2584-2592, 2006. [PubMed: 16775239] [Полный текст: https://www.nejm.org/doi/10.1056/NEJMcpc069009?url_ver=Z39.88-2003 & rfr_id = ori: rid: crossref.org & rfr_dat = cr_pub% 3dpubmed]
Умехара, Ф., Такенага, С., Накагава, М., Такахаши, К., Идзумо, С., Мацумуро, К., Сакота, С., Нисимура, Т., Йошикава, Х., Осаме, М. Доминирующая наследственная моторная и сенсорная нейропатия с избыточным комплексом сворачивания миелина. Acta Neuropath. 86: 602-608, 1993. [PubMed: 8310815] [Полный текст: https: // dx.doi.org/10.1007/BF00294299]
Уорнер, Л. Э., Хильц, М. Дж., Аппель, С. Х., Киллиан, Дж. М., Колодный, Э. Х., Карпати, Г., Карпентер, С., Уоттерс, Г. В., Уиллер, К., Витт, Д., Боделл, А., Нелис, Э., Ван Брокховен, К., Лупски, Дж. Р. Клинические фенотипы различных мутаций MPZ (P0) могут включать тип 1B Шарко-Мари-Тута, Дежерина-Соттаса и врожденную гипомиелинизацию. Нейрон 17: 451-460, 1996. [PubMed: 8816708] [Полный текст: https: // linkinghub.elsevier.com/retrieve/pii/S0896-6273(00)80177-4]
Уорнер, Л. Э., Шохат, М., Шорер, З., Лупски, Дж. Р. Множественные точечные мутации de novo MPZ (P0) в спорадическом случае Дежерина-Соттаса. Гм. Мутат. 10: 21-24, 1997. [PubMed:
56] [Полный текст: https://doi.org/10.1002/(SICI)1098-1004(1997)10:1<21::AID-HUMU3>3.0.CO; 2-P]Ватанабэ, М., Ямамото, Н., Окоши, Н., Нагата, Х., Коно, Ю., Хаяси, А., Тамаока, А., Сёдзи, С. Кортикостероид-зависимая асимметричная нейропатия с нулевой мутацией гена миелинового белка. Неврология 59: 767-769, 2002. [PubMed: 12221176] [Полный текст: http://www.neurology.org/cgi/pmidlookup?view=long&pmid=12221176]
Врабец, Л., Фельтри, М.Л., Куаттрини, А., Империале, Д., Превитали, С., Д’Антонио, М., Мартини, Р., Инь, X., Трапп, Б.Д., Чжоу, Л., Чиу, С. — Ю., Мессинг, А. Сверхэкспрессия гликопротеина P (0) вызывает врожденную гипомиелинизацию периферических нервов. J. Cell Biol. 148: 1021-1033, 2000. [PubMed: 10704451] [Полный текст: https: // rupress.org / jcb / article-lookup / doi / 10.1083 / jcb.148.5.1021]
Ю, К.-Х., Се, К.-Л., Хейс, К., Шталь, Н., Франк, У., Попко, Б. Последовательность ДНК, геномная организация и хромосомная локализация нулевого гена периферического миелинового белка мыши: идентификация полиморфных аллелей. Геномика 9: 751-757, 1991. [PubMed: 1709914] [Полный текст: https: // dx.doi.org/10.1016/0888-7543(91)
-t]| Функциональный ключ | Позиция (я) | Описание Действия | Графическое представление | Длина | ||
|---|---|---|---|---|---|---|
| VAR_004500 | 30 | I → M в CMT1B. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs770546306EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004501 | 32 | V → F в CMT1B; суровый. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_004502 | 34 | T → I в CMT1B. Ручное утверждение, основанное на эксперименте i
| 1 | |||
| Естественный вариант i VAR_015971 | 35 | D → Y в CMT1B и CMTDID. Ручное утверждение на основе эксперимента в i
6EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_054393 | 39 | H → P в CMT1B; немного снижает межклеточную адгезию; не влияет на нацеливание на клеточную мембрану. Ручное утверждение на основе эксперимента i
| 1 | 1 | ||
| 904 в DSS. Ручное утверждение на основе эксперимента в i | 1 | |||||
| Естественный вариант i VAR_004503 | 44 | S → F в CMT2I и CMT1B. Ручное утверждение на основе эксперимента в i
8EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_054394 | 50 | Отсутствует в CMT1B. Ручное утверждение на основе эксперимента i
| 1 | |||
| Естественный вариант i VAR_054395 | 51-57 | Отсутствует в CMT1B; влияет на нацеливание на клеточную мембрану; снижает межклеточную адгезию. Ручное утверждение, основанное на эксперименте i
| 7 | |||
| Естественный вариант i VAR_029971 | 51 | S → F в CMT1B. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1553259790EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004504 | 54 | S → C в CMT1B; суровый. | 1 | |||
| Естественный вариант i VAR_004505 | 54 | S → P в CMT1B. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_054396 | 56 | E → K в CMT2. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_004506 | 58 | V → F в CMT1B; умеренный. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_029972 | 60 | D → H в CMT2I. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1214EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_031885 | 61 | D → G в CMT2I. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs786204119EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_015972 | 62 | I → F в CMT1B. Ручное утверждение, основанное на эксперименте i
| 1 | |||
| Естественный вариант i VAR_029973 | 62 | I → M в CMT2I. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1215EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004508 | 63 | S → C в DSS. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs121 | 5EnsemblClinVar. | 1 | ||
| Естественный вариант i VAR_004509 | 63 | S → F в CMT1B. Ручное утверждение на основе эксперимента в i
| 5EnsemblClinVar. | 1 | ||
| Естественный вариант i VAR_004507 | 63 | Отсутствует в CMT1B. Ручное утверждение, основанное на эксперименте в i
| 1 | |||
| Естественный вариант i VAR_004510 | 64 | Отсутствует в CMT1B и DSS. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_031886 | 65 | T → A в CMT1B. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1553259760EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_029974 | 65 | T → I в CMT1B. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_004511 | 68 | Y → C в CMT1B; тяжелая / легкая. Ручное утверждение на основе эксперимента в i
| 1 | |||
| Естественный вариант i VAR_015973 | 75 | D → V в CMT2J и CMT2I. Ручное утверждение на основе эксперимента в i
7EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004512 | 78 | S → L в CMT1B; суровый. Ручное утверждение на основе эксперимента в i
| ||||
| Естественный вариант i VAR_031887 | 78 | S → W в CMT1B. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1211EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004513 | 81 | H → R в CMT1B и CMT2I; суровый; снижает межклеточную адгезию; не влияет на нацеливание на клеточную мембрану. Ручное утверждение на основе эксперимента в i
4EnsemblClinVar. | 1 | |||
| 1 | ||||||
| Естественный вариант i VAR_004514 | 82 | Y → C в CMT1B и DSS. Ручное утверждение на основе эксперимента в i
| 1 | |||
| Естественный вариант i VAR_015974 | 89 | I → N в CMT2I; пациент несет также Мет-92 и Мет-162. Ручное утверждение на основе эксперимента i
| 1 | |||
| D → E в CMT1B. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs121 | 4EnsemblClinVar. | 1 | ||||
| Естественный вариант i VAR_015975 | 92 | V → M в CMT2I; пациент несет также Asn-89 и Met-162. Ручное утверждение на основе эксперимента i
| 1 | |||
| G → E в CMT1B. Ручное утверждение на основе эксперимента в i
| 1 | |||||
| Естественный вариант i VAR_004517 | 96 | K → E в CMT1B. Ручное утверждение на основе эксперимента в i
| 3EnsemblClinVar. | 1 | ||
| Естественный вариант i VAR_029975 | 97 | E → V в CMT2J. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1216EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004518 | 98 | R → C в CMT1B и DSS; суровый. Ручное утверждение, основанное на эксперименте i
0EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004519 | 98 | R → H в CMT1B. Ручное утверждение на основе эксперимента в i
| 9EnsemblClinVar. | 1 | ||
| Естественный вариант i VAR_004520 | 98 | R.Соответствует варианту dbSNP: rs121 | 9EnsemblClinVar. | 1 | ||
| Естественный вариант i VAR_004521 | 98 | R → S в CMT1B. Ручное утверждение, основанное на эксперименте i
| 1 | |||
| Естественный вариант i VAR_004522 | 99 | I → T в CMT1B. | 1 | |||
| Естественный вариант i VAR_004523 | 101 | W → C в CMT1B. Ручное утверждение, основанное на эксперименте i
| 1 | |||
| Естественный вариант i VAR_015976 | 103 | G → E в CMT1B. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1210EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_031889 | 109 | D → N в CMT1B. Ручное утверждение на основе эксперимента в i
| 1 | |||
| Естественный вариант i VAR_029976 | 110 | G → D в DSS. Ручное утверждение на основе эксперимента i
| 1 | |||
| Естественный вариант i VAR_004524 | 112 | I → T в CMT1B; суровый. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1553259662EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_031890 | 113 | V → F в CMT; несекретный; связанный с Y-81. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs281865126EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_029977 | 113 | V → I в CMT2. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_004525 | 114 | I → T в DSS; ассоциирован с тем же аллелем, что и His-116 и Asn-128 у одного пациента. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs267607241EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004526 | 116 | N → H в DSS; ассоциирован с тем же аллелем, что и Thr-114 и Asn-128 у одного пациента. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs267607242EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004527 | 118 | D → DFY в DSS. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_021609 | 118 | D → N в CMT2I. Ручное утверждение, основанное на эксперименте на i
| 1 | |||
| Естественный вариант i VAR_031891 | 119 | Y → C в CMT2I. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs8738EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004528 | 122 | N → S в CMT1B; потеря сайта гликозилирования. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_015977 | 123 | G → C в DSS и CMT1B. Ручное утверждение на основе эксперимента i
| 1 | |||
| Естественный вариант i VAR_004530 | 124-125 | Отсутствует в DSS. Ручное утверждение на основе эксперимента в i
| 2 | |||
| Естественный вариант i VAR_029978 | 124 | T → K в CHN2. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1215EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004529 | 124 | T → M в CMT1B, CMT2I и CMT2J; У пациентов с CMTJ2 имеется зрачок Ади; немного снижает межклеточную адгезию; не влияет на нацеливание на клеточную мембрану; влияет на гликозилирование. Ручное утверждение на основе эксперимента в i
5EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004531 | 127 | C → Y в DSS. | 1 | |||
| Естественный вариант i VAR_004532 | 128 | D → E в CMT1B. | 1 | |||
| Естественный вариант i VAR_004533 | 128 | D → N в DSS; ассоциирован с тем же аллелем, что и Thr-114 и His-116 у одного пациента. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs267607243EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004534 | 130 | K → R в CMT1B, CMT2I и DSS. Ручное утверждение, основанное на эксперименте i
| 1 | |||
| Естественный вариант i VAR_015978 | 131 | K в RO454 N.1 | ||||
| Естественный вариант i VAR_004535 | 132 | P → L в CMT1B; умеренный. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_004536 | 134 | D → E в CMT1B. Ручное утверждение на основе эксперимента в i
| 1 | |||
| Естественный вариант i VAR_029979 | 134 | D → G в CMT1B. Ручное утверждение на основе эксперимента на i
| 1 | |||
| Естественный вариант i VAR_004537 | 134 | D → N в CMT1B. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs1553259647EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_004538 | 135 | I → L в CMT1B и DSS. Ручное утверждение, основанное на эксперименте i
| 1 | |||
| Естественный вариант i VAR_004539 | 135 | I → T в CM Ручное утверждение на основе эксперимента в i
| 7EnsemblClinVar. | 1 | ||
| Естественный вариант i VAR_015979 | 136 | V → E в DSS. Ручное утверждение на основе эксперимента i
| 1 | |||
| Естественный вариант i VAR_004540 | 137 | G → S в CMT1B. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs121 | 8EnsemblClinVar. | 1 | ||
| Естественный вариант i VAR_029980 | 138 | K → N в CMT1B. Ручное утверждение на основе эксперимента на i
| 1 | |||
| Естественный вариант i VAR_029981 | 139 | T → N в CMT1B. Ручное утверждение на основе эксперимента на i
| 1 | |||
| Естественный вариант i VAR_029982 | 140 | S → T в CMT1B. Утверждение вручную на основе эксперимента в i
| 1 | |||
| Естественный вариант i VAR_004541 | 143 | T → M в CMT1B.Соответствует варианту dbSNP: rs750724650EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_029983 | 145 | Y → S в CMT1B. Ручное утверждение, основанное на эксперименте i
| 1 | |||
| Естественный вариант i VAR_029984 | 146 | V → F в CMT1B. Ручное утверждение, основанное на эксперименте i
| 1 | |||
| Естественный вариант i VAR_015980 | 162 | I → M в CMT2I; пациент несет также Asn-89 и Met-92. Ручное утверждение на основе эксперимента i
| 1 | 9045 9274 90_454 Естественный вариант i | G → R в CMT1B. Ручное утверждение на основе эксперимента в i
| 1 |
| Естественный вариант i VAR_004543 | 167 | G → A в CMT1B и DSS; суровый. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_004544 | 167 | G → R в CMT2I и DSS. Ручное утверждение на основе эксперимента в i
| 6EnsemblClinVar. | 1 | ||
| Естественный вариант i VAR_029985 | 170 | L → R в CMT1B. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_081765 | 215–248 | Отсутствует в CHN2. Ручное утверждение, основанное на эксперименте i
| 34 | |||
| Естественный вариант i VAR_029986 | 216 | T → ER в CMT1B; обозначается как «T216ER». | 1 | |||
| Естественный вариант i VAR_031892 | 221 | A → T в DSS. Ручное утверждение на основе эксперимента в i | 1 | |||
| Естественный вариант i VAR_054397 | 224 | D → Y в CMT1B; также у двух бессимптомных лиц из одной семьи. Ручное утверждение на основе эксперимента в i Соответствует варианту dbSNP: rs267607247EnsemblClinVar. | 1 | |||
| Естественный вариант i VAR_054398 | 227 | R → S в CMT1B. Ручное утверждение на основе эксперимента i
| 1 | |||
| Естественный вариант i VAR_021610 | 236 | K → E в CMT2I. Ручное утверждение, основанное на эксперименте на i
| 1 | |||
| Естественный вариант i VAR_029987 | 236 | Отсутствует в CMT1B. Ручное утверждение на основе эксперимента на i | 1 | |||
| Естественный вариант i VAR_004545 | 244 | R → L. Соответствует варианту dbSNP: rslinEnarse. | 1 | |||
| Функциональный ключ | Позиция (я) | Описание Действия | Графический вид | Длина | ||
В этом подразделе раздела «Последовательность» описывается последовательность встречающейся в природе альтернативной изоформы (ов) белка.Изменения в аминокислотной последовательности могут быть связаны с альтернативным сплайсингом, использованием альтернативного промотора, альтернативной инициацией или рибосомным сдвигом рамки. Альтернативная последовательность i VSP_045844 | 248 | K → KRLAGRAGDRGLGVESAKGP KVMVIEMELRKDEQSPELRP AVKSPSRTSLKNALKNMMGL NSDK в изоформе L-MPZ. | 1 |
Новая мутация гена MPZ, связанная с CMT в семье Вермонта
Мутация, влияющая на ген MPZ , оказалась связана с болезнью Шарко-Мари-Тута (CMT) у четырех членов одиночная семья.
Исследователи из Университета Вермонта опубликовали отчет о своей семье, озаглавленный «Новая мутация нуля миелинового белка у 3 поколений жителей Вермонтера с демиелинизирующей болезнью Шарко – Мари – Зуба», в журнале Journal of Clinical Neuromuscular Disease .
Команда представила случай семьи, в которой три поколения страдали прогрессирующей слабостью ног. Семейный анамнез также выявил двоюродную бабушку и прабабушку по отцовской линии, которые, как сообщалось, имели фенотип прогрессирующей слабости ног.
На основании этого были дополнительно обследованы две дочери, отец и бабушка по отцовской линии. Генетический анализ выявил единственное изменение одной единицы ДНК — C на T — в положении 314 последовательности гена MPZ . Эта мутация уже была описана ранее, но не сообщалось ни о каком эффекте или ассоциации с заболеванием. Необходимы дальнейшие исследования для оценки молекулярных последствий мутации MPZ .
Ген MPZ кодирует белок, называемый миелиновым белком ноль, который является основным компонентом защитного слоя нервных клеток, известного как миелиновая оболочка.В отсутствие этого белка слой миелина будет дефектным, и электрические импульсы, используемые для связи между нервными клетками, не будут проходить нормально.
Физическая оценка всех четырех членов семьи подтвердила, что они испытали потерю чувствительности, слабость ног и рук и деформации стоп. У всех также было снижение сухожильных рефлексов голени. Анализ способности нервных клеток передавать электрические импульсы подтвердил потерю миелина в дистальных нервных клетках с последующей гибелью нервных клеток.
«Новая замена пары оснований MPZ в этом семействе связана с наследственной дистальной демиелинизирующей невропатией и должна быть переклассифицирована как патогенная [вызывающая болезнь] по Шарко-Мари-Туту», — заявили исследователи.
Несмотря на схожие симптомы, представленные всеми членами семьи, начало болезни было очень разным. Бабушка по отцовской линии испытала первые симптомы слабости в ногах без судорог в возрасте 40 лет, а у отца начались судороги в подростковом возрасте, а слабость в ногах развилась только на третьем десятилетии жизни.Напротив, две дочери впервые проявили симптомы в раннем детстве, когда у одного ребенка родились тугие пяточные шнуры, которые повлияли на ее способность ходить.
Исследователи не смогли найти объяснения этому начальному разнообразию и прогрессивному представлению поколений. Необходимы дополнительные исследования, чтобы прояснить связь между идентифицированной мутацией MPZ и этой прогрессивной презентацией CMT.
Повышение уровня белка большого миелина до нуля приводит к нейропатии Шарко – Мари – Тута у мышей
Материалы
Химические вещества были самой высокой чистоты и были получены от Fujifilm Wako Pure Chemical Co., (Осака, Япония), Sigma – Aldrich Japan / Merck (Токио, Япония), Nacalai Tesque (Киото, Япония) и Kanto Chemical (Токио, Япония).
Мыши
Мышей L-MPZ были получены путем замены канонического стоп-кодона (TAG) на кодон аланина (GCG) с использованием системы редактирования генома CRISPR – Cas9 51 . Мыши-основатели L-MPZ были предоставлены Ресурсным центром лабораторных животных Университета Цукуба. Для обратного скрещивания мышей C57BL / 6J были приобретены в Charles River Laboratories Japan (Иокогама, Япония).
Были получены две линии мышей-основателей, которые передали замененные гены своим потомкам, которые были подтверждены геномным секвенированием. Мышей L-MPZ содержали на фоне C57BL / 6J. Генотипы определяли с помощью аллель-специфической ПЦР с дизайном праймеров, как описано у Hayashi et al. 52 . Аллель-специфическая ПЦР геномной ДНК хвоста мыши выполнялась с использованием Go Taq Green Master Mix (Promega, Мэдисон, Висконсин, США) со следующими праймерами из набора S: P0 STOP Allele Forward (P0_Stop_Allele_Fw), 5′-GGAGTCTCGCAAGGATAAGAGAT-3 ‘и MPZ обратный мутантный геном (MPZ_Mut_Geno_Rv), 5’-TGGTTCTACTGGGGGACTTGACTG-3 ‘; и набор праймеров: P0_MutA_Allele_Fw, 5’-GGAGTCTCGCAAGGATAAGAGAG-3 ‘и MPZ_Mut_Geno_Rv.Набор праймеров S генерировал продукт ПЦР размером 167 п.о. из геномной ДНК WT и Het, а набор праймеров A генерировал продукт ПЦР размером 167 п.о. из геномной ДНК Het и Hom (дополнительный рис. 1b). Условия ПЦР были следующими: предварительная денатурация при 95 ° C в течение 2 минут, затем 32 цикла амплификации: денатурация при 95 ° C в течение 30 секунд, отжиг праймеров при 62 ° C в течение 30 секунд и удлинение при 72 ° C в течение 30 секунд. с, с последним дополнительным удлинением при 72 ° C в течение 5 мин. Для генотипирования на уровне белка гомогенаты нервов каждой мыши анализировали с использованием гелей SDS-PAGE, окрашенных кумасси бриллиантовым синим R-250, или вестерн-блоттинга.Для содержания колонии использовали гетерозиготных животных. В качестве контрольных животных использовали однопометников или мышей WT соответствующего возраста. Линии мышей содержались в специально отведенной среде, свободной от специфических патогенов, в помещении для животных Токийского университета фармацевтики и наук о жизни в соответствии с университетскими руководящими принципами по уходу и использованию животных. Все протоколы для животных были одобрены Комитетом по институциональному использованию животных при Токийском университете фармацевтики и наук о жизни (номер одобрения: P16-95, P17-68, P18-76 и P19-46).
Гомогенизация
Гомогенаты седалищного нерва получали из 10-недельных мышей L-MPZ WT, Het и Hom. Мышей анестезировали внутрибрюшинной инъекцией анестезирующей комбинации, содержащей 0,3 мг -1 медетомидина, 4,0 мг -1 мидазолама и 5,0 мг -1 буторфанол 53 . Все процедуры выполнялись на льду или при 4 ° C. Гомогенаты получали, как описано ранее 13,14,54 с небольшими модификациями. Вкратце, седалищные нервы были рассечены и быстро заморожены в жидком азоте.Затем замороженную ткань измельчали в порошок с помощью BioMasher II (Nippi, Tokyo, Japan) в 0,32 М сахарозе, содержащей 5 мМ трис-HCl (pH 7,5), 2 мМ этиленгликольтетрауксусную кислоту, 0,75 мкМ апротинин, 1 мкМ лейпептин, 1 мкМ. пепстатин А и 0,4 мМ фенилметилсульфонилфторид (буфер для гомогенизации) и, при необходимости, добавляли PhosSTOP (Roche Diagnostics, Mannheim, Germany) для предотвращения дефосфорилирования. Для удаления хромосомной ДНК, клеточного дебриса и волокон гомогенаты центрифугировали при 800 × g в течение 10 минут, а супернатанты собирали и хранили в виде целых фракций гомогената при -80 ° C.Концентрацию белка определяли с использованием анализа бицинхониновой кислоты (Takara Bio, Shiga, Japan). Образцы исследовали с помощью SDS-PAGE или Phos-tag SDS-PAGE и иммуноблот-анализа с различными антителами.
Вестерн-блоттинг и Вестерн-блоттинг Phos-tag
Вестерн-блоттинг выполняли, как описано ранее 54 с небольшими модификациями. Вкратце, каждый образец разделяли на 7,5% или 12% гелях SDS-PAGE и переносили на мембраны из поливинилиденфторида (Merck Millipore, Billerica, MA, USA).Мембраны инкубировали в течение 1 ч с блокирующим буфером, содержащим 0,3% обезжиренного молока или 2% ослиной сыворотки в 50 мМ Tris-HCl (pH 7,4), 150 мМ NaCl и 0,05% Tween 20 (T-TBS) при комнатной температуре. Затем мембраны инкубировали в течение 1 ч с первичными антителами, разведенными в блокирующем буфере, и трижды промывали T-TBS перед инкубацией в течение 1 ч со вторичными антителами в T-TBS. После трехкратного промывания в T-TBS иммунореактивность определяли с помощью системы ECL (GE Healthcare Japan, Токио, Япония).И хемилюминесцентные изображения, и изображения предварительно окрашенных маркеров размера были получены в одном поле зрения с использованием LuminoGraphI (WSE-6100; корпорация ATTO, Токио, Япония). Маркеры размера выравнивали с положительными полосами на том же пятне с помощью программного обеспечения (Photoshop CS5; Adobe systems Inc, Сан-Хосе, Калифорния, США). Для количественной оценки интенсивности полос измеряли с помощью ImageJ (https://imagej.net/Welcome). Чтобы отличить фосфорилированные белки, был проведен Phos-tag (50 мкМ), содержащий 7,5% SDS-PAGE, с последующим вестерн-блоттингом в соответствии с инструкциями производителя (Fujifilm Wako Pure Chemical Co.).
Экстракция РНК и количественная ПЦР в реальном времени
Под наркозом мышей с применением комбинации анестетиков (0,3 мг -1 медетомидина, 4,0 мг кг -1 мидазолама и 5,0 мг кг -1 буторфанола) были умерщвлены цервикальным путем. вывих. Седалищные нервы иссекали и быстро замораживали в жидком азоте. Затем замороженную ткань измельчали в порошок с помощью BioMasher II. Тотальную РНК экстрагировали с использованием Trizol (Invitrogen, Carlsbad, CA, USA). Количественное определение мРНК P0, MBP или гена домашнего хозяйства, гипоксантинфосфорибозилтрансферазы (HPRT), проводили с использованием метода обнаружения в реальном времени на основе флуоресценции.КДНК первой цепи синтезировали с использованием набора для кПЦР ReverTra Ace (Toyobo, Осака, Япония). Затем была проведена ПЦР в реальном времени с использованием системы обнаружения ПЦР в реальном времени CFX Connect (Bio-Rad Laboratories, Геркулес, Калифорния, США) с наборами праймеров: P0_primer_Fw, 5′-CTTCAAGATGGACGCGACAC-3 ‘и P0_primer_Rv, 5′-AGAGTGTCTCAGCCTCCACAG -3 ′; MBP_primer_Fw, 5’-AACATTGTGACACCTCGAACA-3 ‘и MBP_primer_Rv, 5′-TGTCTCTTCCTCCCCAGCTA-3′; HPRT_primer_Fw, 5’-CCCTCTGGTAGATTGTCGCTTA-3 ‘и HPRT_primer_Rv, 5′-AGATGCTGTTACTGATAGGAAATCGA-3’.Относительное число копий транскриптов P0 или MBP на транскрипты HPRT определяли с использованием калибровочных стандартов для каждой из протестированных молекул.
Тест подвешивания за хвост и тест вращающегося стержня
Для выявления двигательной дисфункции обычно проверяется приведение (сцепление) задних конечностей с помощью теста подвески хвоста 55,56,57 . Для количественной оценки тяжести двигательных нарушений использовался модифицированный метод теста подвешивания за хвост, который был принят для скрининга потенциальных антидепрессантов 58 .Для анализа двигательной функции 10-недельных мышей L-MPZ WT, Het и Hom подвешивали за хвост и делали видеозаписи в течение 6 мин. Чтобы изучить двигательную функцию, углы, образованные между двусторонними задними конечностями, измеряли в двух временных точках после начала подвешивания хвоста: 1-2 мин (ранний период) и 4-5 мин (более поздний период) (рис. 1a и дополнительные видеоролики 1-6. ).
Двигательную функцию также исследовали с использованием роторного стержня MK-630B (Muromachi Kikai Co., Токио, Япония). Мышей помещали на покрытый резиной стержень и проводили два испытания с интервалом между испытаниями 10 мин.После тестовых испытаний было проведено испытание на вращающемся стержне. Скорость вращения стержня составляла 20 об / мин с каждыми 5-минутными испытаниями. Латентность измерялась, когда мышь перестала ходить по стержню, либо падая, либо цепляясь за стержень, и для каждой мыши рассчитывалась средняя задержка по трем независимым испытаниям.
Электрофизиологический анализ
NCV двигателя измеряли, как описано ранее. 59 с небольшими изменениями. Вкратце, скорость проводимости в двигательных нервных волокнах, иннервирующих подошвенную мышцу, была исследована под анестезией путем внутрибрюшинной инъекции комбинации анестетиков (0.3 мг кг -1 медетомидина, 4,0 мг кг -1 мидазолама и 5,0 мг кг -1 буторфанола). Температуру тела контролировали на бедре и поддерживали около 30 ° C с помощью грелки. В качестве анода и катода два подкожных игольчатых электрода из нержавеющей стали (0,5 × 27 G; Axon Systems, Hauppauge, NY, USA) помещали в подошвенную мышцу для обнаружения CMAP. Проксимальный и дистальный электроды стимуляции вводили в лодыжку и седалищную вырезку соответственно. Электростимуляция (0.Длительностью 1 мс) применяли каждую секунду с использованием стимулятора постоянного напряжения (DPS-007; Dia Medical Systems, Токио, Япония). Для обнаружения усиленных форм сигналов использовался цифровой регистратор данных (NR-2000; Keyence, Осака, Япония). Для записи и анализа использовалась программа WAVE SHOT 2000 (Keyence). Уровень запуска для записи был установлен на 0,1 В. Данные записывались в течение 10 мс (каждые 5 мкс, 2000 отсчетов) за 500 мкс до срабатывания триггера. Расстояние между дистальным и проксимальным электродами и разница в латентном периоде начала, полученная при стимуляции каждого электрода, использовались для расчета скорости проведения.Продолжительность формы волны измерялась между началом и конечной точкой каждого CMAP.
Исследование иммунофлуоресценции
Методы иммуноокрашивания были изменены, как описано ранее 59 . Седалищные нервы, полученные от анестезированных 10-недельных мышей, быстро препарировали и немедленно фиксировали в ледяном 4% параформальдегиде (PFA) в 0,1 M фосфатном буфере (PB) (pH 7,4) в течение 30 минут. После фиксации нервы подвергали криозащите с помощью 10% сахарозы в 0,1 M PB, а затем 30% сахарозы в течение ночи при 4 ° C.Затем нервы замораживали в OCT-соединении (Sakura Finetek, Токио, Япония). Срезы (10 мкм) вырезали с помощью криостата (CM1850; Leica Microsystems, Wetzlar, Германия) и помещали на предметное стекло FRONTIER (Matsunami Glass, Осака, Япония). Для приготовления раздвоенных волокон седалищные нервы после фиксации переносили в 0,1 М PB (pH 7,4). Затем нервы осторожно разделили, поместили на предметное стекло FRONTIER и высушили на воздухе. При необходимости образцы инкубировали с метанолом -20 ° C в течение 5 минут и промывали фосфатно-солевым буфером (PBS) перед предварительной инкубацией с 0.1 M PB (pH 7,4), содержащий 0,3% Triton X-100 и 10% нормальную козью сыворотку (PBTGS) в течение 1 часа. После этого образцы инкубировали в течение ночи при 4 ° C с первичными антителами, разбавленными до соответствующих концентраций в PBTGS. Образцы тщательно промывали в PBS с последующим нанесением флуоресцентно меченных вторичных антител (1: 2000 в PBTGS) в течение 1 часа при комнатной температуре. Наконец, меченые образцы промывали 0,01 М PBS каждые 5 мин три раза. Образцы помещали на покровные стекла с использованием Vectashield с DAPI (Vector Laboratories, Burlingame, CA, USA) и исследовали с помощью микроскопии BZ-X700 (Keyence) или конфокальной микроскопии FV-1000 (Olympus, Токио, Япония).
Антитела
Кроличьи поликлональные антитела против L-MPZ (иммуноокрашивание, 1: 4000; вестерн-блоттинг, 1: 40 000) получали, как описано ранее 13 . Кроличьи поликлональные антитела против Kv1.2 (иммуноокрашивание, 1: 400; Chemicon, Merck Millipore, прекращено), GFAP (иммуноокрашивание, 1:10; вестерн-блоттинг, 1: 1000; DAKO, Carpinteria, CA, США), фосфо- (Ser ) Субстрат PKC (вестерн-блоттинг, 1: 1000; Cell Signaling, Danvers, MT, США), DRP2 (иммуноокрашивание, 1:50; Sigma – Aldrich), GRP78 (BiP) (иммуноокрашивание, 1: 200; вестерн-блоттинг, 1: 2000; abcam, Кембридж, Великобритания), Iba1 (иммуноокрашивание, 1: 800; Fujifilm Wako Pure Chemical Co.) и рецептор маннозы (CD206) (иммуноокрашивание, 1: 200; abcam), куриные поликлональные антитела против нейрофасцина (иммуноокрашивание, 1: 400; R&D Systems, Миннеаполис, Миннесота, США), мышиные моноклональные антитела против Caspr (1: 400; клон K65 / 35; NeuroMab, Дэвис, Калифорния, США), натриевый канал (Pan) (иммуноокрашивание, 1: 400; клон K58 / 35; Sigma-Aldrich), бета-дистрогликан DAG 43 / DAG 31 (вестерн-блоттинг , 1: 1000; клон 43DAG1 / 8D5; Leica Biosystems, Ньюкасл-апон-Тайн, Великобритания), нейрофиламент (иммуноокрашивание, 1:10; clone2F11; Nichirei Biosciences, Токио, Япония), моэзин (иммуноокрашивание, 1: 100; клон M22; Sanko Junyaku, производство прекращено), KDEL (иммуноокрашивание, 1: 100; клон 10C3; Enzo Life Sciences, Inc., Фармингдейл, Нью-Йорк, США), актин (Вестерн-блоттинг, 1: 1,0000; Fujifilm Wako Pure Chemical Co.), GAPDH (Вестерн-блоттинг, 1: 10 000; Fujifilm Wako Pure Chemical Co.) и CD68 (иммуноокрашивание, 1: 1000; клон ED1; abcam), крысиные моноклональные антитела против MBP (иммуноокрашивание, 1: 200; вестерн-блоттинг, 1: 4000; Chemicon, Merck Millipore), ламинин альфа-2 (вестерн-блоттинг, 1: 1000; клон 4H8- 2; Santa Cruz Biotechnology, Dallas, TX, USA) и E-кадгерин (иммуноокрашивание, 1: 100; клон ECCD-2; Takara Bio, Kusatsu, Japan) и козье поликлональное антитело против P0 (1: 2000; Abnova, Тайбэй, Тайвань).Вторичные антитела, включая конъюгированные с Alexa 488 и 594 видоспецифические антитела (1: 2000; Molecular Probes / Thermo Fisher Scientific, Waltham, MA, USA) и конъюгированные с аминометил кумарином антитела против IgY курицы (1: 500; Jackson ImmunoResearch Laboratories, West Grove, PA, USA) использовали для иммуногистохимии. Для вестерн-блоттинга использовали конъюгированные с пероксидазой хрена антимышиные, антикроличьи, крысиные и козьи антитела IgG (1: 10 000; Jackson ImmunoResearch Laboratories).
Анализ с помощью электронной микроскопии
Восьминедельных мышей подвергали глубокой анестезии путем внутрибрюшинной инъекции комбинации анестетиков. Четырех мышей WT и четырех мышей L-MPZ Hom перфузировали 4% PFA и 2,5% глутаральдегида в 0,1 M PB (pH 7,4) и инкубировали в том же фиксаторе в течение ночи. Для ПЭМ образцы после фиксации в 2% тетроксиде осмия (Nisshin EM Co., Токио, Япония) в PBS, дегидратировали в серии градиентных этанолов, обрабатывали дегидратированным ацетоном и заключали в эпоксидную смолу Quetol 812 (Nisshin EM Co.). Для наблюдения с помощью SBF-SEM подготовка образцов, наблюдение и анализ полученных данных выполнялись, как описано ранее, с небольшими изменениями 60 . Вкратце, образцы обрабатывали 2% тетроксидом осмия (Nisshin EM Co.) и 1,5% ферроцианидом калия в PBS в течение 1 часа при 4 ° C, затем 1% тиокарбогидразидом в течение 20 минут при комнатной температуре, 2% водным раствором четырехокиси осмия в течение 30 минут. мин при комнатной температуре, 2% раствор уранилацетата в течение ночи при 4 ° C и раствор аспартата свинца в течение 30 мин при 65 ° C.Раствор аспартата свинца получали путем добавления нитрата свинца (TAAB, Aldermaston, UK) в 0,03 М 1-аспарагиновой кислоты до конечной концентрации 0,67% (pH 5,0–5,5). Затем образцы дегидратировали в серии градуированных этанолов, обрабатывали дегидратированным ацетоном и заливали эпоксидной смолой Quetol 812, содержащей черный порошок Ketjen 61 . Смолу инкубировали при 70 ° C в течение трех ночей для обеспечения полимеризации. Наблюдение миелиновой мембраны с помощью SBF-SEM проводили с использованием сканирующих электронных микроскопов Sigma или Merlin (Carl Zeiss, Оберкохен, Германия), оснащенных внутрикамерной ультрамикротомной системой 3View (Gatan, Плезантон, Калифорния, США).Последовательности последовательных изображений имели ширину 6144 × 6144 пикселей (4,7–6 нм на пиксель) и 200–1000 срезов с шагом 80 нм. Последовательные изображения обрабатывали с помощью FIJI (https://fiji.sc/), а анализ выполняли с помощью Amira (FEI, Токио, Япония).
Для процента аксонов без компактного миелина, которые были индивидуально заключены в оболочку шванновских клеток, аксоны были подсчитаны на одиночных ЭМ-изображениях. Связки ремаков были исключены из анализов. Диаметры аксонов и миелинизированных волокон были получены путем деления периметра на π .Измерение периодичности выполняли с помощью FIJI путем получения средних значений периодичности и медианы внешней, средней и внутренней частей (по три измерения в каждой части) в отдельных миелинизированных волокнах. Макрофаги на изображениях SBF-SEM были идентифицированы как клетки с относительно короткими, но сложными отростками с неровной поверхностью и многочисленными вакуолями, а также первичными и вторичными лизосомами. Количество макрофагов делили на объем наблюдения, чтобы получить плотность макрофагов (на 10 6 мкм 3 ).
Ширину каждого профиля ER измеряли как наибольшее расстояние между мембранами, которое было перпендикулярно более длинной оси профиля. Среднюю ширину ER каждой клетки объединяли от трех мышей дикого типа и трех гомозиготных мышей.
Окрашивание гематоксилином и эозином
Мышечные ткани собирали у 4-месячных мышей L-MPZ WT, Het и Hom и быстро замораживали с использованием сухого льда и изопентана. Срезы (10 мкм) вырезали криостатом и помещали на предметное стекло FRONTIER. Для гистологического окрашивания слайды инкубировали с раствором гематоксилина Майера (Fujifilm Wako Pure Chemical Co.) в течение 15 минут с последующей 10-минутной стиркой. Затем слайды инкубировали в 1% растворе эозина (Fujifilm Wako Pure Chemical Co.) в течение 1 мин. Затем предметные стекла промывали водопроводной водой в течение 10 мин. Затем их дегидратировали последовательно 70, 80 и 90% этанолом (EtOH) в течение 1 мин, трижды 100% этанолом в течение 1 мин и трижды ксилолом в течение 1 мин. Образцы помещали в MGK-S (Matsunami Glass), покрывали покровными стеклами и наблюдали с помощью микроскопа BZ-X700 (Keyence).
Статистика и воспроизводимость
Статистический анализ выполняли с использованием PRISM 5 (GraphPad Software, Ла-Хойя, Калифорния, США).Данные были выражены как среднее значение ± стандартная ошибка (SE) или стандартное отклонение (SD). Для сравнений использовали критерий Манна – Уитни U , критерий Стьюдента t или односторонний дисперсионный анализ (ANOVA) с последующим апостериорным тестом Тьюки или двухфакторным дисперсионным анализом ANOVA с последующими тестами множественного сравнения Бонферрони. p -значения <0,05 считались статистически значимыми. Подробности каждого статистического теста указаны в подписях к рисункам. Нечисловые данные показаны как репрезентативные результаты более чем трех независимых экспериментов.
Сводка отчетов
Дополнительная информация о дизайне исследований доступна в Сводке отчетов по исследованиям природы, связанной с этой статьей.
Тканевая экспрессия MPZ — сводка
АНДНО
Поле
Все Имя гена Класс белка Uniprot ключевое слово Хромосома Внешний идентификатор Оценка надежности ткань (IHC) Оценка надежности мышиный мозг Оценка надежности клеток (ICC) Белковый массив (PA) Вестерн-блот (WB) Иммуногистохимия (IHC) Иммуноцитохимия (ICC) Местоположение секретома Локация субклеточной аннотации (ICC) Субклеточная аннотация (ICC) (ICC) Фаза пика субклеточного клеточного цикла Экспрессия ткани (IHC) Категория ткани (РНК) Категория типа клеток (РНК) Категория линии клеток (РНК) Категория рака (РНК) Категория области мозга (РНК) Категория клеток крови (РНК) Категория клеток крови (РНК) Категория мозга мыши (РНК) Категория головного мозга свиньи (РНК) Прогностический рак Метаболический путьСводка доказательств Доказательства UniProt Нет данных доказательств HPA Доказательства MSС антителами Имеются данные о белках Сортировать по
Класс
Антигенные белки группы крови Гены, связанные с раком, гены-кандидаты, гены сердечно-сосудистых заболеваний, маркеры CD, белки, связанные с циклом лимонной кислоты, гены, связанные с заболеваниями, ферменты, одобренные FDA лекарственные мишени, рецепторы, сопряженные с G-белками, сопоставленные с neXtProt, сопоставленные с UniProt, SWISS-PROT, ядерные рецепторы, протеины, связанные с плазматической мембраной, прогнозируемые белки, секретируемые клетками, предсказанные белки, секретируемые плазматическим путем, белки, секретируемые через плазму, прогнозируемые белки, секретируемые лекарственным средством, белки, секретируемые плазматическим путем, белки, секретируемые клетками, Белки Рибосомные белки Белки, родственные РНК-полимеразе Факторы транскрипции Транспортеры Ионные каналы, управляемые напряжением
Подкласс
Класс
Биологический процесс Молекулярная функция Болезнь
Ключевое слово
Хромосома
1234567812131415161718122MTUnmappedXY
Надежность
ПовышеннаяПоддерживается УтвержденоНеопределено
Надежность
Поддерживается Одобрено
Надежность
ПовышеннаяПоддерживается УтвержденоНеопределено
Подтверждение
Поддерживается УтвержденоНеопределено
Проверка
Enhanced — CaptureEnhanced — GeneticEnhanced — IndependentEnhanced — OrthogonalEnhanced — РекомбинантнаяПоддерживаемаяПодтвержденнаяНеопределенная
Проверка
Enhanced — IndependentEnhanced — OrthogonalSupportedApprovedUncertain
Проверка
Enhanced — GeneticEnhanced — IndependentEnhanced — РекомбинантнаяПоддерживается УтвержденоНеопределено
Аннотация
Внутриклеточно и мембранно, секретно — неизвестное местоположение, секретируется в головном мозге, секретируется в женской репродуктивной системе, секретируется в мужской репродуктивной системе, секретируется в других тканях, секретируется в кровь, секретируется в пищеварительную систему, секретируется во внеклеточный матрикс
Расположение
актина filamentsAggresomeCell JunctionsCentriolar satelliteCentrosomeCleavage furrowCytokinetic bridgeCytoplasmic bodiesCytosolEndoplasmic reticulumEndosomesFocal адгезия sitesGolgi apparatusIntermediate filamentsKinetochoreLipid dropletsLysosomesMicrotubule endsMicrotubulesMidbodyMidbody ringMitochondriaMitotic chromosomeMitotic spindleNuclear bodiesNuclear membraneNuclear specklesNucleoliNucleoli фибриллярный centerNucleoli rimNucleoplasmPeroxisomesPlasma membraneRods & RingsVesicles
Поисковые запросы
РасширенныйПоддерживаемый УтвержденоНеопределеннаяВариация интенсивностиПространственная вариацияКорреляция интенсивности клеточного циклаПространственная корреляция клеточного цикла Биологически клеточный цикл Зависит от клеточного цикла пользовательских данныхЗависимый от клеточного цикла белокНезависимый от клеточного цикла белокЗависимый от клеточного цикла транскриптСтранскрипт, не зависящий от клеточного циклаМультилокализацияЛокализация 1Локализация 2Локализация 39Локализация 4Локализация 9Локализация 9Локализация 9
Расположение
AnyActin filamentsAggresomeCell JunctionsCentriolar satelliteCentrosomeCleavage furrowCytokinetic bridgeCytoplasmic bodiesCytosolEndoplasmic reticulumEndosomesFocal адгезия sitesGolgi apparatusIntermediate filamentsKinetochoreLipid dropletsLysosomesMicrotubule endsMicrotubulesMidbodyMidbody ringMitochondriaMitotic chromosomeMitotic spindleNuclear bodiesNuclear membraneNuclear specklesNucleoliNucleoli фибриллярный centerNucleoli rimNucleoplasmPeroxisomesPlasma membraneRods & RingsVesicles
Клеточная линия
анйа-431A549AF22ASC TERT1BJCACO-2EFO-21FHDF / TERT166GAMGHaCaTHAP1HBEC3-KTHBF TERT88HDLM-2HEK 293HELHeLaHep G2HTCEpiHTEC / SVTERT24-BHTERT-HME1HTERT-RPE1HUVEC TERT2JURKATK-562LHCN-M2MCF7NB-4OE19PC-3REHRH-30RPTEC TERT1RT4SH-SY5YSiHaSK-MEL-30SuSaTHP-1U-2 ОСУ-251 МГ
Тип
ProteinRna
Фаза
G1SG2M
Ткань
AnyAdipose tissueAdrenal glandAppendixBone marrowBreastBronchusCartilageCaudateCerebellumCerebral cortexCervix, uterineChoroid plexusColonDorsal rapheDuodenumEndometriumEpididymisEsophagusEyeFallopian tubeGallbladderHairHeart muscleHippocampusHypothalamusKidneyLactating breastLiverLungLymph nodeNasopharynxOral mucosaOvaryPancreasParathyroid glandPituitary glandPlacentaProstateRectumRetinaSalivary glandSeminal vesicleSkeletal muscleSkinSmall intestineSmooth muscleSoft tissueSole из footSpleenStomachSubstantia nigraTestisThymusThyroid glandTonsilUrinary bladderVagina
Тип ячейки
Выражение
Не обнаружено Низкое Среднее Высокое
Ткань
AnyAdipose tissueAdrenal glandBloodBone marrowBrainBreastCervix, uterineDuctus deferensEndometriumEpididymisEsophagusFallopian tubeGallbladderHeart muscleIntestineKidneyLiverLungLymphoid tissueOvaryPancreasParathyroid glandPituitary glandPlacentaProstateRetinaSalivary glandSeminal vesicleSkeletal muscleSkinSmooth muscleStomachTestisThyroid glandTongueUrinary bladderVagina
Категория
Обогащенная ткань Обогащенная группа Улучшенная ткань Низкая тканевая специфичность Не обнаружено Обнаружено у всех Обнаружено во многих Обнаружено в некоторых Обнаружено в одиночном Максимально выражено
Тип клетки
AnyAlveolar клетки типа 1Alveolar клетки типа 2B-cellsBasal железистой cellsBasal keratinocytesBipolar cellsCardiomyocytesCholangiocytesCiliated cellsClub cellsCollecting канал cellsCone фоторецептор cellsCytotrophoblastsDistal трубчатой cellsDuctal cellsEarly spermatidsEndothelial cellsEnterocytesErythroid cellsExocrine железистой cellsExtravillous trophoblastsFibroblastsGlandular cellsGranulocytesHepatocytesHofbauer cellsHorizontal cellsIntestinal эндокринного cellsIto cellsKupffer cellsLate spermatidsLeydig cellsMacrophagesMelanocytesMonocytesMucus-секретирующее cellsMuller глии cellsPancreatic эндокринных cellsPaneth cellsPeritubular cellsProximal трубчатых клетки стержневые фоторецепторные клетки клетки сертоли гладкомышечные клетки сперматоциты сперматогонии супрабазальные кератиноциты синцитиотрофобласты Т-клетки недифференцированные клетки уротелиальные клетки
Категория
Тип клеток обогащенный Группа обогащенный Тип клеток улучшенный Низкая специфичность типа клеток Не обнаружено Обнаружено во всех Обнаружено во многих Обнаружено в некоторых Обнаружено одним Обнаружено наивысшим уровнем экспрессии
Клеточная линия
анйа-431A549AF22AN3-CAASC diffASC TERT1BEWOBJBJ hTERT + BJ hTERT + SV40 большой Т + BJ hTERT + SV40 большой Т + RasG12VCACO-2CAPAN-2DaudiEFO-21FHDF / TERT166GAMGHaCaTHAP1HBEC3-KTHBF TERT88HDLM-2HEK 293HELHeLaHep G2HHSteCHL-60HMC-1HSkMCHTCEpiHTEC / SVTERT24-BHTERT-HME1HTERT- RPE1HUVEC TERT2JURKATK-562Karpas-707LHCN-M2MCF7MOLT-4NB-4NTERA-2OE19PC-3REHRH-30RPMI-8226RPTEC TERT1RT4SCLC-21HSH-3-SY5YSiHaSK-25-MGU-1 MGU-138-MGU-217-MGU-217-MGU-217-MGU-217-MGU-217-MGUSK-25-MGU-21-MGU-21-MGU-217-MGU-217 / 70U-266 / 84U-698U-87 MGU-937WM-115
Категория
Клеточная линия обогащена Группа обогащена Линия клеток улучшена Низкая специфичность линии клеток Не обнаружено Обнаружено у всех Обнаружено во многих Обнаружено в некоторых Обнаружено в одиночном Максимально выражено
Рак
ЛюбойРак грудиРак шейкиКолоректальный ракРак эндометрияГлиомаРак головы и шеиРак печениРак легкихМеланомаРак яичниковРак поджелудочной железыРак предстательной железыРак почкиРак желудкаРак тестируемого ракаРак щитовидной железыРак уротелия
Категория
Обогащенный раком Группа обогащенныйРак усиленный Низкая специфичность рака Не обнаружено Обнаружено у всех Обнаружено во многих Обнаружено в некоторых Обнаружено в одиночном Максимально выражено
Область головного мозга
Любая АмигдалаНазальные ганглии МозжечокКора больших полушарий Гиппокамп Формирование Гипоталамус Средний мозг Обонятельная область Мост и мозговое вещество Таламус
Категория
Обогащенная по региону Обогащенная по группе Улучшенная по региону Низкая специфичность по региону Не обнаружено Обнаружено во всех Обнаружено во многих Обнаружено в некоторых Обнаружено в одиночном Максимально выражено
Тип клеток
AnyBasophilClassical monocyteEosinophilGdT-cellIntermediate monocyteMAIT T-cellMemory B-cellMemory CD4 T-cellMemory CD8 T-cellMyeloid DCNaive B-cellNaive CD4 T-cellNaive CD8 T-cellNeutrophilas DC-PBT9
Категория
Тип клеток обогащенный Группа обогащенный Тип клеток улучшенный Низкая специфичность типа клеток Не обнаружено Обнаружено во всех Обнаружено во многих Обнаружено в некоторых Обнаружено одним Обнаружено наивысшим уровнем экспрессии
Клеточная линия
AnyB-клетки Дендритные клетки Гранулоциты МоноцитыNK-клетки Т-клетки
Категория
Линия обогащена Группа обогащена Линия расширена Низкая специфичность линии Не обнаружено Обнаружено во всех Обнаружено во многих Обнаружено в одиночной Наивысшей экспрессии
Область мозга
AnyAmygdalaБазальные ганглии мозжечокКора большого мозга мозолистое тело Формирование гиппокампа Гипоталамус Средний мозг Обонятельная область Гипофиз Мосты и продолговатый мозг РетинаТаламус
Категория
Обогащенная по региону Обогащенная по группе Улучшенная по региону Низкая специфичность по региону Не обнаружено Обнаружено во всех Обнаружено во многих Обнаружено в некоторых Обнаружено в одиночном Максимально выражено
Область головного мозга
AnyAmygdalaБазальные ганглии мозжечокКора большого мозга мозолистое тело Формирование гиппокампа Гипоталамус Средний мозг Обонятельная область Гипофиз Мосты и продолговатый мозг Ретина Спинной мозг Таламус
Категория
Обогащенная по региону Обогащенная по группе Улучшенная по региону Низкая специфичность по региону Не обнаружено Обнаружено во всех Обнаружено во многих Обнаружено в некоторых Обнаружено в одиночном Максимально выражено
Рак
Рак молочной железыРак маткиКолоректальный ракКолоректальный ракРак эндометрияГлиомаРак головы и шеиРак печениРак легкихРак легкихМеланомаРак яичниковРак поджелудочной железыРак предстательной железыРак почкиРак почкиРак почкиРак желудкаРак рака щитовидной железы
Прогноз
Благоприятный Неблагоприятный
Путь
Гидролиз ацил-КоА Метаболизм ацилглицеридов Аланин; метаболизм аспартата и глутамата, метаболизм аминосахаров и нуклеотидных сахаров, биосинтез аминоацил-тРНК, метаболизм андрогенов, метаболизм арахидоновой кислоты, метаболизм аргинина и пролина, метаболизм скорбата и альдарата, бета-окисление жирных кислот с разветвленной цепью (митохондриальные) (митохондриальные), бета-окисление бета-ненасыщенных жирных кислот, бета-ненасыщенные 6 диоксидных кислот диненасыщенные жирные кислоты (n-6) (пероксисомальные) Бета-окисление жирных кислот с четной цепью (митохондриальные) Бета-окисление жирных кислот с четной цепью (пероксисомальные) Бета-окисление жирных кислот с нечетной цепью (митохондрии) Бета-окисление фитановых кислот кислотное (пероксисомальное) Бета-окисление полиненасыщенных жирных кислот (митохондриальные) Бета-окисление ненасыщенных жирных кислот (n-7) (митохондриальное) Бета-окисление ненасыщенных жирных кислот (n-7) (пероксисомальное) Бета-окисление ненасыщенных жирных кислот ( n-9) (митохондрии) Бета-окисление ненасыщенных жирных кислот (n-9) (пероксисомальный) Метаболизм бета-аланина Биосинтез желчных кислот Рециклинг желчных кислот Биоптерин me таболизм, метаболизм биотина, биосинтез группы крови, метаболизм бутаноатов, метаболизм С5-разветвленной двухосновной кислоты, карнитиновый челнок (цитозольный), карнитиновый челнок (эндоплазматический ретикуляр), карнитиновый челнок (митохондриальный), карнитиновый челнок (пероксисомальный), холестерин-метаболический путь, биосинтез холестерина, биосинтез холестерина, биосинтез холестерина, путь биосинтеза, метаболизм, метаболизм, биосинтез холестерина, метаболизм, биосинтез холестерина, метаболизм, биосинтез холестерина Биосинтез гепарансульфата Деградация хондроитинсульфата Синтез CoA Метаболизм цистеина и метионина Метаболизм лекарственных препаратов Метаболизм эстрогенов Метаболизм эфирных липидов Реакции обмена / спроса Активация жирных кислот (цитозольный) Активация жирных кислот (эндоплазматическая ретикулярная цепь) Биосинтез жирной кислоты биосинтез (ненасыщенные) Десатурация жирных кислот (четная цепь) Десатурация жирных кислот (нечетная цепь) Удлинение жирных кислот (четная цепь) Удлинение жирных кислот (нечетная цепь) Окисление жирных кислот Метаболизм жирных кислот Формирование d гидролиз эфиров холестерина, метаболизм фруктозы и маннозы, метаболизм галактозы, биосинтез глюкокортикоидов, метаболизм глутатиона, метаболизм глицеролипидов, метаболизм глицерофосфолипидов, глицин; серин и треонин metabolismGlycolysis / GluconeogenesisGlycosphingolipid биосинтез-ganglio seriesGlycosphingolipid биосинтез-Globo seriesGlycosphingolipid биосинтез-лакто и neolacto seriesGlycosphingolipid metabolismGlycosylphosphatidylinositol (GPI) -anchor biosynthesisHeme degradationHeme synthesisHeparan сульфат degradationHistidine metabolismInositol фосфат metabolismIsolatedKeratan сульфат biosynthesisKeratan сульфат degradationLeukotriene metabolismLinoleate metabolismLipoic кислота metabolismLysine metabolismMetabolism из другой аминокислоты acidsMetabolism ксенобиотиков пути цитохром P450 Разное Метаболизм N-гликанов Метаболизм никотинатов и никотинамидов Метаболизм азота Метаболизм нуклеотидов Метаболизм O-гликанов Метаболизм жирных кислот омега-3 Метаболизм жирных кислот Омега-6 Метаболизм жирных кислот Окислительное фосфорилированиеПантотенат и КоА Биосинтез Пуронинатный путь метаболизм глюконатина тирозин и триптофан biosynthesisPhosphatidylinositol фосфат metabolismPool reactionsPorphyrin metabolismPropanoate metabolismProstaglandin biosynthesisProtein assemblyProtein degradationProtein modificationPurine metabolismPyrimidine metabolismPyruvate metabolismRetinol metabolismRiboflavin metabolismROS detoxificationSerotonin и мелатонина biosynthesisSphingolipid metabolismStarch и сахароза metabolismSteroid metabolismSulfur metabolismTerpenoid магистральная biosynthesisThiamine metabolismTransport reactionsTriacylglycerol synthesisTricarboxylic цикл кислота и глиоксилат / дикарбоксилат metabolismTryptophan metabolismTyrosine metabolismUbiquinone synthesisUrea cycleValine; лейцин; Метаболизм витамина A Метаболизм витамина B12 Метаболизм витамина B2 Метаболизм витамина B6 Метаболизм витамина C Метаболизм витамина D Метаболизм витамина E Метаболизм ксенобиотиков
Категория
Доказательства на уровне белка Доказательства на уровне транскрипта Нет доказательств человеческого белка / транскрипта
Оценка
Доказательства на уровне белка Доказательства на уровне транскрипта Нет доказательств человеческого белка / транскрипта
Оценка
Доказательства на уровне белка Доказательства на уровне транскрипта Нет доказательств человеческого белка / транскрипта
Оценка
Доказательства на уровне белка Доказательства на уровне транскрипта Нет доказательств человеческого белка / транскрипта
Оценка
Доказательства на уровне белка Доказательства на уровне транскрипта Нет доказательств человеческого белка / транскрипта
В атласе
TissueCellPathologyBrainBlood — конц.иммуноанализ Кровь — конц. масс-спектрометрия кровь — горох детектированный
Столбец
Позиция гена Оценка, специфичная для ткани Прогностическая надежность (IF) Надежность (IH)
Addgene: промотор MPZ (P0) pGL3-TATA
Эти плазмиды созданы вашими коллегами. Пожалуйста, примите во внимание Главный исследователь, процитируйте статью, в которой были описаны плазмиды: и включите Addgene в Материалы и методы ваших будущих публикаций.
Для вашего Материалы и методы раздел:
Промотор MPZ (P0) pGL3-TATA был подарком от Джерри Крэбтри (Плазмида Addgene # 21259; http: // n2t.сеть / addgene: 21259; RRID: Addgene_21259)
Для вашего Ссылки раздел:
Передача сигналов кальциневрина / NFAT необходима для регулируемой нейрегулином дифференцировки шванновских клеток .Као С.К., Ву Х., Се Дж., Чанг С.П., Раниш Дж.А., Грэф И.А., Крэбтри Г.Р. Наука. 2009 30 января. 323 (5914): 651-4. 10.1126 / science.1166562 PubMed 136
Об авторе