Отчетность в ифнс за год: Сроки сдачи отчетности в 2021, 2020, 2019, 2018 и 2017 году (таблица) — Контур.Бухгалтерия
В налоговую |
||
| Среднесписочная численность | Отдельный отчёт сдавать не нужно, с 2021 он вошёл в РСВ за год | |
| Расчёт по страховым взносам |
До 1 февраля — за 2020 год До 30 апреля — за 1 квартал 2021 года До 30 июля — за полугодие До 1 ноября — за 9 месяцев |
Отчёт о страховых взносах на пенсионное, медицинское и социальное страхование, которые вы платите за сотрудников в налоговую. Подробнее о РСВ читайте в статье. |
| 6-НДФЛ |
До 1 марта — за 2020 год До 30 апреля — за 1 квартал 2021 года До 31 июля — за полугодие До 1 ноября — за 9 месяцев |
Не нужно сдавать, если вы не платили зарплату сотрудникам, дивиденды учредителям, и другие физлица не получали от вас доходы в тот период, за который нужно отчитаться. |
| 2-НДФЛ | Отдельный отчёт сдавать не нужно, с 2021 он вошёл в 6-НДФЛ за год | Не нужно сдавать, если вы не платили зарплату сотрудникам, дивиденды учредителям, и другие физлица не получали от вас доходы в 2020 году. Подробнее о 2-НДФЛ читайте в статье. |
В пенсионный фонд |
||
| Отчёт СЗВ-Стаж за 2020 год | До 1 марта 2021 года. | Новый отчёт о стаже сотрудников. Его нужно сдавать раз в год. |
| Отчёт СЗВ-М в ПФР | Ежемесячно до 15 числа — за предыдущий месяц. Если дата выпадает на выходной или праздник, то срок переносится на следующий рабочий день. | Отчёт со списком всех работающих у вас сотрудников. |
| Отчёт СЗВ-ТД | Не позже, чем на следующий рабочий день после приёма или увольнения сотрудника; по другим кадровым событиям — до 15 числа следующего месяца. |
Отчёт о трудовой деятельности сотрудников. На его основании ПФР будет формировать электронные трудовые книжки. |
В фонд социального страхования |
||
| Отчёт 4-ФСС |
До 20 января на бумаге, до 25 января в электронном виде — за 2020 год. До 20 апреля на бумаге, до 26 апреля в электронном виде — за I квартал. До 20 июля на бумаге, до 26 июля в электронном виде — за полугодие. До 20 октября на бумаге, до 26 октября в электронном виде — за 9 месяцев. |
Отчёт о взносах на травматизм сотрудников, которые вы платите в ФСС. |
| Только для ООО — подтвердить основной вид деятельности | До 15 апреля 2021 года |
Основной вид деятельности — тот, от которого организация в 2020 году получила больше всего доходов. ИП не подтверждают вид деятельности, а ставка взносов на травматизм определяется по основному коду ОКВЭД. |
Отчетность по итогам 2020 для ИП и ООО на УСН, ЕНВД
Отчётность для всех ИП и ООО в налоговую
Отчётность по УСН
Заплатить налог и сдать декларацию: до 30 апреля 2021 года — для ИП, до 31 марта 2021 года — для ООО.
Подробнее про УСН и отчётность на этой системе налогообложения читайте в статье Упрощённая система налогообложения.
Последняя отчётность по ЕНВД
Сдать декларацию до 20 января 2021 года, заплатить налог до 25 января 2021 года.
Подробнее про отчётность по ЕНВД читайте в статье.
Сдавайте отчётность в три клика
Эльба рассчитает налог и подготовит отчётность для бизнеса на УСН, ЕНВД и патенте. А ещё поможет cформировать счета, акты и накладные.
А ещё поможет cформировать счета, акты и накладные.
Только для ООО — сдать бухгалтерскую отчётность
До 31 марта 2020 года.
Это отчёт, в котором содержится информация в денежном выражении об имуществе, долгах, выручке, прибыли, расходах и финансовых результатах. Бухотчётность составляют и утверждают по итогам каждого года и сдают в налоговую в электронной форме.
Отчётность за сотрудников — для всех ООО и ИП с сотрудниками
6-НДФЛ в налоговую
До 1 марта 2021 года — за 2020 год.
Отчёт нужно сдать, если за прошедший год физлица получали от вас доходы. Например, вы выдавали зарплату сотрудникам, дивиденды учредителям или беспроцентные займы. В отчёте 6-НДФЛ отражаются сведения о доходах физлиц и удержанном налоге.
Если вы не выплачивали доходы физикам, нулевой отчёт сдавать не нужно.
О нюансах 6-НДФЛ читайте в статье.
2-НДФЛ в налоговую
До 1 марта 2021 года — за 2020 год.
Не нужно сдавать, если вы не платили зарплату сотрудникам, дивиденды учредителям, и другие физлица не получали от вас доходы в 2019 году.
Подробнее о 2-НДФЛ читайте в статье.
Расчёт по страховым взносам в налоговую
До 30 января 2021 года — за 2020 год.
РСВ — ежеквартальный отчёт, который сдают ИП с сотрудниками и все ООО. Из него фонд узнаёт о ваших сотрудниках, их зарплате и начисленных страховых взносах. В отчёте нужно показать сотрудников как по трудовому, так и по гражданско-правовому договору.
Если в ООО нет сотрудников, то всё равно нужно сдать нулевой отчёт. ИП без сотрудников не отчитываются по этой форме.
О том, что это за отчёт и как заполнить его в Эльбе, читайте в статье «Новый отчёт за сотрудников в налоговую».
СЗВ-М в пенсионный фонд
До 15 января 2021 года — за декабрь 2020 года, и далее — каждый месяц.
СЗВ-М нужно сдавать каждый месяц ИП с сотрудниками и всем ООО. Отчёт содержит список работников, их ИНН и СНИЛС.
Отчёт содержит список работников, их ИНН и СНИЛС.
Если вы — ИП без сотрудников, сдавать этот отчёт не нужно. А в каждом ООО есть хотя бы один сотрудник — директор. Отразите его в СЗВ-М, даже если он не получает зарплату.
Подробнее об отчёте СЗВ-М читайте в статье.
4-ФСС в фонд социального страхования
До 20 января 2021 года на бумаге, до 25 января 2021 года в электронном виде — за 2020 год.
ИП с сотрудниками по трудовому договору и все ООО отчитываются в ФСС. В отчёте 4-ФСС отражаются список сотрудников, их зарплата и размер страховых взносов на травматизм.
Если в ООО нет ни одного сотрудника, нужно сдать нулевой 4-ФСС. ИП, который уволил всех сотрудников, но не снялся с учёта в ФСС как работодатель, тоже продолжает отчитываться.
Только ООО — подтвердить вид деятельности в ФСС
До 15 апреля 2021 года.
О том, как и зачем это делать, читайте в статье.
Сдаём отчётность за 2020 год новость от 17.
 03.2021
03.2021Отчётность за 2020 год необходимо сдавать по новым правилам. Об изменениях в бухгалтерской отчётности, налоговой отчётности упрощенцев и декларациях, на которые нужно обратить особое внимание, читайте в статье ведущего экономиста-консультанта Татьяны Чапаевой.
Бухгалтерская отчётностьВ 2020 году по-прежнему применяются формы бухгалтерской отчётности, утверждённые Приказом Минфина России от 02.07.2010 № 66н.
Состав бухгалтерской отчётности — баланс, отчёт о финансовых результатах и приложения (ст. 14 Федерального закона от 06.12.2011 № 402-ФЗ (ред. от 26.07.2019)).
Отчёт о финансовых результатах составляйте по изменённой форме. Нововведения, внесённые Приказом Минфина России от 02.07.2010 № 66н (ред. от 19.04.2019), вступают в силу начиная с бухгалтерской отчётности за 2020 год. Налог на прибыль в бухотчётности отражают по новым правилам.
Остальные формы и правила заполнения отчётности не изменились.
Упрощённую бухгалтерскую отчётность могут сдавать все малые предприятия, кроме перечисленных в части 5 статьи 6 Закона о бухучёте.
В состав бухгалтерской отчётности малых предприятий входят только две сокращённые формы — баланс и отчёт о финансовых результатах. Пояснения и другие приложения к отчётности можно не сдавать.
С отчётности за 2020 год все организации обязаны представлять в налоговый орган годовую бухгалтерскую отчётность в электронной форме (ч. 5 ст. 18 Федерального закона от 06.12.2011 № 402-ФЗ, Приложение к Письму Минфина России от 29.12.2020 № 07-04-09/115445). Годовая бухгалтерская отчётность и аудиторское заключение о ней представляются в форматах, утверждённых Приказом ФНС России от 13.11.2019 № ММВ-7-1/570@.
Срок сдачи бухгалтерской отчётности за 2020 год — 31.03.2021.
Рекомендуем посмотреть:
Налоговая отчётность упрощенцевДля представления отчётности по УСН за 2020 год применяется форма, утверждённая Приказом ФНС России от 26. 02.2016 № ММВ-7-3/99@. Код КНД для декларации по УСН за 2020 год — 1152017.
02.2016 № ММВ-7-3/99@. Код КНД для декларации по УСН за 2020 год — 1152017.
С 2021 года по УСН используется форма по КНД 1152017, утверждённая Приказом ФНС России от 25.12.2020 № ЕД-7-3/958@.
Однако в соответствии с пояснениями по Письму ФНС России от 02.02.2021 № СД-4-3/1135@, в целях исключения формального подхода, связанного с отказом в приёме налоговых декларацией по УСН за 2020 год, в том числе после вступления в силу Приказа № ЕД-7-3/958@, налоговым органам надлежит обеспечить приём указанной отчётности по формам и форматам, утверждённым Приказом ФНС России от 26.02.2016 № ММВ-7-3/99@, а также Приказом № ЕД-7-3/958@, в случае их представления с 20.03.2021.
В новой декларации учтены изменения в главу 26.2 НК РФ, внесённые Федеральным законом от 31.07.2020 № 266-ФЗ. В связи с этим форма декларации дополнена графами для указания кода признака применения налоговой ставки (стандартной или переходной повышенной). В разделах 1.1 и 1.2 обновлённой декларации появилась новая строка 101 «Сумма налога, уплаченная в связи с применением ПСН, подлежащая зачёту».
По итогам календарного года организации на УСН представляют налоговую декларацию в налоговый орган по месту своего нахождения не позднее 31 марта года, следующего за истекшим налоговым периодом (за исключением случаев, предусмотренных п. 2 и 3 ст. 346.23 НК РФ) (пп. 1 п. 1 ст. 346.23 НК РФ). За 2020 год — 31.03.2021.
Индивидуальные предприниматели на УСН представляют декларацию по итогам года по месту своего жительства не позднее 30 апреля года, следующего за истекшим налоговым периодом (за исключением случаев, предусмотренных п. 2 и 3 ст. 346.23 НК РФ) (пп. 2 п. 1 ст. 346.23 НК РФ). За 2020 год — 30.04.2021.
Рекомендуем посмотреть:
Декларация по налогу на прибыльФорма декларации по налогу на прибыль за 2020 год и Порядок её заполнения утверждены Приказом ФНС России от 23.09.2019 № ММВ-7-3/475@ (в ред. Приказа ФНС России от 11.09.2020 № ЕД-7-3/655@). Форма по КНД 1151006.
Срок сдачи годовой декларации по прибыли для всех организаций одинаковый — не позднее 28 марта года, следующего за истекшим годом (п. 1 ст. 289 НК РФ).
1 ст. 289 НК РФ).
Срок сдачи декларация по налогу на прибыль за 2020 год — 29.03.2021.
Рекомендуем посмотреть:
Декларация по НДСФорма декларации по НДС и Порядок её заполнения утверждены Приказом ФНС России от 29.10.2014 № ММВ-7-3/558@ (ред. от 19.08.2020).
Новый бланк утверждён Приказом ФНС России от 19.08.2020 № ЕД-7-3/591@, применяется начиная с представления налоговой декларации по налогу на добавленную стоимость за четвёртый квартал 2020 года.
Срок предоставления декларации по НДС за первый квартал 2021 года – не позднее 26.04.2021.
Рекомендуем посмотреть:
Декларации по транспортному и земельному налогамДекларации за 2020 год сдавать не надо. После уплаты налога за год инспекция отправит вам свой расчёт налога. О транспорте или земле, которых не будет в этом расчёте, надо сообщить в инспекцию (ст. 23 НК РФ).
Декларация по налогу на имуществоЕсли декларация по налогу на имущество представляется до 13 марта 2021 года (включительно), её следует представить по форме, которая установлена приложением 1 к Приказу ФНС России от 14. 08.2019 № СА-7-21/405@ (в ред. Приказа ФНС России от 28.07.2020 № ЕД-7-21/475@). Однако данная форма не учитывает положение пункта 1 статьи 386 НК РФ, согласно которому в декларацию нужно включать сведения о среднегодовой стоимости объектов движимого имущества, учтённых на балансе организации в качестве объектов основных средств.
08.2019 № СА-7-21/405@ (в ред. Приказа ФНС России от 28.07.2020 № ЕД-7-21/475@). Однако данная форма не учитывает положение пункта 1 статьи 386 НК РФ, согласно которому в декларацию нужно включать сведения о среднегодовой стоимости объектов движимого имущества, учтённых на балансе организации в качестве объектов основных средств.
С 14 марта 2021 года декларацию нужно подавать по форме, приведённой в приложении 1 к Приказу ФНС России от 09.12.2020 № КЧ-7-21/889@ (п. 2 данного Приказа). Эта форма декларации содержит раздел для отражения сведений о среднегодовой стоимости объектов движимого имущества в соответствии с пунктом 1 статьи 386 НК РФ.
Если в организации имеется движимое имущество, учитываемое как объекты основных средств, рекомендуем подавать декларацию по новой форме.
По общему правилу срок представления декларации — не позднее 30 марта года, следующего за истекшим (п. 3 ст. 386 НК РФ).
Срок сдачи декларации по налогу на имущество за 2020 год — 30.03. 2021.
2021.
Рекомендуем посмотреть:
Декларация по ЕСХНПриказом ФНС России от 18.12.2020 № ЕД-7-3/926@ внесены изменения в форму, порядок заполнения и формат представления налоговой декларации по единому сельскохозяйственному налогу в электронной форме, утверждённые Приказом ФНС России от 28.07.2014 № ММВ-7-3/384@. Приказ № ЕД-7-3/926@ вступает в силу 29.03.2021 и применяется начиная с представления налоговой декларации по ЕСХН за налоговый период 2020 года.
Налоговая декларация по ЕСХН по итогам налогового периода в общем случае должна быть представлена не позднее 31 марта года, следующего за истекшим налоговым периодом (п. 2 ст. 346.10 НК РФ).
ФНС России разрешила представлять декларацию по ЕСХН по старой форме и после вступления в силу приказа о новой (Письмо ФНС России от 12.02.2021 № СД-4-3/1776@ «О налоговой декларации по ЕСХН»).
Срок представления декларации по ЕСХН за 2020 год — 31.03.2021.
Рекомендуем посмотреть:
Декларации по 6-НДФЛ и 2-НДФЛДекларацию по 6-НДФЛ за первый квартал 2021 года сдают по новой форме, за 2020 год отчёт предоставляется по старой форме.
С отчётности за 2021 год справка 2-НДФЛ отменена — сведения из справки включены в годовой отчёт 6-НДФЛ. 2-НДФЛ за 2020 год предоставляется в прежний срок.
Срок представления 6-НДФЛ и 2-НДФЛ за 2020 год — 01.03.2021.
Рекомендуем посмотреть:
Все компании и ИП должны сдавать статистическую отчётность. Конкретные формы статотчётности зависят от вида деятельности, статуса (является субъектом малого/среднего предпринимательства и т. д.) и иных показателей.
До 01.04.2021 организации, относящиеся к малым предприятиям (в том числе к микропредприятиям), должны сдать статформу № МП-сп «Сведения об основных показателях деятельности малого предприятия за 2020 год». А все ИП — форму № 1-предприниматель «Сведения о деятельности индивидуального предпринимателя за 2020 год».
Узнать полный перечень форм статотчётности, подлежащих представлению налогоплательщиком, можно на сайте статистики по ИНН, перейдя по ссылке Получение данных о кодах статистики и перечня форм.
Важно! Если вы представите в налоговый орган декларацию (расчёт) не по установленной форме (формату), это является основанием для отказа в её приёме (пп. 3 п. 19 Административного регламента ФНС России (утв. Приказом ФНС России от 08.07.2019 № ММВ-7-19/343@)).
Таким образом, бухотчётность за 2020 год необходимо сдавать по новым правилам. Все организации, и в частности субъекты СМП, представляют бухгалтерскую отчётность только в электронной форме. Применяются изменения по форме отчётности о финансовых результатах с отчётности за 2020 год.
По сдаче отчётности за 2020 год Минфин России выпустил рекомендации аудиторам по проверке бухгалтерской отчётности за 2020 год (приложение к Письму Минфина России от 29.12.2020 № 07-04-09/115445).
Также внесены имения и в формы налоговой отчётности: по декларации по НДС, по налогу на прибыль, по налогу на имущество, по УСН и ЕСХН и по 6-НДФЛ.
Ряд деклараций за 2020 год сдавать не нужно. В частности, не действует обязанность представлять декларации отмены по земельному и транспортному налогам.
Сведения о среднесписочной численности за 2020 год также отдельно подавать не нужно. Среднесписочную численность теперь указывают в РСВ (ст. 80 НК РФ).
Правильное заполнение актуальных форм отчётности и своевременное представление их в сроки помогут вам закончить период без стресса и штрафов.
Сроки сдачи отчетности в 2021 году — Контур.Экстерн
Количество отчетов и порядок их сдачи меняются каждый год. Контролирующие органы вводят новые формы, убирают старые, пересматривают сроки сдачи и изменяют бланки.
В статье расскажем, о каких изменениях в отчетности с 2021 года должен знать бухгалтер. Это подсказки с видами отчетов по каждой системе налогообложения, бланками, сроками и особенностями сдачи. Проверяйте себя каждый квартал, чтобы вовремя сдавать отчеты и не забывать об изменениях в формах и сроках.
Шпаргалка подходит организациям и предпринимателям на всех системах налогообложения. Изучите информацию и составьте для себя график сдачи деклараций, расчетов и сведений на 2021 год.
Общая система налогообложения
На ОСНО отчетности больше, чем на специальных налоговых режимах. Бухгалтерам организаций и ИП на общей системе в 2021 году надо сдать больше десяти отчетов.
Организации отчитываются по всем налогам и взносам, которые платят на ОСНО: налог на прибыль, НДС, НДФЛ, налог на имущество организаций, акцизы. А еще надо отчитаться по сотрудникам. ИП на ОСН не сдают декларацию по налогу на имущество, а вместо отчета по прибыли сдают 3-НДФЛ, других отличий от организаций нет.
Декларация по НДС
Организации и предприниматели на ОСНО отчитываются по НДС каждый квартал (ст. 174 НК РФ). Платить налог сразу не обязательно, его можно разбить на три части и платить один раз в месяц. Внимательно заполняйте декларацию и не допускайте отражения недостоверных сведений. Сверьте счета-фактуры с контрагентами, чтобы не подать налоговой разные данные. Например, если вы приняли к зачету налог, который поставщик не отразил, у инспекции возникнут вопросы и она потребует пояснений.
Кто сдает. Российские организации и ИП на ОСН или ЕСХН, налоговые агенты и неплательщики-НДС, иностранные организации, импортеры, комиссионеры, доверительные управляющие, участники товариществ.
Сроки сдачи. В 2021 году сдать декларацию по НДС нужно не позднее следующих сроков:
- за IV квартал 2020 года — 25 января 2021 года;
- за I квартал 2021 года — 26 апреля 2021 года;
- за II квартал 2021 года — 26 июля 2021 года;
- за III квартал 2021 года — 25 октября 2021 года.
За четвертый квартал 2021 года отчитаться нужно уже в январе 2022 года. Если ничего не изменится, крайний срок будет установлен на 25 января.
В сроках учтен перенос даты сдачи с выходных и праздничных дней на рабочие. Например, для декларации за I квартал срок сдачи выпадает на воскресенье. Его переносят на понедельник, чтобы не заставлять бизнес работать в выходной.
Бланк и формат сдачи. Форма декларации, действующая с IV квартала 2020 года, утверждена приказом ФНС от 19.08.2020 № ЕД-7-3/591@. Сдавать декларацию по НДС нужно в электронной форме. Право использовать бумажный бланк осталось только у некоторых налоговых агентов и тех, кто платит НДС с электронных услуг.
Посредники-неплательщики НДС вместо декларации сдают электронный журнал учета счетов фактур. Это нужно сделать до 20-го числа месяца, следующего за отчетным кварталом.
Декларация по налогу на прибыль
Сдавать декларацию по налогу на прибыль надо по итогам года, а также в конце каждого отчетного периода. Отчетные периоды зависят от выбранного способа уплаты авансовых платежей. Их можно вносить как за каждый месяц, так и за первый квартал, полугодие, девять месяцев. По итогам года налогоплательщик платит налог на прибыль, уменьшенный на авансы. Если получен убыток, налог платить не нужно.
Кто сдает. Российские и иностранные организации, ответственные участники КГН, налоговые агенты. Организации на спецрежиме сдают декларацию, если налоговый агент не удержал налог с их доходов.
Организации на спецрежиме сдают декларацию, если налоговый агент не удержал налог с их доходов.
Сроки сдачи. Годовую декларацию все сдают в единый срок. Отчитаться по итогам 2020 года нужно до 29 марта 2021 года. Сроки сдачи деклараций за отчетные периоды зависят от порядка уплаты авансовых платежей.
Если вы платите квартальные и ежемесячные авансовые платежи или только квартальные, декларацию надо сдать в следующие сроки:
- за 2020 год — 29 марта 2021 года;
- I квартал — 28 апреля 2021 года;
- полугодие — 28 июля 2021 года;
- 9 месяцев — 28 октября 2021 года.
Если вы платите ежемесячные авансовые платежи по фактической прибыли, отчитываться надо ежемесячно не позднее 28-го числа месяца, следующего за отчетным. Не забывайте, что при выпадении даты сдачи на праздник или выходной она переносится на следующий рабочий день.
Бланк и формат сдачи. Отчитывайтесь по форме, утвержденной приказом ФНС от 11. 09.2020 № ЕД-7-3/655. Сдать декларацию на бумаге могут организации, у которых в 2020 году среднесписочная численность не превысила 100 человек, и вновь созданные организации, уложившиеся в этот лимит по численности работников. Остальные отчитываются в электронной форме.
09.2020 № ЕД-7-3/655. Сдать декларацию на бумаге могут организации, у которых в 2020 году среднесписочная численность не превысила 100 человек, и вновь созданные организации, уложившиеся в этот лимит по численности работников. Остальные отчитываются в электронной форме.
Декларация по налогу на имущество
Кто сдает. Организации, у которых есть недвижимость, облагаемая налогом на имущество. Отчитаться нужно, даже если все имущество подпадает под льготу или его остаточная стоимость равна нулю.
Сроки сдачи. Отчитывайтесь один раз в год. Для декларации за 2020 год срок — не позднее 30 марта 2021 года.
Бланк и формат сдачи. Форма декларации за 2020 год утверждена приказом ФНС от 28.07.2020 № ЕД-7-21/475@. В электронной форме сдать отчет должны крупнейшие налогоплательщики, организации, у которых в 2020 году среднесписочная численность превысила 100 человек, и вновь созданные организации с численностью работников более 100. Остальные могут отчитываться на бумаге.
Остальные могут отчитываться на бумаге.
3-НДФЛ
Кто сдает. ИП на ОСНО, предприниматели, утратившие право на спецрежим, и те, кто получил доход, по которому физлица должны сами платить НДФЛ. А также нотариусы, адвокаты и другие лица, занимающиеся частной практикой.
Сроки сдачи. Сдать декларацию за 2020 год нужно до 30 апреля 2021 года. Если ИП прекратил деятельность до конца года, декларацию надо сдать в течение пяти рабочих дней со дня внесения сведений в ЕГРИП.
Бланк и формат сдачи. Форма декларации за 2020 год утверждена приказом ФНС от 28.08.2020 № ЕД-7-11/615@. Сдать отчет в налоговую можно лично, по почте или через МФЦ. Электронную форму принимают по ТКС и через личный кабинет налогоплательщика. Предприниматели, у которых среднесписочная численность в 2020 году превысила 100 человек, могут отчитываться только электронно.
Упрощенная система налогообложения
УСН — один из спецрежимов, который делает работу бизнеса и жизнь бухгалтера проще. На упрощенке не нужно платить и отчитываться по трем налогам: прибыли, НДС и налогу на имущество. Это приходится делать лишь в исключительных случаях.
На упрощенке не нужно платить и отчитываться по трем налогам: прибыли, НДС и налогу на имущество. Это приходится делать лишь в исключительных случаях.
Все упрощенцы-работодатели должны отчитываться по страховым взносам и доходам сотрудников, а также передавать сведения о них в фонды. Эти отчеты рассмотрим далее.
Специфический отчет для упрощенки — декларация по УСН.
Кто сдает. Организации и предприниматели на упрощенке, даже если не ведут деятельность или взяли налоговые каникулы.
Сроки сдачи. Для организаций и ИП сроки отличаются. Организации отчитываются за 2020 год до 31 марта 2021 года. Предприниматели — до 30 апреля 2021 года.
Бланк и формат сдачи. Форма декларации не менялась давно, она утверждена приказом ФНС России от 26.02.2016 № ММВ-7-3/99@. Отчитаться можно на бумаге и электронно. Для бумажной формы установлено то же ограничение — среднесписочная численность не более 100 человек.
Единый налог на вмененный доход
ЕНВД — удобный спецрежим, на котором сумма налогов не зависит от фактических доходов. С 1 января 2021 года ЕНВД отменят, поэтому сдавать декларацию больше не придется. Но отчет за четвертый квартал 2020 года никто не отменял, а сдать его нужно в 2021 году.
С 1 января 2021 года ЕНВД отменят, поэтому сдавать декларацию больше не придется. Но отчет за четвертый квартал 2020 года никто не отменял, а сдать его нужно в 2021 году.
Кто сдает. Организации и предприниматели, которые работают на ЕНВД.
Сроки сдачи. Отчитываться нужно ежеквартально. Последнюю декларацию по ЕНВД за IV квартал 2020 года нужно будет сдать до 20 января 2021 года. Других отчетов в 2021 году не предполагается.
Бланк и формат сдачи. Сдать отчет можно в бумажном и электронном виде. Форма декларации утверждена приказом ФНС от 26.06.2018 № ММВ-7-3/414@.
Бухгалтерская отчетность
Годовая бухотчетность состоит из баланса, отчета о финансовых результатах и приложений к ним. Если отчетность подлежит обязательному аудиту, то вместе с ней нужно сдать аудиторское заключение. Все организации сдают отчетность в ФНС, а вот в Росстат ее сдавать больше не нужно. Исключение — организации, в отчетности которых есть сведения государственной тайны.
Кто сдает. Организации на любых режимах налогообложения. ИП учет вести не обязаны и могут не сдавать отчетность.
Сроки сдачи. Сдать отчетность нужно в течение трех месяцев после окончания 2020 года, то есть до конца марта. Аудиторское заключение сдавайте либо вместе с отчетностью, либо в течение 10 рабочих дней с даты его составления.
Бланк и формат сдачи. Отчитаться и сдать аудиторское заключение нужно в электронном виде. Формы отчетов мы собрали в статье «Годовая бухгалтерская отчетность организации».
Заявление о подтверждении основного вида деятельности
Основной вид деятельности нужно подтверждать каждый год, направляя соответствующее заявление и документы в ФСС. От него зависит тариф взносов на травматизм. Если не подтвердить вид деятельности, фонд выберет самый опасный вид деятельности из вашего перечня, придется платить взносы по повышенному тарифу.
Кто сдает. Организации-страхователи.
Сроки сдачи. Заявление по итогам 2020 года подайте до 15 апреля 2021 года.
Бланк и формат сдачи. Форма заявления дана в Приложении № 1 к Приказу Минздравсоцразвития от 31.01.2006 № 55. К нему нужно приложить справку-подтверждение из Приложения № 2 и копию пояснительной записки к бухбалансу.
Отчетность по сотрудникам
У бухгалтеров, которые обслуживают организации и предпринимателей на спецрежимах, основную часть работы составляет отчетность по сотрудникам. Одни формы нужно сдавать каждый квартал, другие каждый месяц, а некоторые вообще привязаны к определенным событиям.
НДФЛ
Организации и ИП-работодатели являются налоговыми агентами. Они должны удержать с доходов своих работников НДФЛ и перечислить в бюджет. Об этом предусмотрено два отчета — справка 2-НДФЛ и расчет 6-НДФЛ.
Кто сдает. ИП с сотрудниками и организации.
Сроки сдачи. Справки 2-НДФЛ за 2020 год со всеми «признаками» подайте до 1 марта 2021 года. Расчеты 6-НДФЛ нужно сдавать каждый квартал в следующие сроки:
- за 2020 год — 1 марта 2021;
- за I квартал 2021 года — 30 апреля 2021;
- за полугодие 2021 года — 2 августа 2021;
- за 9 месяцев 2021 года — 1 ноября 2021.
Бланк и формат сдачи. Справку 2-НДФЛ сдавайте по форме, утвержденной приказом ФНС от 02.10.2018 № ММВ-7-11/566@. Ее можно сдать в ИФНС на бумаге или электронно. Бумажная форма разрешена, если вы выплатили доход 10 людям или меньше.
Форма расчета 6-НДФЛ утверждена Приказом ФНС России от 14.10.2015 № ММВ-7-11/450@. Ограничения для сдачи бумажного расчета те же, что для справки 2-НДФЛ.
Расчет по страховым взносам
Кто сдает. Организации и ИП, которые платят страховые взносы с доходов физлиц. Главы КФХ.
Сроки сдачи. Расчеты нужно подать за I квартал, полугодие, 9 месяцев и год. В 2021 году сроки следующие:
- за 2020 год — 1 февраля 2021;
- за I квартал 2021 года — 30 апреля 2021;
- за полугодие 2021 года — 30 июля 2021;
- за 9 месяцев 2021 года — 1 ноября 2021.

Бланк и формат сдачи. Способ сдачи расчета зависит от количества физлиц, которым вы начислили взносы в текущем периоде. Если их численность не превышает 10 человек, расчет можно сдать как на бумаге, так и электронно. Остальным доступен только электронный формат.
Расчет 4-ФСС
Кто сдает. Все страхователи: организации и физлица, которые нанимают работников по трудовым договорам и договорам ГПХ, если в них есть такое условие.
Сроки сдачи. Сроки зависят от формы сдачи расчета: бумажная или электронная. В 2021 году крайние даты следующие:
| Период | Для электронной формы | Для бумажной формы |
|---|---|---|
| 2020 год | 25 января | 20 января |
| I квартал 2021 | 26 апреля | 20 апреля |
| полугодие 2021 | 26 июля | 20 июля |
| 9 месяцев 2021 | 25 октября | 20 октября |
Бланк и формат сдачи.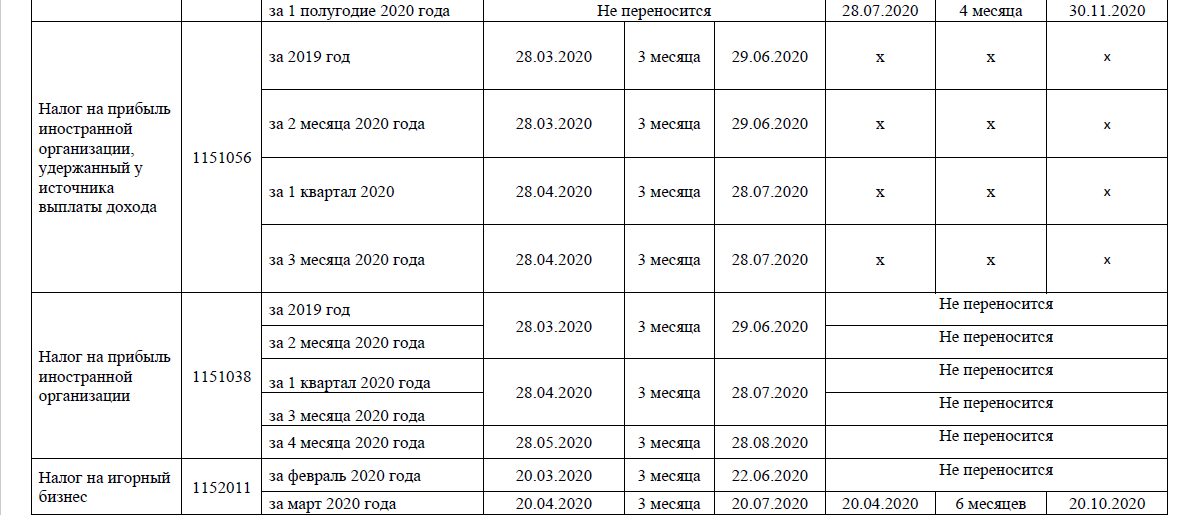 Бланк расчета 4-ФСС утвержден приказом ФСС от 26.09.2016 N 381. Способ сдачи зависит от среднесписочной численности в 2020 году. Если она превысила 25 человек, отчитываться нужно электронно, если нет можно выбрать бумажный формат.
Бланк расчета 4-ФСС утвержден приказом ФСС от 26.09.2016 N 381. Способ сдачи зависит от среднесписочной численности в 2020 году. Если она превысила 25 человек, отчитываться нужно электронно, если нет можно выбрать бумажный формат.
Отчетность в ПФР
Организации и ИП-страхователи регулярно сдают в ПФР отчетность по персучету. В список попадает ежемесячная СЗВ-М, ежеквартальная ДСВ-3 и ежегодная СЗВ-СТАЖ. Еще один отчет — СЗВ-ТД, его сдача привязана к изменению сведений о трудовой деятельности.
Формат сдачи зависит от того, на сколько лиц подаете сведения. Если их 24 и менее, сдать можно как на бумаге, так и электронно. Иначе — только электронно.
СЗВ-М — ежемесячная форма. Ее нужно сдавать каждый месяц не позднее 15-го числа следующего месяца. Помните о переносах сроков сдачи с выходных и праздников. Форма утверждена постановлением Правления ПФР от 01.02.2016 № 83п.
ДСВ-3 — ежеквартально сдают страхователи, которые перечисляют дополнительные страховые взносы на накопительную пенсию. На сдачу дано 20 календарных дней по окончании квартала, выходные и праздники из расчета не исключаются. Форма утверждена постановлением Правления ПФР от 09.06.2016 г. № 482п.
СЗВ-СТАЖ — ежегодная форма. Сдать отчет за 2020 год нужно до 1 марта 2021 года. Форма утверждена постановлением Правления ПФР от 06.12.2018 № 507п.
СЗВ-ТД сдавайте не позднее рабочего дня, следующего за днем оформления документов о приеме или увольнении сотрудника. Также форму надо сдать при переводе на другую работу, подаче заявления о продолжении ведения ТК или о представлении сведений о трудовой деятельности — до 15-го числа месяца, следующего за месяцем с событием. Форма утверждена постановлением Правления ПФР от 25.12.2019 № 730п.
Таким образом, организациям и предпринимателям с сотрудниками нужно помнить гораздо больше сроков, чем фирмам без работников. Чтобы не запутаться в датах и использовать только актуальные формы, пользуйтесь нашим календарем-шпаргалкой.
| Хоть что-то отменили в 2021 году? | ||
| Отчет о среднесписочной численности работников сдавать больше не нужно! Он отменен законом от 28 января 2020 года № 5-ФЗ. Данные о количестве сотрудников будут передаваться в ФНС в составе Расчета по страховым взносам (РСВ), начиная с отчетности за 2020 год | ||
| Декларацию по ЕНВД отменили, потому что отменили ЕНВД 🙁 Последний раз декларацию надо подать за 4-ый квартал 2020 года | ||
| Какие новые формы отчетов в 2021 году? | ||
| Новая форма РСВ, начиная с отчетности за 2020 год – читайте об изменениях | ||
| Изменения в заполнении СЗВ-СТАЖ, начиная с отчетности за 2020 год | ||
| Новая форма НД по прибыли, начиная с отчетности за 2020 год Читайте “Новая форма декларации по налогу на прибыль за 2020 год: изменения и пояснения” | ||
| Новая форма 4-ФСС, начиная с отчетности за 1-й квартал 2021 года | ||
| Новая форма 6-НДФЛ, начиная с отчетности за 1-й квартал 2021 года | ||
| Небольшие изменения в декларации по НДС, начиная с отчетности за 4-й квартал 2020 года | ||
Сплошное стат. наблюдение, новые формы для всего малого и среднего бизнеса и ИП наблюдение, новые формы для всего малого и среднего бизнеса и ИП | ||
| Крайний срок | Какую отчетность сдаем | Кто сдает |
|---|---|---|
| 1 квартал2 квартал3 квартал4 квартал | ||
| 15.01.2021 | СЗВ-М за декабрь 2020 года | Все страхователи |
| СЗВ-ТД за декабрь 2020 года | Все работодатели при наличии оснований | |
| 20.01.2021 | Единая упрощенная налоговая декларация за 2020 год | Юридические лица, у которых отсутствуют объекты налогообложения, а также обороты по банкам и кассе |
| Декларация по водному налогу за 4 квартал 2020 года | Компании, имеющие водные объекты | |
| Декларация по ЕНВД за 4 квартал 2020 года – в последний раз! | Страхователи, выбравшие системой налогообложения ЕНВД | |
| 4-ФСС за 2020 год на бумаге | Все страхователи с численностью сотрудников менее 25 человек | |
25. 01.2021 01.2021 | Декларация по НДС за 4 квартал 2020 года – по обновленной форме! | Плательщики, налоговые агенты, компании которые освобождены от обязанностей налогоплательщика или не являются плательщиками и организации, реализующие товары и услуги освобожденные от налогообложения |
| 4-ФСС за 2020 год в электронном формате | Страхователи с численностью сотрудников более 25 человек | |
| 01.02.2021 | Расчет страховых взносов за 2020 год – по новой форме! | Все страхователи |
| 15.02.2021 | СЗВ-М за январь 2021 года | Все страхователи |
| СЗВ-ТД за январь 2021 года или за 2020 год Читайте СЗВ-ТД 2020-21: новая форма с 01.07.2021, образец заполнения, сроки сдачи, как заполнить отчет в СБИС | Все работодатели при наличии оснований | |
| 01.03.2021 | 2-НДФЛ с признаком “2” при невозможности удержать налог | Налоговые агенты |
| 6-НДФЛ за 2020 год – по старой форме! Читайте Расчет 6-НДФЛ 2021: изменения 2021 года, сроки сдачи, заполнение, штрафы | Налоговые агенты | |
| СЗВ-СТАЖ за 2020 год Читайте СЗВ-СТАЖ: сдача за 2020 год, форма, сроки сдачи, порядок заполнения | Все страхователи | |
| Декларация по налогу на прибыль за февраль 2021 года | Компании, которые отчитываются ежемесячно | |
| Расчет по налогу на прибыль за февраль 2021 года | Налоговые агенты, уплачивающие ежемесячные авансовые платежи по фактически полученной прибыли | |
15. 03.2021 03.2021 | СЗВ-М за февраль 2021 года | Все страхователи |
| СЗВ-ТД за февраль 2021 года | Все работодатели при наличии оснований | |
| 29.03.2021 | Декларации по налогу на прибыль за 2020 год – по новой форме! Читайте “Новая форма декларации по налогу на прибыль за 2020 год: изменения и пояснения” | Организации на ОСНО |
| Декларации по налогу на прибыль за февраль | Организации на ОСНО, подающие отчет каждый месяц | |
| Налоговый расчет по налогу на прибыль за февраль | Налоговые агенты, которые ежемесячно исчисляют авансовые платежи по фактической прибыли | |
| 30.03.2021 | Декларация по налогу на имущество компании за 2020 год Читайте “Новая декларация по налогу на имуществу за 2020 год – “свежие” пояснения ФНС” | Организации, имеющие на балансе имущество |
31. 03.2021 03.2021 | Бухгалтерская отчетность за 2020 год Читайте Бух отчетность – теперь только в электронном виде! | Все организации |
| Декларация по УСН за 2020 год – сдают компании Читайте “Декларация по УСН 2021 – новая форма с 20 марта, все изменения и сроки сдачи” | Организации на УСН | |
| 1 квартал2 квартал3 квартал4 квартал | ||
| 15.04.2021 | СЗВ-М за март 2021 года | Все страхователи |
| СЗВ-ТД за март 2021 года | Все работодатели при наличии оснований | |
| Документы о подтверждении вида деятельности в ФСС за 2020 год Читайте “Подтверждение ОВЭД в ФСС 2021: заявление, справка, сроки сдачи, документы” | Компании, зарегистрированные в 2020 году и ранее | |
| 20.04.2021 | Декларация по водному налогу за 1 квартал 2021 года | Компании, имеющие водные объекты |
Журнал учета полученных и выставленных счетов-фактур за 1 квартал 2021 года в электронном виде | Экспедиторы, посредники и застройщики | |
| Единая упрощенная налоговая декларация за 1 квартал 2021 года | Организации без объектов налогообложения | |
| 4-ФСС за 1 квартал 2021 года на бумаге | Все страхователи с численностью сотрудников менее 25 человек | |
26. 04.2021 04.2021 | Декларация по НДС за 1 квартал 2021 года | Плательщики, налоговые агенты, компании которые освобождены от обязанностей налогоплательщика или не являются плательщиками и организации, реализующие товары и услуги освобожденные от налогообложения |
4-ФСС за 1 квартал 2021 года в электронной форме | Страхователи с численностью сотрудников более 25 человек | |
| 28.04.2021 | Декларация по налогу на прибыль за 1 квартал 2021 года | Компании, которые отчитываются ежеквартально |
| Декларация по налогу на прибыль за март 2021 года | Компании, которые отчитываются ежемесячно | |
| Расчет по налогу на прибыль за март или 1 квартал 2021 года | Налоговые агенты по налогу на прибыль | |
| 30.04.2021 | 6-НДФЛ за 1 квартал 2020 года Читайте 6-НДФЛ 2021: последние новости, сроки сдачи, заполнение, штрафы, новая форма | Налоговые агенты по НДФЛ |
| 3-НДФЛ за 2020 год | ИП | |
| Декларация по УСН за 2020 год – сдают ИП Читайте “Декларация по УСН 2021 – новая форма с 20 марта, все изменения и сроки сдачи“ | ИП на УСН | |
| Расчет по страховым взносам за 1 квартал 2021 года Читайте “РСВ 2021: последние изменения, форма, заполнение” | Все страхователи с численностью сотрудников более 10 | |
17. 05.2021 05.2021 | СЗВ-М за апрель 2021 года | Все страхователи |
| СЗВ-ТД за апрель 2021 года | Все работодатели при наличии оснований | |
| 20.05.2021 | Уведомление о контролируемых сделках за 2020 год | Компании, участвовавшие в контролируемых сделках |
| 28.05.2021 | Декларация по налогу на прибыль за апрель 2021 года | Организации, которые отчитываются ежемесячно |
| Расчет по налогу на прибыль за апрель 2021 года | Налоговые агенты, уплачивающие ежемесячные авансовые платежи по фактически полученной прибыли | |
| 15.06.2021 | СЗВ-М за май 2020 года | Все страхователи |
| СЗВ-ТД за май 2020 года | Все работодатели при наличии оснований | |
| 28.06.2021 | Декларация по налогу на прибыль за май 2021 года | Компании, которые отчитываются ежемесячно |
| Расчет по налогу на прибыль за май 2021 года | Налоговые агенты, уплачивающие ежемесячные авансовые платежи по фактически полученной прибыли | |
| 1 квартал2 квартал3 квартал4 квартал | ||
Налоговая отчетность через интернет для предприятий и индивидуальных предпринимателей – ООО «Партнер и К» – налоговая бухгалтерская отчетность
Налоговая отчетность — это первое, с чем сталкивается
предприниматель после того, как организовал свое собственное дело.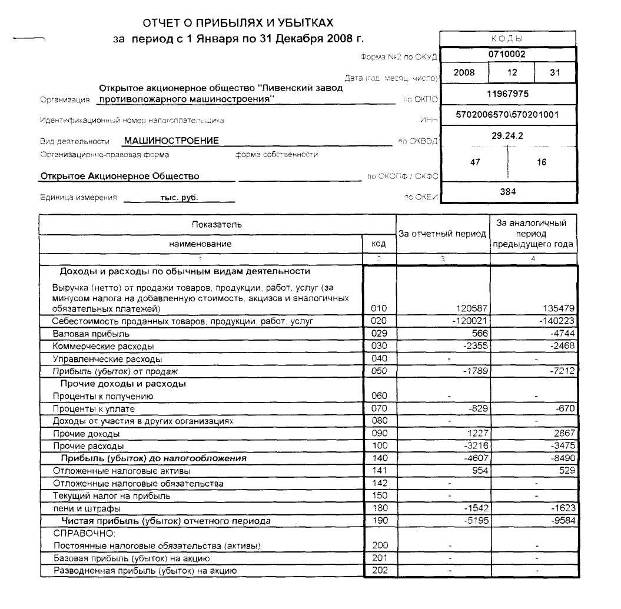 И не важно,
будет это отчет по УСН, по ЕНВД или по НДС. Поэтому грамотно подготовленные
документы помогут Вам не только сохранить, но и приумножить Ваше состояние.
И не важно,
будет это отчет по УСН, по ЕНВД или по НДС. Поэтому грамотно подготовленные
документы помогут Вам не только сохранить, но и приумножить Ваше состояние.
Наша компания «Партнер и К» знает способ сделать так, чтобы налоговая и бухгалтерская отчетность всегда была точной и не причиняла головной боли. Мы предлагаем уникальную услугу, которая сохранит Ваше время и Ваши деньги. А что может быть важнее для бизнесмена?
Сегодня налоговая отчетность, как и многие другие
официальные документы, может быть оформлена непосредственно через
Интернет. Это просто, быстро и более чем удобно. Мы являемся не просто
посредником, который доставит Ваши бумаги в нужное место в нужное время. Наша
компания предоставляет целый комплекс услуг в этой области.
Мы являемся не просто
посредником, который доставит Ваши бумаги в нужное место в нужное время. Наша
компания предоставляет целый комплекс услуг в этой области.
Специальные программы, которые предлагает ООО «Партнер и К», полностью соответствуют всем государственным стандартам и являются официальными способом сдачи налоговой отчетности.
Мы предоставляем Вам уникальную возможность вести учет в режиме онлайн — вне зависимости от размеров Вашего предприятия, начиная от ИП и заканчивая крупным заводом любой формы организации. Электронная отчетность деятельности индивидуального предпринимателя или организации ничем не отличается от бумажного варианта, что делает ее еще более привлекательной формой работы с налоговой службой.
Налоговая отчетность через Интернет
Все больше и больше предпринимателей предпочитают сдавать бухгалтерскую отчетность в налоговую службу через нашу компанию, по причине того, что критерии нашей работы просты и понятны всем нашим клиентам:
- прозрачность;
- оперативность;
- доступность.

Подробнее Вы можете прочесть в разделе «О компании».
Налоговая отчетность через Интернет — это удобно, доступно и быстро. Мы знаем, насколько важно, чтобы не только Ваша компания работала, как часы, но и вся её отчетность полностью соответствовала реальному положению дел. Специалисты ООО «Партнер и К» самым лучшим образом подготовят для Вас все необходимые документы.
Наличие стандартных форм заполнения, а также полное соответствие законодательству Российской Федерации гарантируют качество нашей работы, а следовательно, и сохранность Ваших доходов.
Грамотный налоговый учет и отчетность — это гарантия успешного и стабильного развития Вашего бизнеса, не забывайте об этом — и фортуна никогда не отвернется от Вас!
Если есть вопросы, пожалуйста, обращайтесь к он-лайн консультанту на сайте.
Или позвоните нам по телефонам: (861) 373−11−01, (918) 633−23−42, (964) 901−10−73, (928) 405−14−51
Корректировка бухгалтерской отчетности после сдачи в налоговую в 2021 году
Корректировка бухгалтерской отчетности за прошлый период — это исправление ошибки в балансе или приложениях к нему после сдачи в ИФНС или уполномоченные органы. Для разных ситуаций алгоритм отличается.
Для разных ситуаций алгоритм отличается.
Правила и сроки утверждения финансовых отчетов
В соответствии с законом №402-ФЗ, бухотчетность подписывается главным бухгалтером и руководителем компании. Также свою подпись ставит руководитель экономической службы, если в отчетах присутствуют аналогичные сведения. Затем отчеты утверждаются владельцами (собственниками, учредителями, акционерами) фирмы.
Напомним, что обычный срок сдачи финотчетов в ФНС — до 31 марта года, следующего за отчетным. Аналогичный срок установлен и для иных контролирующих госорганов, например, Минюста. Для утверждения финотчетов установлены иные даты. Так, например, учредители ООО должны провести утверждение в марте или апреле года, следующего за отчетным. А вот собственники акционерных обществ вправе провести данную процедуру еще позже — с марта по июнь включительно.
Следовательно, в большинстве случаев в ФНС предоставляются сведения, которые еще не прошли процедуру утверждения, регламентированную в законе №402-ФЗ. Таким образом, становится закономерным вопрос, можно ли сдать корректирующую бухгалтерскую отчетность за 2020 год, если обнаружена существенная погрешность в учете, — это зависит от того, утвержден баланс и остальные формы или еще нет. После того как бухотчетность утверждена владельцами компании, вносить исправления нельзя. Разрешается сдать заново только бухгалтерскую отчетность, которая еще не прошла утверждение.
Степень существенности ошибок
Все ситуации, когда вносятся исправления, касаются только существенных ошибкок. Если бухгалтер нашел незначительную помарку или неточность, то, независимо от срока выявления, исправительные записи вносятся текущим периодом. То есть отчетный прошлый период не затрагивается и новые исправительные финотчеты не составляются.
Следовательно, можно ли подать корректировку годовой бухгалтерской отчетности при незначительной помарке? Нет, нельзя. Исправления вносятся только по существенным ошибкам.
В ПБУ 22/2010 сказано, что существенной признается ошибка, которая в отдельности или в совокупности с другими ошибками за один и тот же отчетный период может повлиять на экономические решения пользователей, принимаемые ими на основе бухгалтерской отчетности, составленной за этот отчетный период. Существенность ошибки определяется организацией самостоятельно с учетом ее величины и характера соответствующей статьи (статей) бухгалтерской отчетности.
Порядок определения существенности закрепляют в учетной политике:
«Ошибка признается существенной, если ее значение искажает показатель любой строки отчета более, чем на 10%».
Чтобы внести корректировку в учетные данные, применяется ретроспективный метод пересчета. Иными словами, все показатели финотчетов подлежат пересчету с условием, как если бы выявленная ошибка никогда бы не совершалась. Субъекты, ведущие упрощенный бухучет, вправе не применять ретроспективный метод пересчета.
Корректировка после сдачи отчета
Порядок внесения изменений в уже сданный годовой финансовый отчет регламентирован на законодательном уровне, в принципе, как и правила составления бухотчетности. Приказ Минфина от 28.06.2010 №63н, или ПБУ 22/2010 устанавливает ключевые правила корректировки бухотчетности после отчетной даты.
Алгоритм действия зависит от даты выявления ошибки, от степени ее существенности, значительности и от того, была утверждена финотчетность владельцами компании или нет. Отметим, что корректировка бухгалтерской отчетности проводится по аналогии.
Для одной ситуации корректировка невозможна, а для другой проводится в обязательном порядке. Разберемся, какие действия предпринять бухгалтеру в каждом случае и нужно ли сдавать уточненный баланс за прошлые периоды, если отчетные данные изменились, но отчетность уже утверждена. В этом случае бухгалтер вносит корректирующие записи уже в текущем периоде, не изменяя данные отчетного года и не сдавая уточненный баланс с приложениями. Проводка составляется с использованием счета 84 «Нераспределенная прибыль или непокрытый убыток» в корреспонденции со счетом, по которому была обнаружена существенная неточность. Для примера возьмем ситуацию, когда неправильно начислена амортизация. Проводка выглядит так:
Дата выявления ошибки
Мы определились, что направлять измененный отчет в ФНС после его утверждения не нужно. Теперь рассмотрим порядок исправления ошибок в бухгалтерской отчетности «до утверждения». В этом случае сдать уточненный баланс, форму 2 и другие отчеты необходимо. Если отчетная форма еще не утверждена, то коррективы в учет внести обязательно. Но изменения следует вносить с учетом даты обнаружения ошибки. Законодатели в ПБУ 22/2010 предусмотрели несколько ситуаций. Рассмотрим каждую из них.
Ситуация №1. Нашли ошибку до или во время составления финотчетности
В таком случае бухгалтер вносит корректирующие записи в отчетном периоде. Иными словами, если ошибка найдена в момент составления бухгалтерской отчетности, то неверная запись (операция, проводка) исправляется. Следовательно, в отчет войдут корректные данные, и корректировка бухгалтерской отчетности после сдачи в налоговую не потребуется.
Ситуация №2. Неточность выявлена до сдачи финансовой отчетности в ФНС
Годовой отчет составлен, но еще не отправлен на проверку в госорганы и не передан на утверждение владельцам. Если ошибка выявлена в этот период, то для нормализации бухгалтерской отчетности необходима корректировка. Бухгалтер обязан исправить неточность и переформировать бухбаланс. Причем исправительные проводки вносятся последним месяцем отчетного периода (декабрь). Неправильная версия отчета подлежит замене на достоверный экземпляр.
Ситуация № 3. Корректировка бухгалтерской отчетности после направления в ИФНС
Отчет сформирован и отправлен в ФНС. На заседании учредителей компании выявлена существенная неточность, и отчет возвращен в бухгалтерию на доработку. Бухгалтер исправляет найденную ошибку, исправления в бухучете регистрирует декабрем. Затем формирует финотчет повторно, но уже с изменениями и предоставляет его учредителям на рассмотрение. В этом случае не возникает вопроса, можно ли пересдать бухгалтерскую отчетность за 2020 год — это сделать необходимо. Бланки отчетных документов используются те же, только проставляется номер корректировки. Например, для подачи первого корректирующего отчета проставляют «001» или «—1».
Как сдать «уточненку»
Порядок внесения изменений и предоставления исправляющей финотчетности зависит от конечного получателя, то есть от того, кому адресован исправленный экземпляр отчета.
Если отчитываемся в ФНС, то действуйте в соответствии с установленными алгоритмами заполнения отчетных форм. Иными словами, при подготовке корректирующего финотчета используйте тот же бланк и те же правила заполнения, что и при первичной отправке информации в ФНС.
О том, какие формы бухотчетов необходимо составлять в обязательном порядке, читайте в отдельной статье «Формы бухгалтерской отчетности».
Если сдана некорректная бухгалтерская отчетность, сопроводите ее пояснительной запиской. В документе раскройте следующую информацию:
- характер выявленной ошибки;
- сумму отклонений в денежном выражении, а при необходимости и в количественном выражении;
- способ исправления.
Информацию раскройте по каждой статье бухучета, в которой были выявлены значительные неточности. Такую пояснительную записку направляют в ФНС вместе с корректировками.
Правовые документы
Аутоантител против интерферонов I типа у пациентов с опасным для жизни COVID-19
Аутоантитела к IFN типа I у пациентов с опасным для жизни COVID-19
Автор: Пол Бастард, Линдси Б. Розен, Цянь Чжан, Элефтериос Михайлидис, Ханс-Генрих Хоффманн, Ю Чжан, Карим Доргам, Квентин Филиппот, Джереми Розаин, Вивьен Безиат, Джереми Лори, Элана Шав, Лийз Хальясмэро, Лийз Хальясмаро , Люси Бизьен, Софи Труйе-Ассан, Керри Доббс, Адриана Алмейда де Хесус, Александр Бело, Энн Калласте, Эмили Катерино, Ясин Танджауи-Ламбьотт, Джереми Ле Пен, Гаспар Кернер, Бенедетта Биджо, Йоанн Зелеангнер, Йоанри Йоанн Зелеангнер Андраш Н.Спаан, Оттавия М. Делмонте, Майкл С. Аберс, Алессандро Айути, Джорджио Касари, Вито Лампасона, Лоренцо Пьемонти, Фабио Чичери, Кая Бильгувар, Ричард П. Лифтон, Марк Вассе, Давид М. Смаджа, Мелани Мигамин, Жером Хаджадж, Бенедикт Терьер, Дарраг Даффи, Луис Кинтана-Мурси, Дидерик ван де Бик, Люси Руссель, Дональд Винь, Стюарт Г. Танжье, Филомин Херинк, Дэвид Далмау, Хавьер Мартинес-Пикадо, Петтер Броден, Мишель К. Нуссенцвейг, Стефани Бодени Дюпюи, Карлос Родригес-Гальего, Гийом Фогт, Трине Х.Могенсен, Эндрю Дж. Олер, Джингвен Гу, Питер Д. Бурбело, Джеффри И. Коэн, Андреа Бионди, Лаура Рэйчел Беттини, Мариэлла Д’Анджио, Паоло Бонфанти, Патрик Россиньоль, Жюльен Майо, Фредерик Риё-Локат, Эйстейн С. Хусебай , Франческа Фуско, Матильда Валерия Урсини, Луиза Имберти, Алессандра Соттини, Симоне Пагера, Юджиния Кирос-Ролдан, Камилло Росси, Риккардо Кастаньоли, Даниэла Монтанья, Амелия Ликари, Джан Луиджи Марселья, Ксавье Дюваль, Джейд-Галиа Группа иммунного ответа на COVID, клиницисты COVID, клиницисты COVID-STORM, Imagine COVID Group, французская группа когортных исследований COVID, The Milieu Intérieur Consortium, CoV-Contact Cohort, Amsterdam UMC Covid-19 Biobank, COVID Human Genetic Effort, John S.Цанг, Рафаэла Гольдбах-Мански, Кай Кисанд, Михаил С. Лионакис, Энн Пуэль, Шен-Ин Чжан, Стивен М. Холланд, Гай Горохов, Эммануэль Жуанги, Чарльз М. Райс, Орели Кобат, Луиджи Д. Нотаранджело, Лоран Абель, Хелен С. Су, Жан-Лоран Казанова
Наука
Аутоантител к IFN типа I у пациентов с опасным для жизни COVID-19
Аутоантитела к IFNs типа I у пациентов с опасным для жизни COVID-19
Пол Бастард, Линдси Б.Розен, Цянь Чжан, Элефтериос Михайлидис, Ханс-Генрих Хоффманн, Ю Чжан, Карим Доргам, Квентин Филиппо, Жереми Розен, Вивьен Безиа, Джереми Манри, Элана Шоу, Лийс Хальясмяги, Пярт Петерсон, Лазаро Лоренцо, Люси Бизьен, Софи Труйе-Ассан, Керри Доббс, Адриана Алмейда де Хесус, Александр Бело, Энн Калласте, Эмили Катерино, Ясин Танджауи-Ламбьотт, Жереми Ле Пен, Гаспар Кернер, Бенедетта Бигио, Йоанн Зелеутнер, Руи Ян, Александр Больце, Андраш Н.Спаан, Оттавия М. Делмонте, Майкл С. Аберс, Алессандро Айути, Джорджио Касари, Вито Лампасона, Лоренцо Пьемонти, Фабио Чичери, Кая Бильгувар, Ричард П. Лифтон, Марк Вассе, Дэвид М. Смаджа, Мелани Миго, Жером Хаджадж, Бенджамин Терьер, Дарра Даффи, Луис Кинтана-Мурси, Дидерик ван де Бик, Люси Руссель, Дональд Винь, Стюарт Дж. Танье, Филомин Хэринк, Дэвид Далмау, Хавьер Мартинес-Пикадо, Петтер Броден, Мишель К. Нуссенцвейг, Стефани Буассон-Дюпюи, Карлос Родригес-Гальего, Гийом Фогт, Трина Х.Могенсен, Эндрю Дж. Олер, Джингвен Гу, Питер Д. Бурбело, Джеффри Коэн, Андреа Бионди, Лаура Рэйчел Беттини, Мариэлла Д’Анджио, Паоло Бонфанти, Патрик Россиньоль, Жюльен Майо, Фредерик Рье-Локат, Эйстейн С. Хусебай, Франческа Фуско, Матильда Валерия Урсини, Луиза Имберти, Алессандра Соттини, Симоне Пагера, Эухения Кирос-Ролдан, Камилло Росси, Риккардо Кастаньоли, Даниэла Монтанья, Амелия Ликари, Джан Луиджи Марселья, Ксавье Дюваль, Джейд Гон, HGID Lab, NIAID-USUHS Immune Ответ на COVID Group, COVID клиницисты, COVID-STORM клиницисты, Imagine COVID Группа, Французская группа исследования COVID, Консорциум внутренней среды, CoV-Contact Cohort, Амстердамский биобанк UMC Covid-19, COVID Human Genetic Effort, John S.Цанг, Рафаэла Гольдбах-Мански, Кай Кисанд, Михаил С. Лионакис, Энн Пуэль, Шен-Ин Чжан, Стивен М. Холланд, Гай Горохов, Эммануэль Жуанги, Чарльз М. Райс, Орели Кобат, Луиджи Д. Нотаранджело, Лоран Абель, Хелен С. Су, Жан-Лоран Казанова
Аутоантитела к IFN типа I у пациентов с опасным для жизни COVID-19
Аутоантитела к IFN типа I у пациентов с опасным для жизни COVID-19
Пол Бастард, Линдси Б.Розен, Цянь Чжан, Элефтериос Михайлидис, Ханс-Генрих Хоффманн, Ю Чжан, Карим Доргам, Квентин Филипбот, Джереми Розайн, Вивьен Безиат, Джереми Манри, Элана Шоу, Лийс Хальясмэги, Пярт Петерсон, Софи Ласаро Ласаро Ласаро Ласаро Ласаро Ласаро Ласаро Ласаро , Керри Доббс, Адриана Алмейда де Хесус, Александр Бело, Энн Калласте, Эмили Катерино, Ясин Танджауи-Ламбьотт, Джереми Ле Пен, Гаспар Кернер, Бенедетта Биджо, Йоанн Зелеутнер, Руи Ян, Александр Больце, Орас Н. Спаан Дельмонте, Майкл С.Аберс, Алессандро Айути, Джорджио Касари, Вито Лампасона, Лоренцо Пьемонти, Фабио Чичери, Кая Бильгувар, Ричард П. Лифтон, Марк Вассе, Дэвид М. Смаджа, Мелани Миго, Жером Хаджадж, Бенджамин Терьер, Дарраги Даффинти, Ллухам Дидерик ван де Бик, Люси Руссель, Дональд Винь, Стюарт Г. Танье, Филомин Хэринк, Дэвид Далмау, Хавьер Мартинес-Пикадо, Петтер Броден, Мишель К. Нуссенцвейг, Стефани Буассон-Дюпюи, Карлос Родригес-Гальмелего, Карлос Родригес-Гальмелего, Трина Х. Могенсен, Эндрю Дж.Олер, Джингвен Гу, Питер Д. Бурбело, Джеффри И. Коэн, Андреа Бионди, Лаура Рэйчел Беттини, Мариэлла Д’Анджио, Паоло Бонфанти, Патрик Россиньоль, Жюльен Майо, Фредерик Риё-Локат, Эйстейн С. Хусебай, Франческа Фуско, Матильдэуско Валерия Урсини, Луиза Имберти, Алессандра Соттини, Симоне Пагера, Юджиния Кирос-Ролдан, Камилло Росси, Риккардо Кастаньоли, Даниэла Монтанья, Амелия Ликари, Джан Луиджи Марселья, Ксавье Дюваль, Джейд Госн, HGID Labse, NIAID-Group Immune , COVID-клиницисты, COVID-STORM-клиницисты, Imagine COVID Group, Французская группа когортных исследований COVID, The Milieu Intérieur Consortium, CoV-Contact Cohort, Amsterdam UMC Covid-19 Biobank, COVID Human Genetic Effort, John S.Цанг, Рафаэла Гольдбах-Мански, Кай Кисанд, Михаил С. Лионакис, Энн Пуэль, Шен-Ин Чжан, Стивен М. Холланд, Гай Горохов, Эммануэль Жуанги, Чарльз М. Райс, Орели Кобат, Луиджи Д. Нотаранджело, Лоран Абель, Хелен С. Су, Жан-Лоран Казанова
Наука
Интерфероны: успех в противовирусной иммунотерапии
Abstract
Интерфероны (IFN) — это гликопротеины с сильной противовирусной активностью, которые представляют собой одну из первых линий защиты организма от вторжения патогенов.Эти белки классифицируются на три группы, IFN типа I, II и III, в зависимости от структуры их рецепторов на поверхности клетки. Благодаря своей способности модулировать иммунные реакции, они стали привлекательными терапевтическими вариантами для борьбы с хроническими вирусными инфекциями. В сочетании с другими лекарственными препаратами ИФН типа I считаются «стандартом лечения» при подавлении инфекций гепатита С (ВГС) и гепатита В (ВГВ), в то время как ИФН типа III дает обнадеживающие результаты в качестве лечения инфекции ВГС в клинической фазе III. испытания.Однако, несмотря на их эффективность, использование интерферонов в качестве лечения не лишено осторожности. IFN — это такие мощные цитокины, которые влияют на широкий спектр типов клеток; в результате пациенты обычно испытывают неприятные симптомы, при этом у некоторого процента пациентов отмечаются общесистемные эффекты. Таким образом, за пациентами, получающими ИФН, требуется постоянный мониторинг для достижения целей лечения по подавлению вирусной инфекции и поддержанию качества жизни.
Ключевые слова: Противовирусная терапия, IFN-α / β, IFN-γ, IFN-λ
1.Введение
Интерфероны (IFN) были впервые описаны в 1957 г. как гетерогенный класс растворимых гликопротеинов с сильной противовирусной активностью. Индукция их экспрессии происходит в ответ на вирусную или бактериальную инфекцию. IFN подразделяются на три типа IFN: I, II и III типы, в зависимости от структуры их рецепторов на поверхности клеточной мембраны. Благодаря их способности модулировать иммунные ответы, они были рассмотрены в качестве варианта лечения нескольких видов рака и аутоиммунных заболеваний ().С развитием рекомбинантных IFN, IFN становятся еще более привлекательными терапевтическими вариантами, поскольку их предложение больше не ограничено. Вследствие клинических неудач в борьбе с хронической вирусной инфекцией с использованием только противовирусных препаратов из-за образования штаммов, устойчивых к лекарственным средствам, варианты лечения, такие как IFNs, которые нацелены на иммунный ответ хозяина, а не на специфические вирусные белки, становятся важным компонентом схемы лечения . Действительно, в последние годы ИФН типа I стали частью стандартного лечения инфекций ВГС и ВГВ, и появления устойчивых к ИФН вирусных субпопуляций не наблюдалось.Кроме того, растет интерес к тестированию противовирусной эффективности нового члена IFN, IFN типа III, при инфекции HCV на основании того факта, что рецептор IFN типа III более ограничен в своей экспрессии и присутствует в гепатоцитах. В этом обзоре мы обсудим биологию и противовирусную активность IFN, а также их использование в противовирусной терапии заболеваний человека.
Таблица 1
Текущие одобренные FDA терапевтические агенты IFN
| Торговая марка | Общее название | Производители | Описания |
|---|---|---|---|
| IFN типа I | |||
| Alferon N | IFN- αn3 | Hemispherx | Одобрено для лечения генитальных и перианальных бородавок, вызванных вирусом папилломы человека (ВПЧ) |
| Infergen | IFN-αcon1 | Intermune Pharms | Одобрено для лечения HCV |
| Pegasys | Peg-IFN-α2a | Roche | Одобрено для лечения взрослых пациентов с HBV отрицательным, пациентов с HCV в возрасте 5 лет и старше, ранее не получавших IFN-α, и пациентов с коинфекцией HCV / HIV. |
| Справка A | IFN-α2a | Roche | Одобрено для лечения волосатоклеточного лейкоза, связанной со СПИДом саркомы Капоши и хронического миелогенного лейкоза. |
| Интрон A | IFN-α2b | Schering | Одобрен для лечения пациентов с HBV в возрасте 1 год и старше и пациентов с HCV 18 лет и старше |
| PegIntron / Sylaton | Peg-IFN -α2b | Schering | Одобрено для лечения пациентов с гепатитом С 18 лет и старше, ранее не получавших IFN-α |
| Rebif | IFN-β1a | Merk Serono | Одобрено для лечения рассеянного склероза |
| Avonex | IFN-β1a | Biogen Idec | Одобрено для лечения рассеянного склероза |
| Betaseron | IFN-β1b | Bayer | Одобрено для лечения рассеянного склероза |
| Extavia | IFN-β1b | Novartis | Одобрено для лечения рассеянного склероза |
| 90 176 | |||
| IFN типа II | |||
| Actimmune | IFN-γ1b | Vidara Therapeutics | Одобрено для лечения хронической гранулематозной болезни и тяжелого злокачественного остеопетроза |
2.Интерфероны I типа: интерферон-альфа / бета (IFN-α / β)
2.1. ИНТЕРФЕРОНЫ ТИПА I СИГНАЛЬНЫЙ ПУТЬ
IFN типа I относятся к семейству α-спиральных цитокинов класса II, включая IFN-γ, IFN-λ (IFN типа III), IL-10 и несколько гомологов IL-10 (IL- 19, ИЛ-20, ИЛ-22, ИЛ-24 и ИЛ-26). IFN типа I могут продуцироваться всеми ядросодержащими клетками в ответ на вирусные или микробные инфекции. У человека семейство IFN типа I состоит из 12 подтипов IFN-α, кодируемых 14 генами, IFN-β, кодируемого одним геном IFNB , и IFN-ε, IFN-κ и IFN-ω [1].В этом обзоре мы сосредоточимся на двух хорошо охарактеризованных ИФН типа I, ИФН-α и ИФН-β. Все IFN типа I передают сигнал путем связывания с одним и тем же гетеродимерным рецептором IFNα / β рецептором (IFNAR). IFNAR экспрессируется почти всеми типами клеток и состоит из субъединиц IFNAR1 и IFNAR2, которые связаны с тирозинкиназой 2 (TYK2) и янус-киназой 1 (JAK1) соответственно. Связывание с IFNAR приводит к активации TYK2 и JAK1, которые фосфорилируют остатки тирозина в цитоплазматических доменах IFNAR, создавая, таким образом, стыковочные сайты для сигнальных преобразователей и активаторов транскрипции (STAT) (STAT1, STAT2 и STAT3 в большинстве типов клеток), которые являются затем направляется JAK для фосфорилирования.Фосфорилированные STAT (pSTAT) образуют гомодимеры или гетеродимеры и перемещаются в ядро. Гомодимер pSTAT1 связывается с гамма-активированной последовательностью (GAS, TTCNNNGAA) в промоторной области генов, стимулированных интерфероном (ISG), и инициирует транскрипцию этих генов-мишеней, в то время как гомодимер, образованный pSTAT3, активирует транскрипцию генов, содержащих энхансерную последовательность STAT3. -обвязочный элемент. Фосфорилированные STAT1 и STAT2 образуют гетеродимер, который приводит к рекрутированию IRF9 и образованию комплекса генного фактора 3, стимулированного IFN (ISGF3).Этот комплекс затем переносится в ядро и связывается с IFN-стимулированными ответными элементами (ISRE) в промоторной области IFN-чувствительных генов (ISG), чтобы инициировать транскрипцию генов, которые имеют решающее значение для противовирусной активности типа I () [2, 3]. В дополнение к STAT1, STAT2 и STAT3 было показано, что IFN типа I может также активировать STAT4, STAT5 и STAT6 в определенных типах ячеек [4]. Активация JAK также может индуцировать несколько альтернативных путей передачи сигналов, включая пути PI3K, NF-kB и MAPK, которые дополнительно усиливают силу и величину передачи сигналов IFN I типа.
Канонические сигнальные пути интерферонаIFN типа I, II и III связываются со своими специфическими рецепторами на клеточной мембране и запускают сигнальный путь JAK-STAT. В то время как типы I и III могут фосфорилировать как STAT1, так и STAT2 с образованием ISGF3 и GAF, которые связываются с ISRE и GAS соответственно в промоторной области отвечающих генов, IFN типа II может фосфорилировать только STAT1 и индуцировать экспрессию генов с GAS в промоторной области.
2.2. АНТИВИРУСНАЯ АКТИВНОСТЬ
IFN типа I индуцирует ряд белков, которые препятствуют репликации вируса, чтобы ограничить и ограничить распространение вируса от клетки к клетке [5, 6].2’ – 5’-олигоаденилатсинтетаза (OAS) — это фермент, индуцируемый IFN типа I, который активирует латентную нуклеазу RNaseL, которая затем опосредует деградацию вирусной РНК. Другой индуцированный фермент, РНК-активированная протеинкиназа (PKR), член семейства эукариотических факторов инициации 2α, предотвращает рециклинг гуанидиндифосфата, который, в свою очередь, блокирует трансляцию вирусной РНК. Другими заметными противовирусными белками, индуцируемыми IFN типа I, являются GTPазы устойчивости к миксовирусу (Mx), которые ограничивают локализацию вирусного нуклеокапсида, стимулированный интерфероном ген 15 (ISG15) и белок трехчастичного мотива (TRIM), которые препятствуют высвобождению вирусных частиц, а также APOBEC3, белок, который вызывает гипермутацию вирусной ДНК.Чтобы ограничить и локализовать инфекцию, IFN типа I также могут активировать механизм апоптоза для уничтожения инфицированных вирусом клеток путем активации лиганда Fas (FasL), PDL-1 и TRAIL. Помимо активации противовирусного механизма в инфицированных клетках, IFN типа I также может ограничивать вирусную инфекцию, модулируя как врожденный, так и адаптивный иммунитет. IFN типа I непосредственно активируют NK-клетки, чтобы усилить их цитотоксичность, устранить инфицированные клетки и ограничить инфекцию. Однако полное устранение внутриклеточной инфекции патогенами требует активации адаптивного иммунного ответа, и IFN типа I играют активную роль в этом процессе активации.IFN типа I способствуют созреванию дендритных клеток (DC), которые способствуют дифференцировке CD4 + Т-клеток в клетки Th2 или Th3 [5, 6]. Исследования показали, что опытные APC IFN типа I способны к перекрестной презентации и стимулировать наивные CD8 + Т-клетки, что приводит к клональной экспансии и пролиферации. Эти опытные ДК IFN типа I обладают повышенной экспрессией хемокинов, которые привлекают NK, T и B-клетки к месту инфекции, и IL-15, который важен для поддержания клеток памяти NK и CD8 + .Все эти внутренние и внешние эффекты IFN типа I подготавливают иммунную систему хозяина к выработке эффективного ответа против внутриклеточных патогенов.
2.3. IFN-α КАК ТЕРАПЕВТИЧЕСКИЙ АГЕНТ ПРИ ВГС-ИНФЕКЦИЯХ
Хроническая инфекция ВГС является серьезной проблемой для здоровья, и во всем мире инфицировано около 180 миллионов человек. В то время как более 80% хронической инфекции ВГС протекает бессимптомно, у 5–30% инфицированных пациентов развивается цирроз и иногда развивается тяжелое заболевание печени, включая кровотечение из варикозно расширенных вен и гепатоцеллюлярную карциному (ГЦК).В настоящее время существует несколько препаратов, направленных на репликацию вируса, которые были одобрены FDA для клинического использования. Однако из-за высокой распространенности штаммов ВГС с лекарственной устойчивостью, последствий беспорядочной РНК-полимеразы, лечение только противовирусными препаратами было менее эффективным, хотя новые противовирусные препараты выглядят более многообещающими [7]. Обладая обширной противовирусной активностью, рекомбинантный IFN-α был впервые использован для лечения HCV в 1986 году. Однако из-за быстрой абсорбции, короткого периода полувыведения и быстрого выведения почками результат был менее желательным, даже с добавлением аналог нуклеозидов рибавирин.Чтобы обеспечить более медленное всасывание и поддержание устойчивого и стабильного уровня в крови, пегилированный IFN, синтезируемый путем присоединения фрагмента полиэтиленгликоля (PEG), был введен в клинику в 2001 году [8, 9]. Это изменение было менее травматичным для пациентов, поскольку потребовалось только еженедельное введение IFN типа I вместо инъекции три раза в неделю. В настоящее время общепринятым стандартным лечением хронической инфекции HCV является еженедельная подкожная инъекция пегилированного IFN-α (PEG-IFN-α) с ежедневным пероральным приемом рибавирина.Целью лечения является достижение устойчивого вирусологического ответа (УВО) с неопределяемой РНК ВГС к концу периода лечения. Лечение PEG-IFN-α / рибавирином при инфекции HCV дает очень желаемые результаты. Примерно 80% пациентов достигают УВО в конце периода лечения. В настоящее время для лечения ВГС доступны два PEG-IFN-α, доступных для клинического использования, IFN-α2a и IFN-α2b. Хотя подтип IFN-α2 имеет более низкое сродство связывания со своим рецептором, что связано с более низкой антипролиферативной активностью, нет никакой разницы в противовирусном эффекте по сравнению с другими подтипами [10].Однако сравнение эффективности IFN-α2a и IFN-α2b в терапии HCV дало противоречивые результаты, которые можно объяснить разными режимами дозирования (т.е. фиксированными для PEG-IFN-α2a и основанными на массе для PEG-IFN-α2b). и немного другая дозировка рибавирина. Более того, история лечения субъектов ВГС может повлиять на интерпретацию результатов в этих испытаниях, поскольку многие пациенты с ВГС коинфицированы другими патогенами, включая ВИЧ, и эти сочетанные инфекции могут повлиять на результат лечения [11].
Несмотря на успех, лечение IFN часто сопровождается нежелательными системными побочными эффектами, поскольку практически все типы клеток экспрессируют IFNAR. Общие побочные эффекты, вызываемые IFN-α, включая усталость, головную боль, гипертермию, миалгию, озноб и психиатрические симптомы. Анемия, одна из распространенных гематологических аномалий, наблюдаемых во время лечения, в основном вызывается рибавирином, в то время как нейтропения и тромбоцитопения являются результатом лечения IFN-α [12]. В зависимости от тяжести симптомов может потребоваться снижение дозы или прекращение лечения.Из-за потенциальных системных побочных эффектов другие молекулы IFN, в том числе альбумин-IFN-α, IFN-λ (подробно обсуждается далее в этом обзоре) и консенсусный IFN-α, изучаются как потенциальные кандидаты на замену PEG-IFN. -α. Альбумин IFN-α2b является продуктом слияния гена с генами IFN-α и сывороточного альбумина человека. Это молекула массой 85,7 кДа, которая сохраняет противовирусные свойства IFN-α с 6-дневным периодом полувыведения, который в 2–4 раза больше, чем PEG-IFN-α [13]. Длительный период полувыведения альбумина IFN-α позволяет использовать 2-недельный или даже 4-недельный режим дозирования, который может ограничить частоту побочных эффектов, связанных с IFN-α.Хотя исследование фазы I / II показало многообещающие результаты, результаты исследования фазы III вызвали опасения относительно безопасности альбумина IFN-α из-за увеличения частоты не только общих побочных эффектов, связанных с IFN-α, но и легочных осложнений по сравнению с группы лечения PEG-IFN-α2a. Как следствие, заявка на одобрение FDA была отклонена [14, 15].
Консенсусный IFN (CIFN) представляет собой рекомбинантный белок консенсусного гена, который состоит из наиболее часто встречающихся аминокислот из нескольких подтипов IFN типа I.Было показано, что CIFN имеет в 10–100 раз более высокую противовирусную активность по сравнению со стандартным IFN-α, что позволяет использовать более низкий режим дозирования и потенциально ограничивает частоту побочных эффектов типа IFN-α. Однако, наряду с более сильной противовирусной активностью, CIFN по-прежнему имеет недостатки рекомбинантного IFN-α, то есть быстрое всасывание, короткий период полувыведения и быстрое выведение почками. Таким образом, пациентам требуется ежедневная инъекция для поддержания УВО. Раннее исследование III фазы, предназначенное для оценки эффективности CIFN, показало, что монотерапия CIFN дает более высокий уровень УВО по сравнению с лечением IFN-α2b.Кроме того, в клинических испытаниях было показано, что схема лечения, сочетающая CIFN с рибавирином, эффективна при лечении пациентов, не отвечающих на PEG-IFN-α / рибавирин [16]. Основываясь на этих многообещающих результатах клинических испытаний фазы III, лечение CIFN в настоящее время одобрено в США [11, 17].
Комбинация ПЕГ-ИФН / рибавирин была стандартом лечения инфекции ВГС в течение последнего десятилетия. Однако успех лечения ограничен неоптимальными показателями УВО у резистентных к лечению пациентов, плохой переносимостью и обременительным режимом лечения.Были предприняты огромные усилия по оптимизации схемы лечения ВГС в надежде преодолеть ограничения лечения ПЕГ-ИФН / рибавирином. Полученные к настоящему времени обширные знания о жизненном цикле ВГС стимулировали разработку противовирусных агентов прямого действия (DAA), которые нацелены на вирусные белки, чтобы препятствовать их репликации. Существует четыре основные группы DAA, ингибиторы протеазы NS3 / 4A (ИП), ингибиторы нуклеозидной полимеразы NS5B (NPI), ненуклеозидные ингибиторы полимеразы NS5B (NNPI) и ингибиторы NS5A.В 2011 году два ИП, телапревир и боцепревир были одобрены FDA, и при использовании в сочетании с лечением ПЭГ-ИФН / рибавирин значительно повысили частоту УВО у пролеченных пациентов. В настоящее время проходят клинические испытания несколько многообещающих ПППД для изучения их эффективности в качестве монотерапии или в сочетании с рибавирином или ПЭГ-ИФН / рибавирином. Хотя некоторые из них показали гепатотоксичность, большинство протестированных ПППД хорошо переносились и проявляли сильную противовирусную активность даже у пациентов, устойчивых к лечению. Большинство из них продемонстрировали желаемый УВО в качестве монотерапии и достигли более высокого УВО при сочетании с ПЭГ-ИФН и рибавирином [18, 19].Успех ПППД в клинических испытаниях также стимулировал разработку схемы лечения без интерферона за счет комбинирования ПППД с различными функциональными профилями. Схема лечения без IFN полезна для пациентов с плохой переносимостью IFN и / или страдающих психологическими расстройствами. В настоящее время проводятся клинические испытания, изучающие эффективность различных комбинаций ПППД в качестве терапии против ВГС. Клинические результаты на данный момент показывают, что комбинированное лечение ПППД потенциально может иметь более короткую продолжительность лечения с лучшим УВО [18].Из-за нежелательных побочных эффектов и плохого УВО схемы PEG-IFN / рибавирин будущее терапии HCV будет сосредоточено на разработке лечения без IFN в качестве стандарта лечения. Учитывая успех клинических испытаний, можно предвидеть, что такое лечение станет доступным в ближайшем будущем. Однако проблема в подходах к комбинированному лечению DAA заключается в выборе штаммов вируса, устойчивых к лекарственным средствам. Пациенты, инфицированные такими штаммами, получат только один возможный курс лечения ПЭГ-ИФН / рибавирин, поскольку резистентность к интерферону не наблюдалась.Таким образом, традиционный режим с IFN-α останется критически важной частью терапии против HCV.
2.4. IFN-α КАК ТЕРАПЕВТИЧЕСКИЙ АГЕНТ ПРИ ВГВ-ИНФЕКЦИЯХ
В дополнение к его использованию для лечения HCV, PEG-IFN-α2a также использовался для лечения хронической HBV-инфекции. Даже при наличии эффективной вакцины около 350–400 миллионов человек инфицированы ВГВ, что представляет собой серьезную глобальную проблему для здоровья. Считающийся нецитопатическим, HBV способен вызывать иммунные реакции и приводит к стойкому воспалению печени, которое в конечном итоге приводит к циррозу и ГЦК [20].Было показано, что ПЭГ-ИФН-α2а эффективно очищает сыворотку от е-антигена гепатита В (HBeAg), снижает частоту ГЦК и улучшает выживаемость у пациентов с хроническим ВГВ. Несколько исследований также показали, что PEG-IFN-α2a оказывает длительное влияние на сохранение отрицательного HBeAg в сыворотке крови после лечения по сравнению с аналогами нуклеозидов (NA), такими как ламивудин (LMV), адефовир (ADV), энтекавир (ETV) и телбивудин. (LdT) [21]. Несмотря на успех, использование PEG-IFN-α2a в качестве монотерапии оказалось далеко не идеальным.В дополнение к неприятным побочным эффектам, вызванным IFN-α, как указано в этом обзоре, процент пациентов, у которых достигнута сероконверсия HBeAg (от HBsAg к поверхностным антителам к гепатиту B (анти-HBsAg)), обычно составляет менее 35% с частотой рецидивов. 5–10% [22]. Тем не менее, поскольку побочные эффекты IFN можно контролировать путем снижения дозы или прекращения лечения, PEG-IFN-α2a по-прежнему остается стандартом лечения хронической инфекции HBV в соответствии с рекомендациями Всемирной организации здравоохранения [23].Чтобы улучшить результаты лечения, несколько групп исследовали возможность комбинирования PEG-IFN-α2a с NA. У HBsAg-положительных пациентов с хроническим HBV частота неопределяемой сывороточной ДНК HBV и сероконверсии была выше в группе, получавшей комбинированную терапию. Кроме того, комбинированная терапия также показала превосходство в поддержании долгосрочного клиренса HBeAg и сероконверсии после окончания периода лечения по сравнению с монотерапией PEG-IFN-α2a [24–26]. Во время лечения PEG-IFN-α2a некоторые пациенты теряют HBeAg в сыворотке, сохраняя при этом высокие уровни ДНК HBV.У этих HBeAg-отрицательных пациентов не было обнаружено слабого вирусологического и серологического ответа на лечение PEG-IFN-α2a и более высокой частоты вирусологических рецидивов. Было показано, что длительное лечение ПЭГ-ИФН-α2a по сравнению с традиционным 48-недельным режимом лечения улучшает эффективность у HBeAg-отрицательных пациентов. Кроме того, было показано, что последовательная терапия NA и PEG-IFN-α2a, монотерапия NA или PEG-IFN-α2a с последующей комбинированной терапией или монотерапией NA или PEG-IFN-α2a является многообещающим методом лечения HBsAg. отрицательные пациенты, поскольку более 50% HBsAg-отрицательных пациентов смогли ответить на лечение и достигли УВО со значительным снижением сывороточной ДНК HBV [27, 28].Поскольку эти исследования проводились с небольшой когортой, потребуется клиническое испытание со значительным количеством участников для дальнейшей проверки эффективности последовательной терапии у HBsAg-отрицательных пациентов.
2.5. IFN-β КАК ТЕРАПЕВТИЧЕСКИЙ АГЕНТ ПРИ ВГС-ИНФЕКЦИИ
Хотя IFN-β чаще всего используется для лечения рассеянного склероза, его также использовали в противовирусной терапии, поскольку было показано, что IFN-β имеет противовирусную активность, сравнимую с IFN-α. . Эффективность IFN-β в качестве альтернативного терапевтического варианта или в сочетании со стандартным лечением инфекции HCV широко исследовалась в Азии, включая Японию, Корею и Китай [29–31].Эти исследования не только доказали эффективность IFN-β в качестве терапии HCV, но также показали многообещающие результаты в преодолении блока лечения у пациентов, у которых был плохой ответ на IFN-α-2b / рибавирин. Ishikawa et al. показали, что более высокий процент пациентов, инфицированных генотипом 1 ВГС, которые плохо реагировали на лечение IFN-α-2b / рибавирин, достиг УВО при лечении IFN-β в первые 2 недели с последующим IFN-α-2b / рибавирином по сравнению с IFN-α-2b / рибавирин отдельно. Более того, недавнее исследование показало, что 2-недельная предварительная терапия IFN-β / рибавирином с последующим 46-недельным лечением PEG-IFN-α / рибавирином значительно снизила вирусную нагрузку у пациентов, несущих аллель риска IL-28 , a группа, не отвечающая на лечение PEG-IFN-α / рибавирином [32].Кроме того, лечение IFN-β показало меньшую частоту побочных эффектов по сравнению с IFN-α. Однако лечение IFN-β довольно обременительно, поскольку для лечения доступна только рекомбинантная форма IFN-β. Эта форма IFN-β имеет более короткий период полувыведения и требует введения один или два раза в день для достижения желаемого результата.
2.6. ИФН ТИПА I КАК ДОБАВИТЕЛЬ ДЛЯ ПРОТИВОВИРУСНОЙ ТЕРАПИИ
Помимо сильного противовирусного агента, ИФН типа I также является мощным иммуномодулирующим средством.Таким образом, во многих исследованиях IFN типа I использовался в качестве адъюванта для повышения эффективности схемы вакцинации. Исследование, посвященное изучению эффективности IFN-α в качестве адъюванта вакцины против HBV в индукции ответа антител против HBeAg у лиц, не ответивших на вакцину, обнаружило незначительное увеличение процента пациентов, у которых вырабатывались антитела; 53% субъектов, получавших IFN-α, по сравнению с 41% в группе плацебо [33]. Однако в более недавнем исследовании включения IFN-α в схему вакцинации против HBV у здоровых субъектов не наблюдалось различий в скорости сероконверсии и Т-клеточных ответах между группами IFN-α и плацебо [34].Поскольку наблюдалась тенденция к повышению уровня активации APC, авторы предполагают, что оценка форм IFN-α, дозировки и режима вакцинации, которые должны использоваться в таких исследованиях, необходима для точной оценки эффективности IFN-α. α в качестве адъюванта.
3. Интерферон II типа: интерферон-гамма (IFN-γ)
3.1. СИГНАЛЬНЫЙ ПУТЬ IFN-γ
Активная молекула IFN-γ состоит из двух антипараллельных и интеркалирующих полипептидов, которые образуют двойную симметрию.Образование и сворачивание димера важны для его биологической функции и, как было показано, сохраняются среди позвоночных [35]. Хотя практически все клетки экспрессируют рецепторы IFN-γ, источник IFN-γ ограничен определенными типами клеток, а именно естественными киллерами (NK), Т-клетками и NKT-клетками. Биологическая активность IFN-γ инициируется при связывании с его рецептором, который состоит из двух лиганд-связывающих цепей IFN-γR1, уровень экспрессии которых среди клеток неизменно высок, и двух сигнальных цепей IFN-γR2, уровень экспрессии которых определяется клеткой. типы и состояние активации клеток.IFN-γ сначала связывается с IFN-γR1, и образование комплекса IFN-γ: IFN-γR1 способствует его ассоциации с IFN-γ R2, который затем инициирует нижестоящие сигнальные события [36]. Образование этого рецепторного комплекса лиганда позволяет JAK1 и JAK2, которые конститутивно связывают IFN-γR1 и IFN-γR2 соответственно через свои N-концевые домены, трансактивировать друг друга. Затем активированные JAK фосфорилируют остаток тирозина на каждой цепи IFN-γR1 с образованием стыковочного сайта для STAT1, который затем фосфорилируется JAK.PSTAT1s образуют гомодимер, который перемещается в ядро и инициирует транскрипцию генов-мишеней () [37]. Путь JAK / STAT является основным сигнальным путем, инициируемым стимуляцией IFN-γ. Подобно IFN типа I, IFN-γ также может активировать STAT1-независимые пути, такие как MAP-киназа, PI3K и сигнальный путь NF-κB, поскольку все они, как было показано, активируются после обработки IFN-γ [38]. Кроме того, было показано, что IFN-γ может также индуцировать неканонический сигнальный путь.По этому пути IFN-γ вместе с одной из его субъединиц рецептора IFNGR1 и pSTAT1 перемещаются в ядро и индуцируют экспрессию гена, связываясь с элементами GAS в промоторной области IFN-индуцибельных генов [39].
3.2. IFN-γ ПРОТИВОВИРУСНАЯ АКТИВНОСТЬ
Во время вирусной инфекции IFN-γ может включать клеточный противовирусный механизм, индуцируя экспрессию нескольких противовирусных белков. В дополнение к PKR, OAS и Mx GTPase, упомянутым в предыдущем разделе, IFN-γ может также запускать экспрессию dsRNA-специфической аденозиндезаминазы (ADAR), которая ингибирует репликацию вируса, редактируя или вызывая неправильную трансляцию вирусных белков.Подобно IFN типа I, IFN-γ может индуцировать апоптоз за счет активации FasL для уничтожения инфицированных вирусом клеток. Кроме того, IFN-γ усиливает экспрессию IFN типа I, что дополнительно увеличивает антивирусное состояние клеток. Помимо индукции противовирусных белков, IFN-γ также проявляет свою противовирусную активность, модулируя как врожденные, так и адаптивные иммунные ответы. Во-первых, IFN-γ может индуцировать экспрессию провоспалительных цитокинов и хемокинов эндотелиальными клетками, эпителиальными клетками и фибробластами, рекрутируя макрофаги, нейтрофилы и Т-клетки в очаг инфекции [40].Важно отметить, что IFN-γ играет решающую роль в передаче противовирусных сигналов от врожденного иммунного ответа к адаптивному, чтобы полностью активировать противовирусный иммунитет хозяина. Получив сигнал IFN-γ, APC увеличивают экспрессию MHC класса II и костимулирующих молекул, что, в свою очередь, способствует активации CD4 + Т-клеток и инициации адаптивного иммунного ответа против вирусной инфекции. IFN-γ также индуцирует экспрессию IL-12 с помощью APC. IL-12 не только активирует NK-клетки, основной противовирусный клеточный компонент врожденного иммунитета, но также стимулирует развитие CD4 + Th2 T-клеток, процесс, который имеет решающее значение для борьбы с вирусной инфекцией.
3.3. IFN-γ КАК ТЕРАПЕВТИЧЕСКИЙ АГЕНТ ПРИ ВИРУСНОЙ ИНФЕКЦИИ
Несмотря на то, что IFN-γ является отличительным признаком ответа Th2, который приводит к сильной противовирусной активности, при клинических испытаниях IFN-γ в качестве противовирусного средства для лечения ВИЧ дал неутешительные результаты. Даже с его способностью увеличивать активность CTL и NK-клеток, IFN-γ не смог снизить вирусную нагрузку ВИЧ у пациентов в клинических испытаниях, разработанных для оценки токсичности и эффективности IFN-γ [40]. Таким образом, внимание к IFN-γ и ВИЧ сместилось с его использования в качестве монотерапии к его комбинации с высокоактивной антиретровирусной терапией (ВААРТ).ВААРТ представляет собой комбинацию двух или более антиретровирусных препаратов, которая подавляет репликацию ВИЧ и резко снижает заболеваемость и смертность, связанные с ВИЧ. Однако возникновение оппортунистических инфекций остается серьезной проблемой у пациентов с ВИЧ, леченных HARRT, из-за нарушения Т-клеточного иммунитета. IFN-γ использовался с положительным результатом для лечения ВИЧ-ассоциированных оппортунистических инфекций с использованием или без HARRT для восстановления иммунного ответа у пациентов с ВИЧ [41]. Учитывая важность IFN-γ в Th2-ответе хозяина, несколько групп включили IFN-γ в схемы вакцинации ДНК в качестве адъюванта в моделях ВИЧ на животных [40].Однако результаты не были впечатляющими, поскольку IFN-γ не улучшал или лишь незначительно улучшал защитные иммунные ответы против последующих вирусных проблем. Помимо возможного использования в лечении ВИЧ, IFN-γ также рассматривался как вариант лечения HCV и HBV. Однако в недавнем сообщении добавление IFN-γ в схему лечения HCV не привело к успешному подавлению инфекции HCV у пациентов, которые не отвечали на PEG-IFN / рибавирин [42]. Однако в этом исследовании время лечения IFN-γ может быть проблемой, поскольку он был добавлен позже в схему лечения, и сообщалось, что элиминация вируса на ранней фазе лечения тесно связана с лучшим показателем УВО. .Хотя результаты использования IFN-γ при лечении HCV и HBV были противоречивыми, IFN-γ может иметь дополнительные преимущества. Исследование, проведенное Wu et al. показали, что HBsAg-положительные пациенты со 2–4 стадиями фиброза печени достигли значительного улучшения показателей фиброза после 9 месяцев лечения IFN-γ [43].
4. Интерферон III типа: интерферон-лямбда (IFN-λ)
4.1. СИГНАЛЬНЫЙ ПУТЬ IFN-λ
Человеческие IFN или IFN-λ типа III, включая IFN-λ1, IFN-λ2 и IFN-λ3 (или IL-29, IL-28A и IL-28B соответственно), были идентифицированы двумя независимыми группами. в 2003 г.Хотя IFN-λ структурно родственен цитокинам, связанным с IL-10, он может индуцировать противовирусную активность в различных клетках-мишенях, которые экспрессируют рецептор IFN-λ [44]. Таким образом, они были функционально классифицированы как новый тип IFN. Белки IFN-λ связываются и передают сигнал через рецепторный комплекс, состоящий из цепи IL-10R2 (также важной частью рецепторных комплексов для IL-10, IL-22 и IL-26) и цепи IFN-λR1 ( также известный как IL-28RA), который используется только IFN-λ. Хотя IFN-λ может экспрессироваться практически всеми типами клеток, которые могут быть инфицированы вирусом, субъединица IFN-λR1 конститутивно экспрессируется ограниченными типами клеток, в первую очередь клетками эпителиального происхождения.Было показано, что IFN-λR1 также экспрессируется на некоторых иммунных клетках крови, включая В-клетки, Т-клетки, DC и макрофаги. Однако эти клетки экспрессировали короткий вариант сплайсинга рецептора IFN-λ (sIFN-lR1 / sIL-28R1), что приводит к более слабой силе передачи сигнала при стимуляции IFN-λ [45]. Напротив, фибробласты, эндотелиальные клетки и большинство лейкоцитов не экспрессируют полноразмерную цепь IFN-λR1; следовательно, они не реагируют на стимуляцию IFN-λ. IFN-λ сначала связывается с цепью IFN-λR1, что приводит к изменению конформации, которое способствует привлечению IL-10R2.Образование рецепторного комплекса IFN-λ и IFN-λ приводит к активации JAK с последующим фосфорилированием тирозина внутриклеточного домена цепи IFN-λR1, что приводит к активации STAT1 и STAT2 (). Передача сигналов через рецепторные комплексы IFN-λ или IFN-α приводит к активации одного и того же каскада передачи сигнала JAK-STAT; хотя сила передачи сигналов, индуцированная IFN-λ, сравнительно слабее [46].
4.2. ПРОТИВОВИРУСНАЯ АКТИВНОСТЬ
Подобно IFN типа I, IFN-λ обладает способностью индуцировать противовирусную активность в клетках-мишенях.Установлено, что IFN-λ может ингибировать репликацию HBV в различных клеточных линиях гепатоцитов мыши, а также репликацию субгеномного и полноразмерного репликона HCV в клеточной линии гепатомы человека [47, 48]. Недавние сообщения также показали, что IFN-λ ингибирует репликацию ВИЧ-1 в макрофагах и первичных Т-клетках [49, 50]. Ингибирование вируса IFN-λ также было показано in vivo , когда локально доставленный рекомбинантный IFN-λ ингибировал репликацию HHV-1, HHV-2 и IAV во влагалище и легких [51].Подобно IFN типа I и II, IFN-λ также может индуцировать экспрессию антивирусных белков-маркеров, OAS и белка Mx [52]. Помимо ингибирования репликации вируса, IFN-λ может ограничивать длительную вирусную инфекцию за счет повышения уровня экспрессии белков MHC класса I на поверхности клетки, что, в свою очередь, способствует распознаванию и разрушению инфицированных вирусом клеток врожденной иммунной системой. , и индуцируя апоптоз инфицированных вирусом клеток [53].
4.3 ПЕГ-ИФН-λ КАК ТЕРАПЕВТИЧЕСКИЙ АГЕНТ ДЛЯ ИНФЕКЦИИ ВГС
Из-за быстрых генетических изменений, которые делают ВГС устойчивым к лекарствам, направленным на репликацию и сборку вируса, лечение ИФН-α остается эффективным средством лечения инфекции ВГС, несмотря на множество системных побочных эффектов.Однако, поскольку ограниченная тканевая экспрессия цепи IFN-λR1 обеспечивает локализованную реакцию, противовирусная активность IFN-λ делает его гораздо более безопасным и менее токсичным выбором в качестве терапевтического агента для вирусной инфекции. Поскольку доклинические исследования показали, что ПЭГ-ИФН-λ ингибирует репликацию ВГС в гепатоцитах человека без гематологической цитотоксичности, в 2007 г. было проведено исследование фазы IA с увеличением дозы на здоровых добровольцах [54, 55]. Субъекты получали однократную дозу ПЭГ-ИФН-λ, вводимую подкожно.Все тестируемые дозы (0,5, 1,5, 5 и 7,5 мкг / кг) хорошо переносились, и у субъектов не наблюдалось побочных эффектов, вызванных IFN. Однако у нескольких добровольцев в группе 7,5 мкг / кг развилось значительное повышение уровня трансаминазы, что считалось дозолимитирующей токсичностью и могло быть отменено снижением дозировки IFN. Последующее исследование фазы IB было проведено для оценки эффективности и цитотоксичности IFN-λ у пациентов, инфицированных HCV, включая пациентов, ранее не получавших лечения, и пациентов, у которых возник рецидив после предыдущего лечения IFN-α.Набранные пациенты получали PEG-IFN-λ с рибавирином или без него еженедельно или раз в две недели в диапазоне доз 0,5–3 мкг / кг в течение 4 недель. Во время испытания у шести пациентов был повышен уровень трансаминазы, который исчез после прекращения лечения. В целом наблюдалось значительное снижение частоты побочных эффектов типа IFN-α, и, в отличие от PEG-IFN-α, обработка PEG-IFN-λ не проявляла значительной гематологической токсичности. Наиболее важно то, что пациенты, получавшие ≥1,5 мкг / кг / неделю, демонстрировали снижение вирусной нагрузки как минимум на 2 log; 4 журнала в сочетании с лечением рибавирином.Неожиданно у двух пациентов, которые ранее лечились IFN-α, развились антитела, перекрестно реагирующие с IFN-λ, наблюдение, которое подразумевает, что эффективность лечения IFN-λ может быть ограничена у некоторых пациентов, ранее получавших IFN-α.
Три независимых полногеномных ассоциативных исследования (GWAS) идентифицировали SNP в гене IL28B как связанные с исходом лечения PEG-IFN-α / рибавирином у пациентов с HCV [56]. Было проведено 12-недельное клиническое исследование фазы IIA, в котором сравнивали безопасность и противовирусную активность 4 фиксированных доз ПЭГ-ИФН-λ и ПЭГ-ИФН-α у пациентов с ВГС, не получавших лечения.Процент пациентов с неопределяемым вирусом был значительно выше среди пациентов с благоприятным генотипом (86%) по сравнению с пациентами, несущими аллель риска (50%). Эти результаты предполагают, что эффективность лечения ПЭГ-ИФН-λ будет различаться в зависимости от генотипа IL28B [54]. Последнее исследование фазы IIB было разработано для оценки безопасности, эффективности и фармакокинетики фиксированной дозы ПЭГ-ИФН-λ по сравнению с ПЭГ-ИФН-α у 526 не получавших лечения пациентов, инфицированных генотипами 1, 2, 3 и 4 ВГС. .Пациенты получали ПЭГ-ИФН-λ 240 мкг, ПЭГ-ИФН-λ 180 мкг, ПЭГ-ИФН-λ 120 мкг или ПЭГ-ИФН-α 180 мкг еженедельно, все в комбинации с ежедневным рибавирином. Период лечения составляет 48 недель для пациентов с генотипами 1 и 4 HCV, которые проявили плохой ответ на лечение PEG-IFN-α и рибавирином, и 24 недели для пациентов с генотипами 2 и 3 HCV. Лечение ПЭГ-ИФН-λ и рибавирином позволило достичь более высоких показателей быстрого вирусологического ответа (БВО) и полного раннего вирусологического ответа (цЭВО) независимо от генотипов ВГС по сравнению с лечением ПЭГ-ИФН-α / рибавирином.Кроме того, было меньше случаев побочных эффектов типа IFN-α, а также меньшее снижение дозы при анемии в группе лечения PEG-IFN-λ до 12 недель. Однако частота серьезных нежелательных явлений была одинаковой во всех группах лечения вплоть до 12 недели [57]. Результаты исследования фазы III на данный момент демонстрируют возможность использования IFN-λ в качестве терапии инфекции HCV. Тщательное титрование дозировки должно привести к такому режиму лечения, который подавлял бы репликацию вируса, но в то же время уменьшал бы побочные эффекты.Основываясь на успехе использования IFN-λ в клинических испытаниях терапии HCV, можно предвидеть возможное включение IFN-λ в лечение других вирусных инфекций.
5. IFN в качестве терапевтических агентов при других заболеваниях
Помимо противовирусной терапии, IFN также использовались в качестве терапевтических агентов при раковых и аутоиммунных заболеваниях. Благодаря своим антипролиферативным, антиангиогенезным и иммуномодулирующим эффектам IFN-α был включен в несколько схем лечения рака в качестве адъюванта.При меланоме режим высоких доз IFN-α2b (HDI, как рекомбинантные, так и пегилированные формы) был одобрен для использования в качестве части лечения, поскольку многочисленные метаанализы показали, что HDI значительно увеличивает выживаемость без признаков заболевания и общую выживаемость в условиях высокой выживаемости. риск кожной меланомы [58, 59]. IFN-α также оценивался в нескольких клинических испытаниях как часть схемы лечения почечно-клеточной карциномы [60–63]. В этих исследованиях пациенты достигли более длительной выживаемости без прогрессирования заболевания при лечении низкими дозами IFN-α в сочетании с различными химиотерапевтическими препаратами.До открытия ингибитора тирозинкиназы, Иматиниба, ИФН-α был выбором лечения хронического миелоидного лейкоза (ХМЛ). Хотя иматиниб по-прежнему остается передовым препаратом для лечения ХМЛ, несколько групп поставили задачу повысить эффективность иматиниба путем комбинирования PEG-IFN-α2a или PEG-IFN-α2b в схему лечения. Результаты этих исследований показали, что добавление ПЭГ-ИФН значительно снижает количество лейкозных клеток у пролеченных пациентов [64–66]. В 1993 году IFN-β был впервые одобрен для лечения рассеянного склероза (MS) в США.В настоящее время доступно несколько продуктов IFN-β, одобренных FDA (). В то время как симптомы гриппа обычно наблюдаются у пролеченных пациентов, лечение ИФН-β для рассеянного склероза считается безопасным и эффективным. Хотя точный механизм того, как IFN-β ингибирует прогрессирование рассеянного склероза, неизвестен, его противовоспалительные эффекты и его способность индуцировать образование регуляторных Т-лимфоцитов, предотвращать пересечение лейкоцитами гематоэнцефалического барьера и способствовать апоптозу в аутореактивных Т-клетках. IFN-β — привлекательный вариант лечения рассеянного склероза [67, 68].По сравнению с IFN типа I IFN-γ не так широко используется в клинике. Однако было показано, что IFN-γ эффективен в борьбе с тяжелым идиопатическим атопическим дерматитом за счет снижения количества эозинофилов в крови и ингибирования синтеза IgE и пролиферации Т-клеток [69]. IFN-γ также использовался у пациентов с хронической гранулематозной болезнью, нарушением с дефектом ферментного комплекса, ответственного за образование супероксида фагоцитами. Однако использование IFN-γ у этих пациентов предназначено для предотвращения повторного возникновения инфекций, а не для лечения основного генетического заболевания [70].
В поисках раннего лекарства от COVID-19, исследователи обращаются к интерферонам
В начале этого года, когда COVID-19 все еще был локальной вспышкой в Китае, Элеонора Фиш, иммунолог из Университета Торонто, обратилась к своим коллегам из Ухани. изучить возможность оценки терапии интерфероном у пациентов, инфицированных коронавирусом. Фиш изучает интерфероны (IFN) — белки, вырабатываемые организмом в ответ на вирусные инфекции — почти 35 лет, и ее предыдущие благоприятные результаты с синтетической версией во время вспышки атипичной пневмонии в Канаде в 2003 году натолкнули на эту идею.
Коллеги Фиша в Китае связали ее с Цюн Чжоу, врачом, который в то время лечил пациентов с COVID-19 в больнице Ухань Юнион. Фиш вспоминает, что Чжоу был очень рад этому предложению. Поскольку это была вспышка, не было времени оптимизировать IFN для использования против SARS-CoV-2, и Фиш и Чжоу пришлось довольствоваться тем, что было доступно и что ранее успешно применялось при других коронавирусных инфекциях. Для клинического исследования команда Чжоу использовала IFN-альфа-2b, впервые одобренный Управлением по контролю за продуктами и лекарствами США (FDA) для лечения рака в 1986 году, благодаря его иммуномодулирующим, антипролиферативным и антиангиогенным эффектам.Исследователи протестировали ИФН вместе с арбидолом, широко используемым противовирусным препаратом широкого спектра действия, у 77 пациентов, поступивших в госпиталь Юнион в январе и феврале с подтвержденной инфекцией SARS-CoV-2. У каждого из них были умеренные симптомы и ни один из них не нуждался в интенсивной терапии.
Результаты, опубликованные 15 мая в журнале Frontiers in Immunology , показали, что пациенты, получавшие только IFN-альфа-2b или в комбинации с арбидолом, выводили вирус из верхних дыхательных путей в среднем на семь дней быстрее, чем группа, получавшая только арбидол. .Наряду с этим у пациентов, получавших IFN-альфа-2b, резко снизились уровни в крови маркеров воспаления, таких как интерлейкин-6 и С-реактивный белок. Фиш добавляет, что еще неопубликованные данные показывают, что IFN-альфа-2b также ограничивает патологии легких, что подтверждается компьютерной томографией.
По общему мнению, любое противовирусное средство от COVID следует использовать на ранней стадии, даже в профилактических целях.
—Людмила Прокунина-Олссон, NIH
«Я думаю, что это достойный клинический отчет, и они обращают внимание на маркеры воспаления, что важно», — говорит Андреас Вак, иммунолог из Института Фрэнсиса Крика в Лондоне, который работает. на IFN, но не участвовал в этом исследовании.Это потому, что известно, что IFN-альфа вызывает провоспалительную среду. Фиш говорит, что в ее исследовании у пациентов, получавших IFN-альфа-2b, не было доказательств цитокинового шторма, одного из опасных иммунных ответов, наблюдаемых у некоторых пациентов с COVID-19.
Джордан Фельд, гепатолог из больницы общего профиля Торонто, говорит, что, хотя это исследование не было рандомизированным контролируемым испытанием, оно тем не менее дает некоторые надежды на идею использования интерферонов при COVID-19. 20 июля британская компания Synairgen сообщила неопубликованные данные фазы 2 испытания экспериментального препарата IFN, распыленного IFN-бета, который, по-видимому, снизил риск развития тяжелого заболевания у госпитализированных пациентов с COVID-19 на 79 процентов.
В этой пандемии приветствуются любые новые источники наркотиков. Только противовирусный агент ремдесивир получил разрешение FDA на экстренное использование для лечения пациентов с тяжелой формой COVID-19. 25 июня обнадеживающие предварительные результаты исследования UK RECOVERY побудили Национальный институт здоровья США (NIH) рекомендовать дексаметазон, кортикостероид, для лечения пациентов с COVID-19 на ИВЛ или пациентов, которым требуется дополнительный кислород. Но пока нет одобренных лекарств, которые можно было бы назначать на ранних стадиях инфекции или в профилактических целях тем, кто находится в группе высокого риска.
В таком безрадостном терапевтическом сценарии растущее количество данных лабораторных исследований и нескольких клинических испытаний IFNs, как по отдельности, так и в комбинации с другими противовирусными препаратами, предполагает, что синтетические IFN могут восполнить этот пробел.
Вирусы и интерфероны взаимно антагонистичны.
Конфокальные микроскопические изображения первичных гепатоцитов человека от доноров печени с (слева) и без (справа) продукции IFN-лямбда, отмеченных красным.
Людмила Прокунина-Олссон
Существует три типа природных IFN, каждый из которых секретируется собственным набором типов клеток.Оба типа I (IFN-альфа и IFN-бета) и тип III (IFN-лямбда) представляют собой противовирусные белки, продуцируемые на ранней стадии в инфицированных клетках для защиты других клеток, находящихся поблизости. «Как только генетический материал [вируса] будет обнаружен, [IFN] его пережевывают», — говорит Фиш. В то же время IFN привлекают к участку инфекции иммунные клетки, которые также помогают избавиться от вируса.
IFNs I и III, по большей части, являются неотъемлемой частью врожденного иммунного ответа организма, при этом тип III специфически участвует в локализованном иммунном ответе в местах, где патогены проникают в организм, таких как слизистые оболочки легких , кишечник и печень.Но естественного ответа организма на IFN, по-видимому, недостаточно, чтобы предотвратить заражение SARS-CoV-2.
В статье, опубликованной 28 мая в Cell , Бенджамином тенОвером, вирусологом из Медицинской школы Икана на горе Синай в Нью-Йорке, и его коллегами было обнаружено, что инфекция SARS-CoV-2 вызывает низкие уровни типов I и III. IFN у хорьков. Фиш и Вак отмечают, что все вирусы обладают многочисленными механизмами подавления ответа IFN.
См. «Ответ клеток на SARS-CoV-2, отличный от гриппа, RSV»
Поэтому логично предположить, что введение синтетических препаратов IFN повысит противовирусный иммунитет организма, что, возможно, даст хозяину преимущество.
Изображение иммунофлуоресцентной микроскопии первичных клеток легких человека (ДНК помечено синим), инфицированных SARS-CoV-2 (зеленый)
Бенджамин Нильссон-Пайант (лаборатория Бенджамина тенОВера)
Тип I или тип III: с чем лучше бороться COVID-19?
Хотя специалисты по IFN утверждают, что препараты типа I и III являются привлекательными терапевтическими вариантами при COVID-19, они расходятся во мнениях относительно того, какой из двух будет наиболее подходящим при COVID-19, и экспериментальные данные показывают, что оба типа имеют потенциал.
Исследование, опубликованное 19 июня, демонстрирует, что IFN-бета-1a типа I, одобренный в настоящее время для лечения рассеянного склероза, оказался высокоэффективным в подавлении репликации SARS-CoV-2 in vitro. В препринте, опубликованном 7 мая, показано, что лечение клиническим кандидатом IFN-lambda-1a, IFN типа III, ингибирует репликацию SARS-CoV-2 как in vitro, так и на моделях на мышах. Другой препринт, опубликованный 20 мая, демонстрирует, что ИФН типа I и типа III снижают репликацию SARS-CoV-2 в первичных культурах эпителия дыхательных путей человека.
Хотя синтетический ИФН-лямбда еще не одобрен FDA, предварительные результаты клинических испытаний на пациентах с гепатитом D показывают, что он обладает такой же противовирусной активностью, что и ИФН типа I, но намного безопаснее и лучше переносится. Исследование на мышах показало, что синтетический ИФН-лямбда столь же эффективен, как ИФН-альфа при лечении гриппа, но не имеет таких же провоспалительных эффектов.
Ограниченные побочные эффекты IFN-лямбда могут быть связаны с характером распределения рецепторов, которые появляются исключительно на барьерных поверхностях, таких как эпителий легких, кишечника и печени, тогда как рецепторы для IFN типа I встречаются повсеместно, говорит Джеффри Гленн, профессор Стэнфордского университета и основатель Eiger BioPharmaceuticals, компании, производящей лекарство с ИФН-лямбда.«Соотношение пользы и риска действительно убедительно [для IFN-лямбда]. IFN-альфа — очень сложный препарат, поскольку он имеет множество побочных эффектов ». К ним относятся гриппоподобные симптомы, усталость, низкие показатели крови, бессонница и расстройства настроения.
Я был бы очень, очень, очень осторожен с этим.
—Андреас Вак, Институт Фрэнсиса Крика
Людмила Прокунина-Олссон, старший научный сотрудник Национального института здравоохранения, открыла и клонировала новый ген IFN-лямбда в 2013 году и не связана с какими-либо клиническими испытаниями IFN для COVID-19. сообщает The Scientist в электронном письме, что IFN типа I является очень мощным противовирусным средством, но его механизм действия более воспалительный.«В легких COVID достаточно воспалений, и критически важно избегать любых дополнительных воспалений», — говорит она. «Если вы используете какие-либо интерфероны, мы рекомендуем использовать IFN-лямбда».
Майкл Гейл-младший, иммунолог из Вашингтонского университета, который в настоящее время работает над тем, как клетки-хозяева распознают SARS-CoV-2 и запускают врожденный иммунный ответ, но не участвует в исследованиях IFN-лямбда, также поддерживает клиническое использование IFN-лямбда. «При SARS-CoV-2 важно не активировать лимфоциты, поскольку они уже активированы в воспалительном процессе.«Поскольку рецепторы IFN-лямбда не экспрессируются на лимфоцитах, иммунные клетки не активируются.
Исследователи IFN-лямбда говорят, что они обеспокоены тем, что IFN типа I, который, как известно, является провоспалительным, может спровоцировать цитокиновый шторм у пациентов с COVID-19. Исследование, опубликованное 10 июля в журнале Science Immunology , подтверждает, что IFN-ответ типа I действительно провоспалительный при коронавирусных инфекциях и играет ключевую роль в развитии тяжелого COVID-19.
«Я бы очень не решился использовать IFN типа I», — говорит Томас Маррон, иммунолог по онкологическим заболеваниям из Медицинской школы Икана на горе Синай, который возглавляет исследование IFN-лямбда.
Но для многих исследователей IFN типа I не исключен для лечения COVID-19. Хотя Фельд, сторонник IFN-лямбда, также обеспокоен безопасностью IFN I типа в этом контексте, он говорит, что привлекательность IFN I типа состоит в том, что, будучи одобренными препаратами, они могут производиться массово и сразу же выдаваться. «Очевидно, даже если мы докажем, что IFN-лямбда очень эффективен, его массовое производство будет проблемой». Кроме того, сторонники препаратов с ИФН I типа утверждают, что опасения по поводу переносимости ИФН-альфа не столько являются проблемой при краткосрочном лечении острой вирусной инфекции, такой как COVID-19.А поскольку SARS-CoV-2 распространяется системно, IFN-лямбда не защищает все типы клеток.
См. «Ответ клеток на SARS-CoV-2 отличается от гриппа, RSV»
IFN-лямбда имеет еще один недостаток. Гейл предупреждает, что если вводить его слишком долго или в слишком высокой дозе, «мы можем столкнуться с проблемами, когда это будет препятствовать регенерации тканей», особенно в легких. В исследовании, опубликованном в июне, команда Вака обнаружила, что IFN типа I и III активируют антипролиферативные пути и пути гибели клеток в эпителиальных клетках дыхательных путей мышей, инфицированных вирусом гриппа, и что чрезмерное или длительное производство IFN нарушает восстановление эпителия легких во время выздоровления от вирусной инфекции.
Иван Занони из Гарвардской медицинской школы возглавил второе исследование, также опубликованное в прошлом месяце, которое дало аналогичные результаты в отношении IFN-лямбда с использованием синтетической версии SARS-CoV-2. Он говорит The Scientist , что IFN могут быть очень хорошими, если их вводить на ранней стадии COVID-19, чтобы ограничить распространение инфекции. «Когда вы переходите к тяжелой форме COVID-19, пациентам в отделении интенсивной терапии или госпитализированным пациентам, нужно быть очень осторожным, поскольку мы обнаружили, что у IFN [как типа I, так и типа III] есть темная сторона», — говорит он.
«Общее мнение в этой области состоит в том, что любые противовирусные препараты при COVID следует использовать на ранней стадии, даже в профилактических целях», — говорит Прокунина-Олссон.«На более поздних стадиях заболевания, когда инфекция распространяется на легкие, любой противовирусный препарат может быть опасен» из-за риска цитокинового шторма или повреждения ткани легких иммунными клетками.
И Вак, и Занони подчеркивают The Scientist необходимость проявлять осторожность с такими мощными противовирусными препаратами, как IFN. «Это сложно, — говорит Вак, — и я был бы очень, очень, очень осторожен с этим».
Срезы тканей легких мышей после заражения гриппом. Изображение слева — это элемент управления.Секции, где передача сигналов IFN-лямбда заблокирована (справа), показывают улучшенный рост и дифференцировку эпителиальных клеток (окрашивание мультицилилированных клеток в красный цвет).
andreas wack
Проведение клинических испытаний ИФН
ИФН типа I и III проходят клинические испытания во всем мире. В многоцентровом рандомизированном исследовании фазы 2 в Гонконге, которое было опубликовано в The Lancet 8 мая, тройная противовирусная терапия с инъекционным IFN-бета-1b, лопинавиром-ритонавиром (пероральный ингибитор протеазы) и рибавирином (пероральный аналог нуклеозидов). ) был безопасен и превосходил один лопинавир-ритонавир в сокращении продолжительности выделения вируса, уменьшении симптомов и позволял пациентам с COVID-19 от легкой до умеренной степени быстрее уйти домой из больницы.
В ходе продолжающегося многоцентрового рандомизированного контролируемого исследования Synairgen в Великобритании исследуется ингаляционный IFN-бета-1a в сравнении с плацебо у госпитализированных пациентов с подтвержденным или подозреваемым COVID-19, не госпитализированных пациентов с хроническими заболеваниями и медицинских работников, находящихся на переднем крае. с высоким риском заражения коронавирусом. Евангелос Андреакос, иммунолог из Афин, Греция, говорит, что использование ингаляционного интерферона I типа — интересный подход, который может обойти системные побочные эффекты препарата, доставив его непосредственно в легкие.
Другие испытания включают испытание ВОЗ SOLIDARITY, начатое 20 марта, которое включает тестирование IFN-бета в сочетании с другими противовирусными препаратами, и открытое испытание в Китае, в препринте которого 7 мая сообщается, что IFN-alpha нос. Капли появились для предотвращения заражения коронавирусом почти у 3000 медицинских работников. Кроме того, Fish активно ищет партнеров для проведения клинических испытаний IFN-альфа у пациентов с COVID-19 в Индии и других странах.
Для IFN типа III в настоящее время проводится шесть клинических испытаний в США и Канаде, в которых тестируется IFN-lambda Eiger BioPharmaceuticals на широком спектре пациентов с COVID-19.
Апиндер Сингх, специалист по инфекционным заболеваниям из Стэнфордского университета, которая проводит одно из этих испытаний IFN-лямбда, говорит, что ее исследование сосредоточено исключительно на амбулаторных пациентах с COVID-19. Обоснование этого состоит в том, что 80 процентов инфицированных пациентов никогда не будут госпитализированы. «Но это они распространяют это в сообществе. Наша цель — выявить пациентов, которые находятся на очень ранней стадии заболевания, идея заключается в том, что, если вы сможете добраться до них на ранней стадии, вы сможете уменьшить распространение вируса и сократить время нахождения в карантине », — говорит она.На данный момент в Стэнфордское испытание набрано около 60 пациентов.
Испытания, которые Маррон проводит на горе Синай, а еще одно — в Массачусетской больнице общего профиля в Бостоне, тестируют IFN-лямбда Эйгера у госпитализированных пациентов с COVID-19, в то время как испытание в Университете Джона Хопкинса проверяет профилактическое использование препарата у людей, находящихся в больнице. высокий риск заражения. Между тем, предварительные результаты исследования стационарных и амбулаторных пациентов, которое возглавляет Фельд, показывают, что препарат безопасен и имеет минимальные побочные эффекты, сообщает он The Scientist .
Клиффорд Лейн, заместитель директора по клиническим исследованиям и специальным проектам Национального института аллергии и инфекционных заболеваний, указывает на руководящие принципы лечения NIH, которые рекомендуют не использовать интерфероны типа I при COVID-19, за исключением случаев клиническое испытание, обоснование которого состоит в том, что эти IFN обычно не проявляют никакой пользы при использовании у пациентов с другими коронавирусными инфекциями, и что значительная токсичность IFN типа I перевешивает потенциальную пользу.
В рекомендациях NIH также указано, что из двух IFN типа I IFN-бета переносится лучше, чем IFN-alpha, но результаты недавнего рандомизированного контролируемого исследования не подтверждают использование IFN-бета-1a для лечения острый респираторный дистресс-синдром.
Отмечая энтузиазм, связанный с использованием IFN-лямбда при COVID-19, Лейн говорит: «Я непредвзято отношусь ко всем новым подходам, если они проходят тщательное тестирование».
Исследование ответа интерферона I типа при ANCA-ассоциированном васкулите
Connelly, K. L. et al. Продольная ассоциация хемокинов, индуцированных интерфероном 1 типа, с активностью заболевания при системной красной волчанке. Sci. Отчет 8 (1), 3268 (2018).
ADS CAS PubMed PubMed Central Статья Google Scholar
Rice, G. I. et al. Оценка интерферон-связанных биомаркеров синдрома Айкарди-Гутьера, связанных с мутациями в TREX1, RNASEh3A, RNASEh3B, RNASEh3C, SAMHD1 и ADAR: исследование случай-контроль. Lancet Neurol. 12 (12), 1159–1169 (2013).
CAS PubMed PubMed Central Статья Google Scholar
Ли А. Дж. И Ашкар А. А. Двойственная природа интерферонов типа I и типа II. Фронт. Иммунол. 9 , 2061 (2018).
PubMed PubMed Central Статья CAS Google Scholar
Porritt, R.A. & Hertzog, P.J. Динамический контроль передачи сигналов IFN типа I с помощью интегрированной сети негативных регуляторов. Trends Immunol. 36 (3), 150–160 (2015).
CAS PubMed Статья PubMed Central Google Scholar
Кроу, Ю. Дж. Интерферонопатии типа I: новый набор врожденных нарушений иммунитета. Ann. Акад. Sci. 1238 , 91–98 (2011).
ADS CAS PubMed Статья Google Scholar
Baechler, E.C. et al. Сигнатура интерферона в периферической крови пациентов с дерматомиозитом связана с активностью заболевания. Мол. Med. 13 (1–2), 59–68 (2007).
CAS PubMed PubMed Central Статья Google Scholar
Kimoto, O. et al. Активация пути интерферона в периферической крови пациентов с синдромом Шегрена. Дж.Ревматол. 38 (2), 310–316 (2011).
CAS PubMed Статья Google Scholar
Хан И. и Уоттс Р. А. Классификация ANCA-ассоциированного васкулита. Curr. Ревматол. Отчет 15 (12), 383 (2013).
PubMed Статья Google Scholar
Pearce, F. A. et al. Заболеваемость ANCA-ассоциированным васкулитом в британской популяции смешанного этнического происхождения. Ревматология (Оксфорд) 55 (9), 1656–1663 (2016).
Артикул Google Scholar
Berti, A. et al. Эпидемиология васкулита, ассоциированного с антинейтрофильными цитоплазматическими аутоантителами, в округе Олмстед, штат Миннесота: американское популяционное исследование, проводимое в течение двадцати лет. Arthritis Rheumatol. 69 (12), 2338–2350 (2017).
CAS PubMed PubMed Central Статья Google Scholar
Hunder, G.G. et al. Критерии классификации васкулита, принятые в 1990 году Американским колледжем ревматологии. Введение .. Arthritis Rheum. 33 (8), 1065–1067 (1990).
CAS PubMed Статья Google Scholar
Роббинс С.Л. и Котран Р.С. Патологическая основа болезни Роббинса и Котрана 7-е издание (ред. Кумар, В., Абул, К. и Фаусто, Н.) 9 (Elsevier Saunders, 2005).
Ui Mhaonaigh, A. et al. Гранулоциты низкой плотности при ANCA-васкулите являются гетерогенными и гипочувствительными к антителам против миелопероксидазы. Фронт. Иммунол. 10 , 2603 (2019).
PubMed PubMed Central Статья CAS Google Scholar
McKinney, E. F. et al. Иммунопатология ANCA-ассоциированного васкулита. Семин. Immunopathol. 36 (4), 461–478 (2014).
CAS PubMed PubMed Central Статья Google Scholar
Berden, A. et al. Диагностика и лечение ANCA-ассоциированного васкулита. BMJ 344 , e26 (2012).
PubMed Статья Google Scholar
Kessenbrock, K. et al. Сетчатые нейтрофилы при аутоиммунном васкулите мелких сосудов. Nat. Med. 15 (6), 623–625 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Ishizu, A. et al. Прогнозирование ответа на терапию индукции ремиссии с помощью профилирования экспрессии генов периферической крови у японских пациентов с микроскопическим полиангиитом. Arthritis Res. Ther. 19 (1), 117 (2017).
PubMed PubMed Central Статья CAS Google Scholar
Yao, Y. et al. Разработка потенциальных фармакодинамических и диагностических маркеров для испытаний моноклональных антител против IFN-α при системной красной волчанке. Hum. Genomics Proteomics 2009 , 374312 (2009).
PubMed PubMed Central Google Scholar
Morand, E. F. et al. Испытание анифролюмаба при активной системной красной волчанке. N. Engl. J. Med. 382 (3), 211–221 (2020).
CAS PubMed Статья Google Scholar
Rice, G. I. et al. Оценка передачи сигналов интерферона типа I при воспалительных заболеваниях у детей. J. Clin. Иммунол. 37 (2), 123–132 (2017).
CAS PubMed Статья Google Scholar
Dominguez-Gutierrez, P. R. et al. Снижение уровней CCL2 и CXCL10 у пациентов с системной красной волчанкой, получающих лечение преднизоном, микофенолятмофетилом или гидроксихлорохином, за исключением подгруппы с высоким уровнем STAT1. Arthritis Res. Ther. 16 (1), R23 (2014).
PubMed PubMed Central Статья CAS Google Scholar
Schoggins, J. W. et al. Различные генные продукты являются эффекторами противовирусного ответа интерферона типа I. Природа 472 (7344), 481–485 (2011).
ADS CAS PubMed PubMed Central Статья Google Scholar
Li, Q. Z. et al. Экспрессия гена сигнатуры интерферона коррелирует с профилями аутоантител у пациентов с синдромами неполной волчанки. Clin. Exp. Иммунол. 159 (3), 281–291 (2010).
CAS PubMed PubMed Central Статья Google Scholar
Ян К. и Бойд Д. Д. Регулирование экспрессии гена матриксной металлопротеиназы. J. Cell Physiol. 211 (1), 19–26 (2007).
CAS PubMed Статья Google Scholar
Perron, B. et al. Может ли ферментативная активность или иначе быть выведена из структурных исследований аннексина III ?. J. Biol. Chem. 272 (17), 11321–11326 (1997).
CAS PubMed Статья Google Scholar
McKinney, E. F. et al. Истощение Т-клеток, костимуляция и клинические исходы аутоиммунитета и инфекции. Природа 523 (7562), 612–616 (2015).
ADS CAS PubMed PubMed Central Статья Google Scholar
Goupil, R. et al. Лимфопения и инфекционные осложнения, связанные с лечением ANCA-ассоциированного васкулита. Clin. Варенье. Soc. Нефрол. 8 (3), 416–423 (2013).
CAS PubMed Статья Google Scholar
Ahn, S. S. et al. Отношение нейтрофилов к лимфоцитам при постановке диагноза может оценить активность васкулита и плохой прогноз у пациентов с ANCA-ассоциированным васкулитом: ретроспективное исследование. BMC Nephrol. 19 (1), 187 (2018).
PubMed PubMed Central Статья CAS Google Scholar
Jung, J. & Jung, H. Методы анализа профилей экспрессии генов, специфичных для определенного типа клеток, в гетерогенных популяциях клеток. Anim. Cells Syst. 20 , 113–117 (2016).
CAS Статья Google Scholar
Diao, B. et al. Снижение и функциональное истощение Т-клеток у пациентов с коронавирусной болезнью 2019 (COVID-19). Фронт. Иммунол. 11 , 827 (2020).
CAS PubMed PubMed Central Статья Google Scholar
Коллинг, У. К. и др. Ответ лейкоцитов и противовоспалительные цитокины при внебольничной пневмонии. Грудь 56 (2), 121–125 (2001).
CAS PubMed PubMed Central Статья Google Scholar
Yao, Y. et al. Интерфероны I типа при синдроме Шегрена. Аутоиммун. Ред. 12 (5), 558–566 (2013).
CAS PubMed Статья Google Scholar
Bauer, J. W. et al. Интерферон-регулируемые хемокины как биомаркеры активности системной красной волчанки: валидационное исследование. Arthritis Rheum. 60 (10), 3098–3107 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Гангули Д. Связывают ли интерфероны типа I системные аутоиммунные реакции и метаболический синдром в патогенетическом континууме ?. Trends Immunol. 39 (1), 28–43 (2018).
CAS PubMed Статья PubMed Central Google Scholar
Feng, X. et al. Связь повышенной экспрессии индуцируемых интерфероном генов с активностью заболевания и волчаночным нефритом у пациентов с системной красной волчанкой. Arthritis Rheum. 54 (9), 2951–2962 (2006).
CAS PubMed Статья Google Scholar
Edvardsen, K. et al. Клетки периферической крови пациентов с аутоиммунной болезнью Аддисона плохо реагируют на интерфероны in vitro, несмотря на повышенные уровни интерферон-индуцируемых хемокинов в сыворотке крови. J. Interferon Cytokine Res. 35 (10), 759–770 (2015).
CAS PubMed PubMed Central Статья Google Scholar
Bratland, E., Hellesen, A. & Husebye, E. S. Индукция хемокина CXCL10 в адренокортикальных клетках путем стимуляции через toll-подобный рецептор 3. Мол. Клеточный эндокринол. 365 (1), 75–83 (2013).
CAS PubMed Статья Google Scholar
Antonelli, A. et al. Хемокиновый (мотив C-X-C) лиганд (CXCL) 10 при аутоиммунных заболеваниях. Autoimmun Rev. 13 (3), 272–280 (2014).
CAS PubMed Статья PubMed Central Google Scholar
Lúdvíksson, B.R. et al. Активный гранулематоз Вегенера связан с HLA-DR + CD4 + Т-клетками, проявляющими несбалансированный цитокиновый паттерн Т-клеток Th2-типа: обращение с IL-10. J. Immunol. 160 (7), 3602–3609 (1998).
PubMed Google Scholar
Lee, K. S. et al. Генетические варианты при васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами: байесовский подход и систематический обзор. J Clin Med 8 (2), 266 (2019).
CAS PubMed Central Статья PubMed Google Scholar
Monach, P. A. et al. Белки сыворотки, отражающие воспаление, повреждение и восстановление, как биомаркеры активности заболевания при ANCA-ассоциированном васкулите. Ann. Реум. Дис. 72 (8), 1342–1350 (2013).
CAS PubMed Статья Google Scholar
Stone, J.H. et al. Сравнение ритуксимаба и циклофосфамида при ANCA-ассоциированном васкулите. N. Engl. J. Med. 363 (3), 221–232 (2010).
CAS PubMed PubMed Central Статья Google Scholar
de Jong, T. D. et al. Влияние преднизона на сигнатуру интерферона I типа при ревматоидном артрите: последствия для прогнозирования ответа на ритуксимаб. Arthritis Res.Ther. 17 , 78 (2015).
PubMed PubMed Central Статья CAS Google Scholar
Уоллес, З. С. и Милославский, Э. М. Управление ANCA-ассоциированным васкулитом. BMJ 368 , m421 (2020).
PubMed Статья Google Scholar
El-Gohary, A. et al. Сывороточный и мочевой гамма-индуцируемый белок 10 при волчаночном нефрите. J. Clin. Лаборатория. Анальный. 30 (6), 1135–1138 (2016).
CAS PubMed PubMed Central Статья Google Scholar
Han, J. H. et al. Связь уровней CXCL10 и CXCL13 с активностью заболевания и кожными проявлениями при активной болезни Стилла у взрослых. Arthritis Res. Ther. 17 , 260 (2015).
PubMed PubMed Central Статья CAS Google Scholar
Gotsch, F. et al. CXCL10 / IP-10: недостающее звено между воспалением и антиангиогенезом при преэклампсии ?. J. Matern. Fetal Neonatal Med. 20 (11), 777–792 (2007).
CAS PubMed PubMed Central Статья Google Scholar
Tam, F. W. et al. Хемоаттрактантный белок-1 моноцитов мочи (МСР-1) является маркером активного почечного васкулита. Нефрол.Набирать номер. Транспл. 19 (11), 2761–2768 (2004).
CAS Статья Google Scholar
Ohlsson, S., Wieslander, J. & Segelmark, M. Профиль циркулирующих цитокинов при антинейтрофильном цитоплазматическом васкулите, ассоциированном с аутоантителами: прогноз исхода ?. Медиаторы воспаления. 13 (4), 275–283 (2004).
CAS PubMed PubMed Central Статья Google Scholar
Land, J. et al. Производство регуляторных и эффекторных цитокинов B-клеток у пациентов с рецидивирующим гранулематозом с полиангиитом. Arthritis Res. Ther. 18 , 84 (2016).
ADS PubMed PubMed Central Статья CAS Google Scholar
Torheim, E. A. et al. Повышенная экспрессия хемокинов у пациентов с гранулематозом Вегенера — модулирующие эффекты метилпреднизолона in vitro. Clin. Exp. Иммунол. 140 (2), 376–383 (2005).
CAS PubMed PubMed Central Статья Google Scholar
Yao, Y. et al. Интерферон типа I: потенциальная терапевтическая мишень для лечения псориаза ?. PLoS ONE 3 (7), e2737 (2008).
ADS PubMed PubMed Central Статья CAS Google Scholar
Романова Ю. и др. Протеомный анализ сыворотки крови пациентов с хроническим заболеванием почек. Биомолекулы 10 (2), 257 (2020).
CAS PubMed Central Статья PubMed Google Scholar
Vitali, C. et al. Критерии классификации синдрома Шегрена: пересмотренная версия европейских критериев, предложенных Американо-европейской консенсусной группой. Ann. Реум. Дис. 61 (6), 554–558 (2002).
CAS PubMed PubMed Central Статья Google Scholar
Мукака, М. М. Статистический уголок: руководство по надлежащему использованию коэффициента корреляции в медицинских исследованиях. Malawi Med. J. 24 (3), 69–71 (2012).
CAS PubMed PubMed Central Google Scholar
Акоглу Х. Руководство пользователя по коэффициентам корреляции. Тюрк. J. Emerg. Med. 18 (3), 91–93 (2018).
PubMed PubMed Central Статья Google Scholar
Perng, Y. C. & Lenschow, D. J. ISG15 в области противовирусного иммунитета и не только. Nat. Rev. Microbiol. 16 (7), 423–439 (2018).
CAS PubMed PubMed Central Статья Google Scholar
Zhang, D. & Zhang, D. E. Интерферон-стимулированный ген 15 и система IS-гилирования белка. J. Interferon Cytokine Res. 31 (1), 119–130 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Ding, Y. et al. Идентификация предиктора экспрессии гена для диагностики и индивидуальной стратификации пациентов с волчанкой. PLoS ONE 13 (7), e0198325 (2018).
PubMed PubMed Central Статья CAS Google Scholar
Akiyama, H. et al. . Интерферон-индуцируемый CD169 / Siglec1 ослабляет анти-ВИЧ-1 эффекты альфа-интерферона . J. Virol. 91 (21), e00972-17. https://doi.org/10.1128/JVI.00972-17 (2017).
Gaudet, P. et al. Филогенетическое распространение функциональных аннотаций в рамках консорциума Gene Ontology. Краткое. Биоинформ. 12 (5), 449–462 (2011).
PubMed PubMed Central Статья Google Scholar
Фитцджеральд К.А. Ген, индуцируемый интерфероном: виперин. J. Interferon Cytokine Res. 31 (1), 131–135 (2011).
CAS PubMed PubMed Central Статья Google Scholar
Ван Х., Hinson, E. R. и Cresswell, P. Интерферон-индуцируемый белок виперин ингибирует высвобождение вируса гриппа, нарушая липидные рафты. Клеточный микроб-хозяин 2 (2), 96–105 (2007).
CAS PubMed Статья Google Scholar
Nasr, N. et al. ВИЧ-1 инфекция макрофагов человека непосредственно индуцирует виперин, который подавляет производство вирусов. Кровь 120 (4), 778–788 (2012).
CAS PubMed Статья Google Scholar
Emamian, E. S. et al. Профили экспрессии генов периферической крови при синдроме Шегрена. Genes Immun. 10 (4), 285–296 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Kumar, P. et al. Ингибирование трансляции членами семейства IFIT определяется их способностью избирательно взаимодействовать с 5′-концевыми областями cap0-, cap1- и 5’ppp-мРНК. Nucl. Acids Res. 42 (5), 3228–3245 (2014).
CAS PubMed Статья Google Scholar
Фенстерл В. и Сен Г. С. Интерферон-индуцированные белки Ifit: их роль в вирусном патогенезе. J. Virol. 89 (5), 2462–2468 (2015).
PubMed Статья CAS Google Scholar
Хуанг, В.C. et al. IFI44L представляет собой новый опухолевый супрессор при гепатоцеллюлярной карциноме человека, влияющий на стволовость рака, метастазирование и устойчивость к лекарствам посредством регулирования пути передачи сигналов met / Src. BMC Рак 18 (1), 609 (2018).
PubMed PubMed Central Статья CAS Google Scholar
Björk, A. et al. Показатели на основе метилирования белков и ДНК в качестве суррогатных маркеров активации системы интерферона у пациентов с первичным синдромом Шегрена. RMD Открыть 6 , e000995 (2020).
PubMed PubMed Central Статья Google Scholar
Cheon, H. & Stark, G.R. Нефосфорилированный STAT1 продлевает экспрессию индуцированных интерфероном иммунных регуляторных генов. Proc. Natl. Акад. Sci. США 106 (23), 9373–9378 (2009).
ADS CAS PubMed PubMed Central Статья Google Scholar
Deshmane, S. L. et al. Моноцитарный хемоаттрактантный белок-1 (MCP-1): обзор. J. Interferon Cytokine Res. 29 (6), 313–326 (2009).
CAS PubMed PubMed Central Статья Google Scholar
Cuadrado, E. et al. Фенотипические вариации при синдроме Айкарди-Гутьера, объясняемые клеточно-специфическим ответом гена, стимулированным IFN, и высвобождением цитокинов. Дж.Иммунол. 194 (8), 3623–3633 (2015).
CAS PubMed Статья PubMed Central Google Scholar
Блокланд, С. Л. М., Флесса, К. М., ван Рун Дж. А. Г. и Маврагани, К. П. Новые роли хемокинов и цитокинов в качестве организаторов иммунопатологии при синдроме Шегрена . Ревматология (Оксфорд) key438. https://doi.org/10.1093/rheumatology/key438(2019).
Баларини, Г. М. и др. Кальпротектин в сыворотке крови является биомаркером атеросклероза сонных артерий у пациентов с первичным синдромом Шегрена. Clin. Exp. Ревматол. 34 (6), 1006–1012 (2016).
PubMed PubMed Central Google Scholar
Vazirinejad, R. et al. Биологические функции, структура и источники CXCL10 и его выдающаяся роль в патофизиологии рассеянного склероза. Нейроиммуномодуляция 21 (6), 322–330 (2014).
CAS PubMed Статья PubMed Central Google Scholar
Yan, Y. et al. Экспрессия CCL19 и CCR7, сигнальные пути и адъювантные функции при вирусной инфекции и профилактике. Фронт. Cell Dev. Биол. 7 , 212 (2019).
PubMed PubMed Central Статья Google Scholar
Pietilä, T. E. et al. Множественные факторы транскрипции семейства регуляторных факторов NF-kappaB и IFN регулируют экспрессию гена CCL19 в дендритных клетках, происходящих из моноцитов человека. J. Immunol. 178 (1), 253–261 (2007).
PubMed Статья PubMed Central Google Scholar
Способность к продукции IFN и здоровое старение: анализ смешанной модели 24-летнего продольного исследования в Японии
Обзор статьи
Статья в центре внимания
Определить изменения в продукции интерферона (IFN) (параметр врожденного иммунитета) в процессе старения посредством 24-летнего продольного исследования.
Создание профиля продукции IFN у здоровых людей, чтобы определить, являются ли эти изменения нормальной частью старения.
Ключевые сообщения
Широко распространено мнение, что с возрастом врожденный иммунитет постоянно снижается. Этот отчет частично соглашается с тем, что производство IFN сокращается; однако это снижение относительно более умеренное, чем часто думают.
- Способность продукции
IFN может увеличиваться после снижения даже у здоровых людей в возрасте от 50 до 60 лет.
Серьезное снижение выработки IFN больше связано с началом заболевания, чем со старением.
Сильные и слабые стороны этого исследования
Нет известных отчетов, показывающих взаимосвязь между способностью продуцировать IFN и старением.
Наши результаты основаны на продольном исследовании, которое превосходит широко используемое поперечное исследование.
Однако исследуемая популяция была не идеального размера.
Введение
Есть много сообщений, свидетельствующих о возрастном снижении иммунитета по мере взросления человека. Старение иммунной системы приводит к иммунологической восприимчивости, ведущей к инфекциям, аутоиммунным заболеваниям и злокачественным новообразованиям, что может увеличить количество госпитализаций и смертность среди пожилых людей.1–3 Хорошо известно, что иммунное старение более тяжелое для приобретенной иммунной системы, чем для врожденного. system.4-8 Некоторые исследователи сообщили о значительном снижении различных аспектов врожденной системы, таких как уменьшение фагоцитоза, изменение клеточной миграции, изменения популяции и количества клеток, связанных с врожденным иммунитетом, нарушение продукции цитокинов и фенотипических, а также функциональных изменения.3, 9, 10 Другие исследователи, однако, не согласны и сообщают лишь о незначительном снижении врожденного иммунитета.11 Напротив, широко распространено мнение о том, что аспект приобретенного иммунитета, такой как выработка специфических антител и наивных Т и В количество ячеек, резко уменьшается с возрастом 12, 13
Система интерферона человека I типа (IFN) выполняет основные функции защиты хозяина, такие как профилактика инфекций и иммунологический надзор за раком; 14 она также способствует созреванию дендритных клеток, что приводит к дифференцировке определенных Т-хелперных клеток.15–18 В результате множества ролей, которые она играет, система IFN важна для врожденной и приобретенной иммунной систем человека.19 Поэтому неудивительно, что пациенты с дефицитом ответа IFN типа I (например, stat 1 , Мутация гена TYK2 ) или дефицит продукции IFN типа I (например, мутация гена UNC93B1 ) очень чувствительны к инфекции.20, 21
В нашем исследовательском центре мы создали уникальный тест на продукцию IFN для анализа и изучения важности системы IFN для человека.22 Чтобы достичь этого, иммунологический тест в форме количественного определения IFN проводится для всех людей (больных и здоровых), которые проходят плановые медицинские осмотры в нашем исследовательском центре с 1987 года по настоящее время. Чтобы пролить свет на взаимосвязь между изменениями в продукции IFN и старением, мы взяли данные из вышеупомянутой базы данных, применили различные критерии выбора и провели всесторонний анализ данных.
Для здорового старения важно поддерживать высокий иммунитет.Следовательно, рациональное решение этого исследования состояло в том, чтобы наблюдать долгосрочную продукцию IFN в когорте людей, поскольку это хороший параметр для понимания иммунной способности и состояния здоровья людей. Если с помощью этого и других исследований будет определено, что снижение происходит даже при здоровом старении, тогда не требуется медицинского вмешательства для людей, у которых выработка IFN уменьшается с возрастом. Однако, если установлено, что снижение выработки ИФН не является функцией здорового старения, необходимо предпринять меры по устранению причины и соответствующему лечению или изменению образа жизни.
В предыдущей статье, посвященной пациентам с различными заболеваниями, мы продемонстрировали, что независимо от их возраста, пациенты с раком легких, диабетом, миелодиспластическим синдромом, прогрессирующим нефритом иммуноглобулина A (IgA), ВИЧ и гепатитом С нарушают выработку IFN-α22– 26 Кроме того, на основании записей 17-летнего последующего исследования (данные являются частью 24-летней базы данных) сравнение здоровых людей соответствующего возраста и пациентов с ВГС показало, что вероятно нарушение выработки IFN-α. связано с увеличением риска рака.25 Кроме того, мы также показали, что снижение выработки IFN-α было очевидным не только у пациентов с раком легких и ВГС, но и у пациентов, у которых развился сахарный диабет.26 Таким образом, на основании этих предыдущих результатов мы поняли, что, несмотря на причину (инфекционное заболевание, рак, нарушение обмена веществ и нефрит), многие виды заболеваний ухудшают продукцию IFN-α, и что дисфункция IFN приводит к более высокому риску инфекционных заболеваний и развития рака.
Продольные исследования сложны с материально-технической и финансовой точек зрения, особенно те, которые включают долгосрочное наблюдение за иммунным ответом.В результате было опубликовано лишь несколько сообщений, включая шведские исследования OCTO, NOVA -imun.12, 27 в Балтиморе и Хисаяме, все из которых, похоже, продолжают приносить интересные данные28–30. Многие исследователи проанализировали здоровое старение с помощью перекрестного анализа. секционные исследования, включающие сравнение молодых и пожилых людей; однако этот метод может давать необъективные данные. Элементы, влияющие на здоровое старение, такие как различия в генетике, окружающей среде, привычках питания и другом образе жизни, не рассматриваются в поперечных исследованиях.В результате перекрестные исследования предлагают лишь ограниченное понимание здорового старения. Чтобы преодолеть это ограничение, мы провели продольное исследование, которое дало превосходные результаты. В этом исследовании нашей целью было определить соотношение иммунитета и возраста у здоровых людей. Мы считаем, что результатов предыдущих поперечных исследований недостаточно, чтобы доказать широко известное убеждение, что старение отрицательно влияет на иммунную способность. По этим причинам мы решили подкрепить нашу теорию данными, полученными ретроспективно из нашей 24-летней базы данных.В этой статье мы прольем свет на изменения в продукции IFN в процессе здорового старения и рассмотрим влияние развития болезни на систему IFN.
Методы
Исследуемая популяция
Медицинские записи были получены о 2387 лицах, которые проходили медицинские осмотры в Центре медицинских исследований Луи Пастера с января 1987 года по декабрь 2010 года. Записи отдельных лиц включали данные об их выработке IFN-α в дополнение к результатам рутинных лабораторных анализов крови. .Эти люди, состоящие из здоровых людей и людей с различными заболеваниями, имели в среднем два посещения в год на человека, в общей сложности 9480 зарегистрированных посещений. Образцы крови были взяты у людей после получения письменного информированного согласия. Все люди являются постоянными членами клуба, которые поддерживают исследования Центра медицинских исследований Луи Пастера.
Статистический анализ
Первичный анализ был проведен с использованием значений продукции IFN-α для 2387 человек.Из этой когорты было отобрано 295 человек; каждый из них удовлетворял следующим условиям: (1) их продукция IFN-α была определена количественно более пяти раз и (2) у них не было в анамнезе рака, аутоиммунных или хронических инфекционных заболеваний. Их периодические логарифмически преобразованные значения IFN-α (y) были нанесены на график в зависимости от возраста (x), а затем адаптированы к линейным (y = mx + n) и квадратным формулам (y = ax 2 + bx + c) выражениям, как показано на рисунке. 1. Регрессионный анализ проводился с использованием пакета статистических программ SAS V.8.2 (SAS Institute Inc, Северная Каролина, США).
Рис. 1 Данные о продукциипродольного интерферона (IFN) α одним человеком, структура которого типична для большей части выборки. индивидуальные периодические логарифмические преобразованные значения IFN-α (y) были построены в зависимости от возраста (x) и подогнаны к (1) линейному выражению (y = mx + n) и (2) квадратичной формуле (y = ax 2 + bx + в).
Результаты первичного анализа показали, что, когда продуцирование IFN-α измерялось более 25 раз, полученные значения показали общую тенденцию к стабилизации, как показано на рисунке 2.Тенденция к отрицательному положению в линейном выражении и тенденция к положительному положению в квадратичном выражении четко прослеживается по точкам данных. Таким образом, из группы, состоящей из 295 здоровых людей, мы выбрали 33 (обозначенных как лиц, находящихся под долгосрочным наблюдением (LT)), чья продукция IFN-α была определена количественно более чем в 25 раз. Затем мы проанализировали данные, используя анализ смешанной модели с помощью статистического программного обеспечения R. Схема процесса отбора показана на рисунке 3.
Рисунок 2Распределение значения коэффициента.(A) Значение коэффициента m было нанесено на график для людей, чей интерферон (IFN) α был определен количественно более пяти раз. (B) Увеличьте распределение значений, найденных в красном овале 2a. Овал состоит из значений для людей, чей IFN был определен количественно более 25 раз. (C) Каждое значение коэффициента a было нанесено более пяти раз. (D) Увеличьте распределение значений, найденных в красном овале 2c. Овал состоит из количественного определения IFN, которое проводилось более 25 раз.
Рисунок 3Процесс отбора физических лиц.
Измерение продукции IFN в цельной крови
Метод количественного определения продукции IFN-α в цельной крови человека был описан ранее.22 Вкратце, образцы гепаринизированной периферической крови использовали в течение 8 часов после индукции IFN. Образцы культивировали с вирусом Сендай (HVJ) и инкубировали при 37 ° C в течение 20 часов. Супернатанты собирали, и активность IFN-α в супернатантах определяли с помощью биоанализа (с использованием клеток FL и вируса Синдбис), после чего определяли значение титра.Титр IFN был стандартизирован в соответствии с международным эталоном ВОЗ IFN-α MRC 69 / 19B, 95/568, а позже мы использовали японский стандарт интерферона-α (J501) с 2005 года. Они были стандартизированы с использованием международного стандарта 95/574 в течение периода исследования.
Результаты
Первичный анализ
Логарифмически преобразованное значение периодических значений IFN-α каждого человека (y) было построено в зависимости от возраста (x) и подогнано к двум выражениям квадратной формулы (y = mx + n и y = ax 2 + bx + c), как показано на рисунке 1.Продукция IFN-α у этих людей была определена в течение 9,2 ± 0,2 года и 13,4 ± 0,5 раза (среднее значение ± стандартная ошибка).
Как показано на фиг. 2A, B, коэффициент m значений линейного выражения показал, что у большего числа людей отмечалось снижение выработки IFN, когда IFN определяли количественно более чем в 25 раз. Коэффициент для каждого уровня частоты измерения IFN показал отрицательное значение, что указывает на тенденцию к снижению.
Напротив, результаты анализа квадратной формулы показали, что среднее значение коэффициента a квадратичного выражения было более положительным, чем отрицательным (рис. 2C, D).Более частая количественная оценка продукции IFN у людей привела к четкой вогнутой U-образной форме, что означает, что когда-то снижавшаяся продукция IFN у людей восстанавливалась по мере старения. Наблюдаемых различий между тенденциями к продукции IFN у мужчин и женщин не было (данные не показаны).
Анализ смешанной модели
Результаты первичного анализа показали, что после 25 измерений продукция IFN показала общую тенденцию к стабилизации. Поэтому мы выбрали 33 здоровых человека с LT, чья продукция IFN была измерена более 25 раз для анализа смешанной модели (мужчины: n = 29, женщины: n = 4).У этих 33 здоровых людей с ЛТ продукция IFN определялась количественно один или два раза в год последовательно в течение более 15 лет (среднее ± SD; 17,84 ± 0,37 года, 34,09 ± 0,87 раза) (см. Дополнительную диаграмму S1 в Интернете). Как показано в таблице 1A, результаты подбора линейной экспрессии показали, что продукция IFN у здоровых людей с LT проявляла небольшую, но статистически значимую тенденцию к снижению (p = 0,045, таблица 1). Среднее популяционное значение коэффициента значения линейного выражения составило -0,003, что указывает на то, что логарифм (значение IFN-α) снизился на 3% за 10 лет (10-25% от фактического значения).
Таблица 1Результаты анализа смешанной модели
Что касается анализа квадратичной формулы для здоровых людей с LT, результаты показали, что среднее популяции коэффициента a квадратичного выражения было положительным (вогнутая U-образная форма), показывая, что у людей с LT после снижения выработки IFN восстановилось по мере старения (это было статистически значимо, p = 0,0107, таблица 1). Возрастное распределение самых низких значений продукции IFN-α находится в диапазоне от 55 до 65 лет (диаграмма 4).
Рисунок 4Распределение людей с наименьшим возрастом продукции интерферона (IFN). Из 33 человек были отобраны 18, у которых самая низкая продукция IFN произошла в течение периода наблюдения данного исследования.
Обсуждение
В нашем 24-летнем продольном исследовании смешанный модельный анализ линейной экспрессии показал, что log (IFN-α), который является основной защитной способностью организма, незначительно снизился на 3% за 10 лет даже у здоровых людей. Это означает, например, что исходное значение IFN-α 10 000 или 5802 МЕ / мл снизилось до 7585 и 4473 МЕ / мл соответственно за 10 лет.Это снижение производства IFN было примерно вдвое меньше, чем мы ожидали. Это может быть связано с тем, что включенные в исследование лица были признаны здоровыми на основании анализов крови, которые исключили возможность рака и других хронических заболеваний. Удивительно, но результаты анализа квадратной формулы показали, что среднее значение коэффициента и квадратичного выражения было положительным (вогнутая U-образная форма), что означает, что когда-то снижавшаяся выработка IFN у людей восстанавливалась с возрастом.Это убедительно свидетельствует о том, что продукция IFN-α может увеличиваться после снижения даже у людей в возрасте от 50 до 60 лет.
Нет известных исследований о влиянии старения на систему IFN, однако в одном отчете было высказано предположение, что количество плазматических клеток, которые являются основными продуцентами IFN-α, значительно ниже у пожилых людей.31 Напротив, другой отчет заявил, что количество миелоидных дендритных клеток (ДК) снизилось у пожилых людей, но плазмацитоидные ДК в периферической крови не показали значительного снижения у пожилых людей.10 В отличие от врожденного иммунитета, где существуют противоположные взгляды, среди исследователей существует общее мнение, что наблюдается серьезное снижение приобретенного иммунитета, такого как количество наивных Т-клеток и количество наивных В-клеток, ответ антител и эффективность вакцинации. Для иммунитета серьезное снижение обычно составляет от половины до двух третей исходной функции, в то время как для приобретенного иммунитета серьезное снижение обычно составляет девять десятых снижения иммунной функции.
Как было указано ранее, результаты анализа квадратичной формулы у здоровых людей с LT показали, что среднее популяции коэффициента a квадратичного выражения было положительным (вогнутый U-образный паттерн), что означает, что у LT-индивидуумов был положительный результат. снижение выработки IFN восстанавливалось по мере их старения.Это открытие очень важно, поскольку широко распространено мнение, что иммунное старение можно обратить вспять только в том случае, если заболевание, вызвавшее снижение иммунной способности, успешно вылечено. В нашей предыдущей статье мы продемонстрировали, что выздоровление от туберкулеза легких или успешная терапия против ВИЧ увеличивают продукцию IFN-α22 (частично неопубликованные данные). Хотя сообщалось, что некоторые цитокины демонстрируют повышенную продукцию у пожилых людей, они, как правило, являются иммуносупрессивными или воспалительными цитокинами32,33 Таким образом, хотя многие реакции врожденной иммунной системы ослабевают с возрастом, имеются существенные доказательства возрастной гиперреактивности врожденный иммунитет.
Мы заметили, что самая низкая продукция IFN-α наблюдается у людей в возрасте от 55 до 65 лет. Почему на данном этапе продукция IFN-α самая низкая? Подавляющее большинство участников этого исследования — это руководители среднего класса или частные предприниматели, которые особенно заботятся о своем здоровье и поэтому дважды в год посещают наш Институт для проверки здоровья. В Японии средний возраст выхода на пенсию составляет от 60 до 65 лет, и мы предполагаем, что эта важная веха может быть причиной повышенного стресса и беспокойства, что приводит к падению производства IFN-α.Японское исследование Осаки, в котором приняли участие около 50000 взрослых в возрасте 40 лет и старше, проживающих в городе Осаки, префектура Мияги, продемонстрировало, что уровни психологического стресса (с использованием K6, инструмента из шести пунктов для оценки неспецифического психологического стресса, разработанного Кесслером) показали четкую U-образную кривую, при этом самые низкие уровни стресса приходятся на возраст 60–69 лет34. Наше исследование отражает этот результат; Самая низкая продукция IFN-α произошла в возрасте от 55 до 65 лет, и в этот период началось выздоровление, которое, как мы связали, снижает уровень стресса.Хотя большинство отчетов, свидетельствующих об улучшении здоровья после выхода на пенсию, датированы, недавний отчет предполагает, что снижение нагрузки на предыдущую работу после выхода на пенсию может привести к улучшению здоровья, особенно у некоторых людей, у которых была стрессовая работа35, 36 Кроме того, исследование с использованием профессиональной когорты французской ГАЗЕЛЬ также пришел к выводу, что выход на пенсию был связан со значительным снижением умственной и физической усталости, а также депрессивных симптомов.25, 37
Это первое известное исследование с использованием продольного подхода, демонстрирующее, что способность продуцировать IFN-α может восстанавливаться у людей среднего возраста.Мы считаем эти результаты обнадеживающими, поскольку они предполагают, что если у среднего здорового человека наблюдается снижение выработки IFN-α, выздоровление возможно с изменением образа жизни, которое включает значительное снижение стресса.
Наши ранее опубликованные результаты показали, что у пациентов с раком легких, диабетом, миелодиспластическим синдромом, распространенным IgA-нефритом, ВИЧ и гепатитом С независимо от причины заболевания наблюдается нарушение продукции IFN-α.22, 25 Кроме того, мы показали, что IFN-α продукция постепенно снижалась не только с развитием ВГС, но и с повышением уровня сахара в плазме крови.25, 26 Эти результаты в сочетании с нашими настоящими результатами подтверждают наш вывод о том, что тяжелая дисфункция IFN возникает не из-за старения, а из-за возникновения различных типов заболеваний (инфекционных заболеваний, рака, нарушений обмена веществ и нефрита). Основываясь на этих выводах, мы предлагаем периодическую оценку и количественную оценку продукции IFN-α для выявления изменений в системе IFN, чтобы определить, стареют ли люди здоровым, подвержены ли заболеваниям или находятся ли они на ранней стадии начала заболевания.Используя эту информацию, можно рекомендовать лечение или изменения в образе жизни, которые могут привести к восстановлению выработки IFN-α и улучшению здоровья человека.
Сильные стороны и ограничения
Одна из основных сильных сторон этого отчета заключается в том, что это 24-летнее продольное исследование по сравнению с поперечным исследованием. Ограничения перекрестных обследований состоят в том, что они предоставляют данные только за определенный или единственный момент времени и, следовательно, не могут выявить каких-либо значимых изменений в выборке из года в год.Поскольку исследование старения должно отслеживать изменения в популяции с течением времени, перекрестное обследование не сможет точно отразить фактический статус. Напротив, лонгитюдные исследования предназначены для отслеживания изменений в данной популяции в течение определенного периода времени, и поэтому тенденции можно наблюдать, сравнивая данные, полученные в отдельные годы. Наше лонгитюдное исследование позволило нам многократно измерить одну и ту же популяцию в течение 24 лет, что дало более надежные данные.
Несмотря на то, что в 33 года наша выборка несколько мала, те же результаты можно было увидеть в нашей выборке из 295 человек, чей IFN был определен количественно более пяти раз (среднее значение 9.2 ± 0,2 года и в среднем 13,4 ± 0,5 раза). Другое ограничение состоит в том, что, хотя мы предположили, что стресс перед выходом на пенсию был причиной самой низкой выработки IFN-α у людей в возрасте от 55 до 65 лет, у нас нет достоверных данных, чтобы показать причинно-следственную связь. Поэтому мы полагались на выводы предыдущих отчетов и наши знания о том, что пенсионеры в этой возрастной группе обычно являются руководителями высшего звена с обязанностями, которые влекут за собой большой стресс. Это может частично объяснить, почему продукция IFN-α восстанавливалась, когда люди были в возрасте от 60 до 65 лет, что отражает период после выхода на пенсию.
Будущее направление / дальнейшие исследования
В этом отчете анализировались только здоровые люди. У нас также есть данные о больных раком, которые прошли курс лечения после теста на ИФН или у которых был диагностирован рак в период количественной оценки их ИФН. Мы полагаем, что дальнейший анализ может выявить структуру продукции IFN-α, которая различается у здоровых людей и людей с заболеваниями.
Благодарности
Мы благодарим всех людей, которые сделали это исследование возможным благодаря их долгосрочному доверию к нашему Институту и их решению использовать нас в качестве основного выбора для медицинских услуг.Мы выражаем благодарность исследовательскому и административному персоналу Центра медицинских исследований Луи Пастера за их помощь в этом проекте. Особая благодарность д-ру Т. Кишиде (скончавшемуся в 2006 г.) и д-ру Дж. Сетогучи за тщательное клиническое наблюдение на начальном этапе исследования. Мы благодарны г-же Л. Рассел за существенное редактирование этой рукописи.
.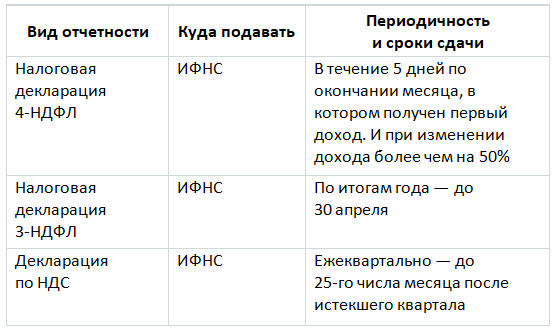 От него зависит ставка взносов на травматизм за сотрудников. Читайте в статье, как заполнить подтверждение.
От него зависит ставка взносов на травматизм за сотрудников. Читайте в статье, как заполнить подтверждение.
Об авторе