Руководство по качеству пример: Пример Руководства по качеству ИСО
Руководство по качеству по новым требованиям ИСО 9001-2015
Содержание:
- Новая версия и новые правила стандарта.
- Функции руководства по качеству ИСО, по новым требованиям ИСО 9001 2015.
- Пример руководства по качеству ИСО 9001 2015.
Последние изменения в стандарте упростили задачи разработчиков и ответственных за систему менеджмента качества на предприятиях даже со специфической деятельностью. Меньше правил относительно документирования, больше возможностей для учета индивидуальных особенностей. Изменения затронули и руководство по качеству ИСО, по новым требованиям ИСО 9001 2015 его упразднили. Однако специалисты не спешат забывать о нем, ведь он может быть полезным для предприятия и СМК.
Функции руководства по качеству ИСО, по новым требованиям ИСО 9001 2015
До новой редакции было обязательным и одним из главных документов для разработки и внедрения систем менеджмента качества, а также их дальнейшей работы и развития. Документ охватывал всю СМК: от структуры до ответственного персонала. Он был первым при знакомстве с системой и в решении вопросов после введения в курс дела. В руководстве отображались цели для определенного промежутка времени, которые ставились перед предприятием в области качества. Для их достижения прописывались процедуры и ссылки для инструкций.
Документ охватывал всю СМК: от структуры до ответственного персонала. Он был первым при знакомстве с системой и в решении вопросов после введения в курс дела. В руководстве отображались цели для определенного промежутка времени, которые ставились перед предприятием в области качества. Для их достижения прописывались процедуры и ссылки для инструкций.
Важно: Согласно п. 7.5.1 обновленной редакции стандарта от 2015 года предприятие может использовать и создавать ту документацию для СМК, которую считает нужной.
Отмена руководства не избавила от необходимости в подобном документе. Просто теперь его создают по собственным правилам с учетом требований стандартов. Как сделать наглядной структуру СМК? Как быстро узнать ответственных за тот или иной процесс? Где найти инструкцию? Общий план СМК с краткими инструкциями — так можно охарактеризовать руководство по качеству ИСО 9001 2015. Для средних и крупных компаний оно поможет упорядочить систему и быстро разобраться с документацией.
Пример руководства по качеству ИСО 9001 2015
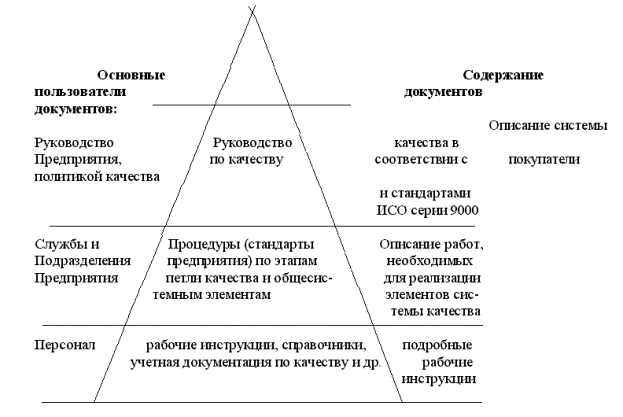
Главное требование к созданию этого документа — отобразить только важную информацию. На практике руководство чаще всего получается объемным, и загружать его дополнительно нет смысла. Вот основная информация, которую должен содержать документ:
- цели в области качества;
- структура СМК;
- требования стандарта, их реализация;
- ответственные лица;
- ссылки на локальные инструкции и т. д.
Требования стандарта удобно использовать в виде содержания руководства. То есть каждый пункт будет соответствовать отдельному требованию, а в теле документа нужно расписать их методы и правила исполнения. Не стоит использовать шаблоны или примеры других компаний — это бессмысленная работа, только индивидуальный подход и учет контекста организации. По такому же принципу работает «Стандарт качества», и наши заказчики получают подготовленный комплект документации для внедрения СМК на своем предприятии.
Руководство по качеству в аптеках
Руководство по качеству в аптеках — готовый шаблон на МедИнфо24скидка 15%
- Описание
- Отзывы
- Доставка документов
- Документ разработан на основании Правил надлежащей аптечной практики лекарственных препаратов для медицинского применения (Приказ Министерства здравоохранения РФ №647н от 31 августа 2016г.), и Правил надлежащей практики хранения и перевозки лекарственных препаратов для медицинского применения (Приказ Министерства здравоохранения РФ №646н от 31 августа 2016г.
 ).
). - Содержит описание и примеры системы качества, определяющей направления развития компании в сфере розничной торговли лекарственными препаратами, структуры документации системы, описание основных и вспомогательных процессов, стандартных операционных процедур (СОП для аптек), документированных процедур, методических и рабочих инструкций, влияющих на обеспечение высокого качества предоставляемых фармацевтических услуг в области розничной торговли лекарственными препаратами.
- Руководство по качеству направлено на наиболее полное удовлетворение потребности населения в обеспечении качественными, эффективными и безопасными лекарственными препаратами, медицинскими изделиями, биологически- активными добавками и прочими товарами аптечного ассортимента, а также предотвращения риска проникновения фальсифицированных лекарственных препаратов в розничную аптечную сеть.
- Устанавливает ответственность руководства за обеспечение соответствия системы качества Правилам надлежащей аптечной практики лекарственных препаратов для медицинского применения и Политике в области качества.

- Руководство по качеству в аптеке или выписки из него обязательны к применению для всего персонала и подразделений компании, прямо или косвенно принимающих участие в работе розничной аптечной сети.
- Руководство поддерживается в актуальном состоянии в соответствии с распределением ответственности в системе качества.
- Документ вляется собственностью компании, может предъявляться для изучения органам государственной власти, органам по сертификации и аккредитации и другим контролирующим сторонам только по согласованию с руководителем компании.
Система качества в аптеке
Система управления качеством в аптеке устанавливает общие требования к процессам по всем видам деятельности и документации, влияющих на качество услуг, оказываемых аптечными организациями, входящими в розничную аптечную сеть компании.
Основными целями в деятельности подразделения аптечной организации являются:
- поддержание сбалансированного ассортимента товаров аптечного ассортимента, в том числе минимального ассортимента лекарственных препаратов и товаров разных ценовых категорий;
- организация процесса закупки товаров аптечного ассортимента с учетом критериев отбора и оценки поставщиков товара;
- организация приемочного контроля товаров аптечного ассортимента в строгом соответствии с действующим законодательством;
- организация хранения товара в соответствии с Правилами надлежащей практики хранения и перевозки лекарственных препаратов для медицинского применения;
- организация работы по выявлению продукции ненадлежащего качества, в том числе по информационным письмам ФС Росздравнадзора и ФС Роспотребнадзора, своевременная изоляция продукции ненадлежащего качества;
- реализация в аптечных организациях лекарственных препаратов рецептурного отпуска в строгом соответствии с правилами отпуска рецептурных препаратов; а также лекарственных препаратов безрецептурного отпуска и прочих товаров аптечного ассортимента;
- фармацевтическое консультирование покупателей о правилах хранения и применения лекарственных препаратов, о наличии и цене лекарственного препарата, в том числе лекарственных препаратах нижнего ценового сегмента;
- оказание консультационных услуг в подборе лекарственных препаратов в случаях ответственного самолечения;
- повышение квалификации фармацевтических работников;
- соблюдение нормативных требований к инфраструктуре аптечных организаций;
- соблюдение санитарно-гигиенического контроля помещений и контроля личной гигиены персонала.

Для достижения этих целей необходимо решить задачи, важнейшими из которых являются:
- разработка и внедрение образцов документов системы качества в аптеке
- повышение уровня управляемости аптечными организациями компании за счет разработки и внедрения системы качества;
- регламентация процессов (подпроцессов) в подразделениях компании, которые прямо или косвенно влияют на работу аптечных организаций РАС;
- автоматизация основных технологических процессов деятельности РАС и аптечных организаций;
- автоматизация управленческой деятельности в области контроля за работой системой качества.
Электронная доставка на e-mail
Доставка документов осуществялется в электронном виде сразу после подтверждения оплаты на Ваш e-mail, который указан при заполнении карточки заказа.
ВНИМАНИЕ!!! Проверяйте папку «Спам», если не получили от нас письмо.
По всем возникающим вопросам обращайтесь в службу поддержки:
тел +7904 866 01 00 (Whatsapp )
e-mail: [email protected]
Сопутствующие документы
Пакет: Все журналы аптечной деятельности1 950 руб Подробнее
Журнал лабораторно-фасовочный150 руб Подробнее
Журнал предметно-количественного учета (ПКУ)300 руб Подробнее
Комплект документов Стандартные операционные процедуры (СОП)»12 810 руб Подробнее
Рекомендуем
СОП «Порядок организации работ по обороту маркированных лекарственных препаратов» для аптек1 275 руб Подробнее
Холодовая цепь в аптеке: Сборник документов по «холодовой цепи» из пакета НАП700 руб Подробнее
Аналогичные документы
Приказ «Об организации контроля качества товаров»300 руб Подробнее
Положение по проведению оценки деятельности надлежащей аптечной практики1 000 руб Подробнее
Приказ «О разработке и внедрении системы качества в аптеке (фармацевтической организации)»300 руб Подробнее
Документированная процедура «Управление документацией» для аптек500 руб Подробнее
Документированная процедура «Управление записями» для аптек500 руб Подробнее
Инструкция «Комплекс мер, направленных на минимизацию риска контаминации лекарственных препаратов» для аптек500 руб Подробнее
Инструкция по проведению первичного (вводного) и повторного инструктажа в аптечной организации500 руб Подробнее
Надлежащая аптечная практика + все журналы для аптек19 500 руб Подробнее
Комплект документов Стандартные операционные процедуры (СОП)»12 810 руб Подробнее
Документ добавлен в избранное Посмотреть
Документ удален из избранного
Руководство по качеству ISO 9001 | ASQ
- Дом /
- Качественные ресурсы /
- Руководство по качеству ISO 9001
Пример руководства по обеспечению качества
, автор Graeme C. Payne
Payne
СКАЧАТЬ:
Формат .doc — Формат .pdf — Формат .odt
Ниже приводится введение в пример руководства по качеству для «Мифической истинной метрологии». Цель состоит в том, чтобы представить и описать пример руководства, а также обсудить некоторые концепции, рассматриваемые в руководстве. Однако это не подробное обсуждение конкретных пунктов данного стандарта соответствия.
Обзор
Образец руководства по качеству (QM) предназначен для обслуживающей организации, желающей продемонстрировать соответствие требованиям ANSI/ISO/ASQ Q9001-2008 Американский национальный стандарт: Системы менеджмента качества. Требования . 1 Пример руководства также демонстрирует, что одно руководство может использоваться для демонстрации соответствия ряду дополнительных требований, таких как правительственные постановления. Нет необходимости иметь отдельный QM для каждого, но желательно иметь матрицу, показывающую, как QM отвечает каждому набору требований. В данном случае пример QM предназначен для воображаемой авиакомпании США, поэтому рассматриваются некоторые пункты Федеральных авиационных правил.
В данном случае пример QM предназначен для воображаемой авиакомпании США, поэтому рассматриваются некоторые пункты Федеральных авиационных правил.
Примеры других различных областей, которые могут быть затронуты в QM, включают здоровье и безопасность, экологические проблемы, финансовый учет, корпоративную этику, основные требования клиентов и многое другое. Идея состоит в том, что «руководство по качеству» не должно быть статичным документом, который видят только в отделе «качества», — это должно быть динамичное руководство по эксплуатации бизнеса, описывающее, «как мы ведем бизнес» во всех подразделениях вашей организации.
Описанная компания и местонахождение являются полностью вымышленными, как и организация вымышленной компании.
Цифровые подписи
На титульном листе QM вы увидите ссылку на цифровую подпись. В примере руководства на самом деле нет цифровой подписи, но ее можно легко применить. Цифровая подпись — это не печатная версия имени человека и не изображение подписи человека. Настоящая цифровая подпись, использующая компьютерный метод, называемый шифрованием с открытым ключом, представляет собой код, который невидимо внедряется в документ. Альтернативными названиями являются криптография с открытым ключом или шифрование RSA (которое определено в QM). Цифровая подпись, созданная с помощью этого метода, состоит из двух частей: «закрытый» ключ, известный только пользователю, и «открытый» ключ, доступный всему миру. При использовании в качестве подписи документ «подписывается» с использованием закрытого ключа подписавшего. Подпись может быть проверена любым, у кого есть открытый ключ подписавшего. Это служит двум целям. Во-первых, он аутентифицирует человека, подписавшего документ, поскольку закрытый ключ есть только у этого человека. Во-вторых, он аутентифицирует документ, поскольку, если какая-либо часть документа была изменена с момента его подписания, проверка завершится неудачей. Таким образом, цифровая подпись доказывает, что ни подпись, ни документ не подделаны и не изменены.
Настоящая цифровая подпись, использующая компьютерный метод, называемый шифрованием с открытым ключом, представляет собой код, который невидимо внедряется в документ. Альтернативными названиями являются криптография с открытым ключом или шифрование RSA (которое определено в QM). Цифровая подпись, созданная с помощью этого метода, состоит из двух частей: «закрытый» ключ, известный только пользователю, и «открытый» ключ, доступный всему миру. При использовании в качестве подписи документ «подписывается» с использованием закрытого ключа подписавшего. Подпись может быть проверена любым, у кого есть открытый ключ подписавшего. Это служит двум целям. Во-первых, он аутентифицирует человека, подписавшего документ, поскольку закрытый ключ есть только у этого человека. Во-вторых, он аутентифицирует документ, поскольку, если какая-либо часть документа была изменена с момента его подписания, проверка завершится неудачей. Таким образом, цифровая подпись доказывает, что ни подпись, ни документ не подделаны и не изменены. Напечатанные имена и графические изображения тоже не годятся, как и чернила на бумаге.
Напечатанные имена и графические изображения тоже не годятся, как и чернила на бумаге.
Контролируемые копии
Степень контроля копий УК и других документов в системе качества варьируется от одной организации к другой. Если документы электронные, контроль может быть значительно упрощен при условии, что каждый, кто в нем нуждается, имеет доступ к компьютерной системе, где и когда это необходимо. Как показано в этом руководстве, любая печатная копия не контролируется, и любая электронная копия, которая не находится на главном файловом сервере организации, не контролируется. На основном файловом сервере, разумеется, должна быть только одна копия текущей версии. Когда ваши люди имеют доступ к QM и другим документам в компьютерной системе, потребность в печатных документах снижается. Это упрощает контроль документов и снижает количество потребляемой бумаги.
Контроль версий на уровне страниц
С электронным документом, таким как этот, нет необходимости в старомодном контроле версий на уровне страниц. В системе ISO 9000 также нет требований к управлению на уровне страниц. В этом примере весь QM представляет собой единый документ. По характеру электронных документов, если где-либо в нем изменяется один символ, то изменяется весь документ. Кроме того, понятие «страница» зависит от формата публикации. Пример QM был подготовлен в Соединенных Штатах с использованием OpenOffice.org Writer и для бумаги стандартного формата Letter (216 x 279).мм). Во всем мире он обычно был бы подготовлен для бумаги формата A4 (210 x 297 мм), что изменило бы места разделения страниц. Если документ сохраняется в виде HTML-файла (для использования на веб-странице), то потенциально это может быть один экран с непрерывной прокруткой без разрывов страниц. Если документ сохранен как двоичный объект в базе данных, случайные разделы могут быть извлечены и отображены в любом формате. Следовательно, контроль версий должен осуществляться на уровне документа, а не на уровне «страницы», потому что «страницы» могут не существовать.
В системе ISO 9000 также нет требований к управлению на уровне страниц. В этом примере весь QM представляет собой единый документ. По характеру электронных документов, если где-либо в нем изменяется один символ, то изменяется весь документ. Кроме того, понятие «страница» зависит от формата публикации. Пример QM был подготовлен в Соединенных Штатах с использованием OpenOffice.org Writer и для бумаги стандартного формата Letter (216 x 279).мм). Во всем мире он обычно был бы подготовлен для бумаги формата A4 (210 x 297 мм), что изменило бы места разделения страниц. Если документ сохраняется в виде HTML-файла (для использования на веб-странице), то потенциально это может быть один экран с непрерывной прокруткой без разрывов страниц. Если документ сохранен как двоичный объект в базе данных, случайные разделы могут быть извлечены и отображены в любом формате. Следовательно, контроль версий должен осуществляться на уровне документа, а не на уровне «страницы», потому что «страницы» могут не существовать.
Тем не менее настоятельно рекомендуется, чтобы QM и другие контролируемые документы были опубликованы как защищенные от несанкционированного доступа документы с возможностью поиска. Никогда не рекомендуется делать изменяемые документы доступными для людей, которым не нужно их изменять. Формат переносимых документов (ISO 32000-1, Управление документами — Формат переносимых документов — Часть 1: PDF 1.7 ) — хороший выбор. Программные инструменты для формата PDF доступны для большинства компьютерных операционных систем, поэтому пользователи не ограничены конкретными платформами. Формат PDF также имеет другие преимущества, включая безопасность, защиту от несанкционированного доступа, возможность поиска, индексирование и многое другое.
Организация руководства по качеству
Не требуется, чтобы руководство по качеству отражало стандарт соответствия. Если МК используется для демонстрации соответствия ряду требований, это невозможно сделать в рамках одного МК. Руководство должно быть организовано таким образом, чтобы это подходило для вашей организации, потому что именно ваши сотрудники используют его каждый день. Простая матрица может использоваться для ссылки частей УК на требования стандартов соответствия.
Руководство должно быть организовано таким образом, чтобы это подходило для вашей организации, потому что именно ваши сотрудники используют его каждый день. Простая матрица может использоваться для ссылки частей УК на требования стандартов соответствия.
Определения
Любые термины, характерные для вашей компании или отрасли и используемые в QM, всегда должны быть определены в QM. Никогда не думайте, что «все знают», что имеется в виду — ваш следующий аудитор может прийти не из вашей отрасли. Например, рассмотрим аббревиатуру «СММ». Это может быть координатно-измерительная машина, модель зрелости возможностей, руководство по контролируемому техническому обслуживанию, метод сопоставления цветов, шахтный метан и многое другое, в зависимости от конкретной отрасли. Внимательные читатели обнаружат по крайней мере одну аббревиатуру в примере QM, которая не определена: MRO, что в данном случае означает техническое обслуживание, ремонт и капитальный ремонт.
Область применения системы менеджмента качества
Если вся организация работает в соответствии с установленной системой управления качеством (СМК), то нет необходимости специально определять область применения. Если СМК применяется только к части организации, то область применения должна быть четко указана. В примере QM только метрологический отдел организации охвачен СМК; предполагается, что остальная часть организации не имеет системы, соответствующей ISO 9001. В примере QM область применения определена в разделе 2.7.
Если СМК применяется только к части организации, то область применения должна быть четко указана. В примере QM только метрологический отдел организации охвачен СМК; предполагается, что остальная часть организации не имеет системы, соответствующей ISO 9001. В примере QM область применения определена в разделе 2.7.
Размер Руководства по качеству
С тех пор, как был выпущен ISO 9001:2000, было много дискуссий о том, насколько большим или маленьким должен быть QM. На самом деле, это должен быть размер, который «в самый раз» для вашей организации. Не пытайтесь втиснуть его в произвольное (небольшое) количество страниц, но и не будьте слишком многословны. QM должен представлять собой общий обзор того, как организация работает и ведет бизнес. Политики, процедуры, рабочие инструкции, конфиденциальная информация и т. п. принадлежат отдельным документам. Хотя QM необходимо регулярно пересматривать, если пункт или раздел меняется каждый раз, то эта часть может быть кандидатом на выделение в отдельный документ.
Решая, что входит в QM, помните о двух основных фазах аудита. Во-первых, ваш QM оценивается на соответствие стандарту(ам) соответствия, чтобы убедиться, что все требования выполнены удовлетворительно. Затем операции и записи вашей организации сравниваются с вашим QM, чтобы убедиться, что вы делаете то, о чем говорите. На второй фазе все, что есть в вашем QM, представляет собой достойную игру для одитора.
Ссылки на другие документы в СМК
Одним из преимуществ электронных документов является то, что в документ могут быть встроены ссылки на другие документы любого типа. В примере QM ссылки представлены синим подчеркнутым текстом, но они смоделированы. В вашем реальном документе каждая ссылка будет фактически указывать на реальный документ на вашем файловом сервере.
Эта возможность упрощает управление документами. При условии, что «живая» текущая версия всегда имеет одно и то же имя файла, вам не нужно менять ссылки в QM. Таким образом, всякий раз, когда кто-то нажимает на ссылку, он всегда — и только — видит текущую версию документа, на который указывает ссылка. Старую версию можно сохранить под другим именем; самый простой способ сделать это — просто добавить дату редакции в формате ISO 8601 2 к имени файла. Например, предположим, что процедура QP 7600 с датой пересмотра 10 ноября 2005 г. заменяется новой версией, пересмотренной сегодня. Старая версия будет переименована с «QP 7600.pdf» на «QP 7600 20051110.pdf», а новая будет сохранена как «QP 7600.pdf». Ссылки менять не нужно, а дата, добавленная к имени файла старой версии, однозначно идентифицирует его.
Старую версию можно сохранить под другим именем; самый простой способ сделать это — просто добавить дату редакции в формате ISO 8601 2 к имени файла. Например, предположим, что процедура QP 7600 с датой пересмотра 10 ноября 2005 г. заменяется новой версией, пересмотренной сегодня. Старая версия будет переименована с «QP 7600.pdf» на «QP 7600 20051110.pdf», а новая будет сохранена как «QP 7600.pdf». Ссылки менять не нужно, а дата, добавленная к имени файла старой версии, однозначно идентифицирует его.
Читатели Sharp также заметят, что версия формата даты ISO 8601 появляется в ряде мест в примере QM. Дата всегда записывается с наибольшей единицей времени (год) слева и наименьшей единицей времени (день месяца для дат) справа. Одним из преимуществ является то, что формат однозначен и не зависит от культуры. Во-вторых, дата в этом формате (как часть имени файла) всегда сортируется компьютером в правильном порядке.
Допустимые исключения
Некоторые пункты ISO 9001 могут быть исключены из СМК, если они не применяются. Наиболее распространенным допустимым исключением является пункт 7.3 «Проектирование и разработка». Однако, как правило, не рекомендуется просто опускать исключенные части из QM. Гораздо лучше включить ссылку на них, конкретно указать, что они исключены и почему, и какие планы, если текущая ситуация когда-либо изменится. Раздел 7.3 примера QM демонстрирует это.
Наиболее распространенным допустимым исключением является пункт 7.3 «Проектирование и разработка». Однако, как правило, не рекомендуется просто опускать исключенные части из QM. Гораздо лучше включить ссылку на них, конкретно указать, что они исключены и почему, и какие планы, если текущая ситуация когда-либо изменится. Раздел 7.3 примера QM демонстрирует это.
Функции, выполняемые другими
В некоторых случаях, например, в примере QM, область применения QMS настолько четко определена, что функции, обычно являющиеся частью QMS, на самом деле выполняются подразделениями организации, которые не входят в определенную QMS. В случае Mythical True Value Metrology покупка является примером этого. Метрологическая организация имеет ограниченные полномочия только в отношении небольших закупок; все остальные должны проходить через отдел корпоративных закупок, не входящий в состав СМК. В таких случаях организация должна сделать две вещи. Во-первых, QM должен описать, что они могут сделать, включая ограничения на это. В УК также должно быть указано, что другие части головной организации – части, находящиеся за пределами определенной СМК – рассматриваются как поставщики или заказчики, в зависимости от ситуации. Это показано в разделе 7.4 примера QM. В такой ситуации также важно, чтобы головная организация была в списке утвержденных поставщиков! В примере системы компания Mythical True Value Metrology должна быть уверена, что Mythical Airlines находится в утвержденном списке поставщиков соответствующих услуг и продуктов. (Обратите внимание, что Mythical Airlines также имеет рейтинг 9.0024 клиент Mythical True Value Metrology.)
В УК также должно быть указано, что другие части головной организации – части, находящиеся за пределами определенной СМК – рассматриваются как поставщики или заказчики, в зависимости от ситуации. Это показано в разделе 7.4 примера QM. В такой ситуации также важно, чтобы головная организация была в списке утвержденных поставщиков! В примере системы компания Mythical True Value Metrology должна быть уверена, что Mythical Airlines находится в утвержденном списке поставщиков соответствующих услуг и продуктов. (Обратите внимание, что Mythical Airlines также имеет рейтинг 9.0024 клиент Mythical True Value Metrology.)
Прослеживаемость
В разделе 7.5.3 говорится о «прослеживаемости». Имея дело с калибровочной организацией, важно всегда проводить четкое различие между двумя наиболее распространенными и неправильно используемыми значениями этого термина. Как используется в 7.5.3 примера QM, «прослеживаемость» относится к физической прослеживаемости физического продукта: возможность взять деталь или сборку и однозначно определить ее конечное физическое происхождение. Во многих отраслях, таких как авиация, это важно для предотвращения использования некачественных контрафактных деталей в процессе производства или обслуживания. Как используется метрологическими (калибровочными) организациями и в разделе 7.6, «прослеживаемость» относится к прослеживаемости измерений: возможность документировать неопределенность результата измерения относительно соответствующей единицы измерения в Международной системе единиц. Это схожие понятия, но в первом случае прослеживаемость относится к происхождению физического предмета, а во втором — к документально подтвержденной неопределенности результата измерения — числа.
Во многих отраслях, таких как авиация, это важно для предотвращения использования некачественных контрафактных деталей в процессе производства или обслуживания. Как используется метрологическими (калибровочными) организациями и в разделе 7.6, «прослеживаемость» относится к прослеживаемости измерений: возможность документировать неопределенность результата измерения относительно соответствующей единицы измерения в Международной системе единиц. Это схожие понятия, но в первом случае прослеживаемость относится к происхождению физического предмета, а во втором — к документально подтвержденной неопределенности результата измерения — числа.
Соответствие другим требованиям
Пример QM предназначен для организации, которая (гипотетически) зарегистрирована в соответствии с ISO 9001 и также работает в регулируемой отрасли. Это означает, что в некоторых случаях может потребоваться рассмотрение нормативных требований в УК. Раздел 7.6.1 является примером этого. Конкретное нормативное требование было добавлено в QM в логическом месте. То же самое можно сделать и для других требований — добавить их в QM в том месте, где это имеет смысл в организации руководства. Например, если соответствие Сарбейнса-Оксли является требованием, логичным местом для его добавления может быть раздел «Обязанности руководства» вашего QM.
То же самое можно сделать и для других требований — добавить их в QM в том месте, где это имеет смысл в организации руководства. Например, если соответствие Сарбейнса-Оксли является требованием, логичным местом для его добавления может быть раздел «Обязанности руководства» вашего QM.
Заключение
Образец руководства по качеству для Mythical True Value Metrology, предоставляющей услуги организации, представлен в качестве примера и учебного пособия. Он демонстрирует несколько проблем системы менеджмента качества, особенно проблемы, которые могут возникнуть в регулируемой отрасли или в небольшом отделе, зарегистрированном отдельно от остальной части головной организации. Хотя это написано, чтобы продемонстрировать, как организация соответствует требованиям ISO 9001, концепция может быть расширена до любого требования соответствия или соответствия или просто как признанная передовая деловая практика.
1 Этот стандарт является юридическим эквивалентом международного стандарта ISO 9001:2008 в США.
2 ISO 8601, Элементы данных и форматы обмена – Обмен информацией – Представление даты и времени . Текущая версия датирована 2004 годом. Обзор и объяснение стандарта доступны по адресу http://www.iso.org/iso/date_and_time_format
Graeme C. Payne — президент GK Systems, консалтинговой фирмы, специализирующейся на измерении наука. Он является автором Справочник по метрологии (ASQ Quality Press, 2004 г.) и в прошлом возглавлял отдел качества измерений ASQ. Пейн является старшим членом ASQ, сертифицированным специалистом по качеству, специалистом по калибровке, инженером по качеству и аудитором по качеству.
Избранные рекламодатели
ISO 9001:2015 Руководство по качеству | Что такое Руководство по качеству?
В чем разница между руководством по качеству и планами качества? Если вы отвечаете за внедрение системы управления качеством в своей компании или отделе, очень важно, чтобы вы понимали разницу между руководством по качеству и планом качества. Хотя эти документы идут рука об руку в управлении качеством организации, они влекут за собой разные вещи.
Хотя эти документы идут рука об руку в управлении качеством организации, они влекут за собой разные вещи.
Руководства по системе менеджмента качества представляют собой наборы документов, используемых для четкого определения и информирования о системе менеджмента качества компании. Эти ресурсы служат основой для удовлетворения требований системы качества и выражают приверженность бизнеса этой системе.
Руководства по СМК содержат все следующие записи:
Заявление о политике в области качества: В этом документе подробно описывается уровень приверженности организации поддержанию качества.
Политика качества: Политика качества подробно описывает планы компании и включает обширную документацию.
Стандартные операционные процедуры: Эти процедуры определяют стороны, ответственные за выполнение каждого вида деятельности, и отведенные им временные рамки.
Рабочие инструкции: Рабочие инструкции выделяют действия и процедуры, которые должны произойти.
Планы качестваПланы качества включают набор документов, определяющих стандарты качества системы менеджмента качества, ресурсы, спецификации, методы и все последовательности действий, относящиеся к конкретному проекту, продукту или услуге. Их цель состоит в том, чтобы определить все организационные требования, которые должны быть установлены для производства продукта или услуги, как предполагалось.
В планах качества описываются все процедуры, подпадающие под следующие виды деятельности:
Обеспечение качества: Эти действия включают в себя все активные подготовительные мероприятия, такие как разработка стандартов качества и создание контрольных списков процессов, и направленные на повышение точности процесса
Качество control: Процедуры контроля качества относятся к реактивным постпроизводственным усилиям, направленным на выявление любых дефектных товаров или услуг. Примеры включают мониторинг продукции и инспекции.
Примеры включают мониторинг продукции и инспекции.
Короче говоря, руководство по качеству определяет систему управления качеством предприятия, а план качества объясняет, как компания будет выполнять требования к качеству для конкретного продукта или услуги.
XX Анализ со стороны руководства
XX.1 Требование: Высшее руководство проводит запланированные обзоры СМК для обеспечения ее пригодности, адекватности, эффективности и соответствия стратегическому направлению с учетом:
- статуса действий предыдущего руководства обзоры;
- изменения внешних и внутренних вопросов, имеющих отношение к СМК;
- информация о функционировании и результативности системы менеджмента качества, включая тенденции в:
- удовлетворенности потребителей и отзывах соответствующих заинтересованных сторон;
- степень достижения целей в области качества;
- производительность процесса и соответствие продукции и услуг;
- несоответствия и корректирующие действия;
- результаты мониторинга и измерений;
- результаты аудита;
- производительность внешних поставщиков;
- достаточность ресурсов;
- эффективность действий, предпринятых для устранения рисков и возможностей;
- возможности для улучшения.

Результаты анализа со стороны руководства должны включать решения и действия, связанные с:
- возможностями для улучшения;
- любая необходимость внесения изменений в систему менеджмента качества;
- потребности в ресурсах.
Сохраняйте документированную информацию в качестве доказательства результатов анализа со стороны руководства.
ОБРАТИТЕ ВНИМАНИЕ, как в этом разделе непосредственно рассматриваются ТРЕБОВАНИЯ того, что ОЖИДАЕТСЯ от каждого собрания по рассмотрению руководством. В нем ОПИСЫВАЕТСЯ, что должно быть выполнено во время каждого сеанса.
XX.2 Политика: Наши проверки руководства планируются и проводятся на [интервальной] основе. Как минимум, в этих проверках принимают участие:
- Президент
- Вице-президент по развитию бизнеса
- Вице-президент по эксплуатации
- Менеджер по качеству
Планируются проверки со стороны руководства, и готовится повестка дня собрания, содержащая все необходимые материалы.
Результаты анализов со стороны руководства включают действия и решения, касающиеся любых возможностей для улучшения, необходимых изменений в СМК и потребностей в ресурсах.
Это краткое и точное изложение ожиданий от этого конкретного раздела руководства и требований, СПЕЦИАЛЬНО относящихся к собраниям по обзору со стороны руководства.
XX.3 Записи: Протоколы собраний и результаты хранятся в [название записи].
Еще раз — просто и по существу, в этом разделе просто указано, где можно получить доступ к записям совещаний по обзору со стороны руководства. Вы можете следовать тому же формату, что и ваша работа, в соответствии с дополнительными применимыми требованиями для вашей системы и бизнеса.
Работая над сертификацией, очень важно постоянно следить за целью, выгодой и балансом при создании необходимой или вспомогательной документации. Тщательное рассмотрение того, как отражаются политики, процедуры и записи, может помочь организациям убедиться, что они выполняют задачи и соответствуют стандартам, которые они для себя установили.
Об авторе